- ДИАГНОСТИКА
- МРТ
- КТ
- КТ ГОЛОВЫ
- КТ ШЕИ
- КТ ГРУДНОЙ КЛЕТКИ
- КТ БРЮШНОЙ ПОЛОСТИ
- КТ МАЛОГО ТАЗА
- КТ ПОЗВОНОЧНИКА
- КТ СУСТАВОВ
- КТ КОСТЕЙ
- КТ АНГИОГРАФИЯ
- КТ ЗУБОВ
- УЗИ
- УЗИ ОРГАНОВ МАЛОГО ТАЗА
- УЗИ БРЮШНОЙ ПОЛОСТИ
- УЗИ ЗАБРЮШИННОГО ПРОСТРАНСТВА
- УЗИ СЕРДЦА
- УЗИ СОСУДОВ
- УЗИ МЯГКИХ ТКАНЕЙ, НЕРВОВ И ЖЕЛЕЗ
- УЗИ СУСТАВОВ
- УЗИ ГОЛОВЫ
- УЗИ ЛИМФОУЗЛОВ
- УЗИ ПРИ БЕРЕМЕННОСТИ
- УЗИ ПЛОДА
- УЗИ НОВРОЖДЕННОМУ РЕБЕНКУ
- УЗИ ПОСЛЕ АБОРТА
- РЕНТГЕН
- ВРАЧИ
- КАКОЙ ВРАЧ ЛЕЧИТ
- АКУШЕР-ГИНЕКОЛОГ
- АЛЛЕРГОЛОГ
- ВЕРТЕБРОЛОГ
- ВЕСТИБУЛОЛОГ
- ГАСТРОЭНТЕРОЛОГ
- ГЕМАТОЛОГ
- ГИНЕКОЛОГ
- ДЕРМАТОЛОГ
- ДИЕТОЛОГ
- ИГЛОТЕРАПЕВТ
- ИММУНОЛОГ
- ИНФЕКЦИОНИСТ
- КАРДИОЛОГ
- ВРАЧ ЛЕЧЕБНОЙ ФИЗКУЛЬТУРЫ
- МАММОЛОГ
- НЕВРОЛОГ
- НЕЙРОХИРУРГ
- НЕОНАТОЛОГ
- НЕФРОЛОГ
- ОНКОЛОГ
- ОНКОЛОГ-МАММОЛОГ
- ОРТОПЕД
- ОРТОПЕД-ХИРУРГ
- ОТОЛАРИНГОЛОГ
- ОФТАЛЬМОЛОГ
- ОСТЕОПАТ
- ПЕДИАТР
- ПРОКТОЛОГ
- ПСИХИАТР
- ПСИХОТЕРАПЕВТ
- ПУЛЬМОНОЛОГ
- РЕВМАТОЛОГ
- РЕФЛЕКСОТЕРАПЕВТ
- СЕКСОЛОГ
- СОМНОЛОГ
- СОСУДИСТЫЙ ХИРУРГ
- СПОРТИВНЫЙ ВРАЧ
- ТЕРАПЕВТ
- ТРАВМАТОЛОГ
- ТРИХОЛОГ
- УРОЛОГ
- ФИЗИОТЕРАПЕВТ
- ФЛЕБОЛОГ
- ФТИЗИАТР
- ВРАЧ ФУНКЦИОНАЛЬНОЙ ДИАГНОСТИКИ
- ХИРУРГ
- ЭНДОКРИНОЛОГ
- ЭНДОСКОПИСТ
- ЭПИЛЕПТОЛОГ
- СПОРТИВНЫЙ МАССАЖИСТ
- ГЕПАТОЛОГ
- ПАРАЗИТОЛОГ
- МАНУАЛЬНЫЙ ТЕРАПЕВТ
- СЕМЕЙНЫЙ ПСИХОЛОГ
- ВРАЧ ОБЩЕЙ ПРАКТИКИ
- ПРОФПАТОЛОГ-ТЕРАПЕВТ
- АНДРОЛОГ
- АНГИОЛОГ
- АРИТМОЛОГ
- АРТРОЛОГ
- БРОНХОЛОГ
- ВЕНЕРОЛОГ
- ГЕМОСТАЗИОЛОГ
- ГИРУДОТЕРАПЕВТ
- ДИАБЕТОЛОГ
- КИНЕЗИОЛОГ
- РАДИОТЕРАПЕВТ
- РЕПРОДУКТОЛОГ
- СУРДОЛОГ
- ФОНИАТР
- ХИМИОТЕРАПЕВТ
- СКИДКИ
- НА КАРТЕ
- МРТ РЯДОМ (поиск по району)
- АДМИРАЛТЕЙСКИЙ РАЙОН
- ВАСИЛЕОСТРОВСКИЙ РАЙОН
- ВЫБОРГСКИЙ РАЙОН
- КАЛИНИНСКИЙ РАЙОН
- КИРОВСКИЙ РАЙОН
- КОЛПИНСКИЙ РАЙОН
- КРАСНОГВАРДЕЙСКИЙ РАЙОН
- КРАСНОСЕЛЬСКИЙ РАЙОН
- КРОНШТАДТСКИЙ РАЙОН
- КУРОРТНЫЙ РАЙОН
- МОСКОВСКИЙ РАЙОН
- НЕВСКИЙ РАЙОН
- ПЕТРОГРАДСКИЙ РАЙОН
- ПЕТРОДВОРЦОВЫЙ РАЙОН
- ПРИМОРСКИЙ РАЙОН
- ПУШКИНСКИЙ РАЙОН
- ФРУНЗЕНСКИЙ РАЙОН
- ЦЕНТРАЛЬНЫЙ РАЙОН
- ЛЕН. ОБЛАСТЬ
- КТ и МСКТ РЯДОМ (поиск по району)
- АДМИРАЛТЕЙСКИЙ РАЙОН
- ВАСИЛЕОСТРОВСКИЙ РАЙОН
- ВЫБОРГСКИЙ РАЙОН
- КАЛИНИНСКИЙ РАЙОН
- КИРОВСКИЙ РАЙОН
- КОЛПИНСКИЙ РАЙОН
- КРАСНОГВАРДЕЙСКИЙ РАЙОН
- КРАСНОСЕЛЬСКИЙ РАЙОН
- КРОНШТАДТСКИЙ РАЙОН
- КУРОРТНЫЙ РАЙОН
- МОСКОВСКИЙ РАЙОН
- НЕВСКИЙ РАЙОН
- ПЕТРОГРАДСКИЙ РАЙОН
- ПЕТРОДВОРЦОВЫЙ РАЙОН
- ПРИМОРСКИЙ РАЙОН
- ПУШКИНСКИЙ РАЙОН
- ФРУНЗЕНСКИЙ РАЙОН
- ЦЕНТРАЛЬНЫЙ РАЙОН
- ЛЕН. ОБЛАСТЬ
- МРТ АДРЕСА БОЛЬНИЦ В СПБ
- МРТ РЯДОМ (поиск по району)
Адреса и стоимость цитокиногенетической терапии в СПБ
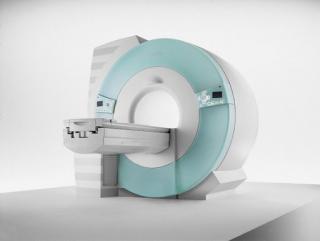
Услуга лечения онкологии
Услуга лечебного сопровождения для пациентов с онкологией — это индивидуальная комплексная помощь, которая может включать:
 Лучшиие онкологидоступ к ведущим специалистам Санкт-Петербурга, которые подберут современные схемы терапии и проконтролируют эффективность лечения на каждом этапе.
Лучшиие онкологидоступ к ведущим специалистам Санкт-Петербурга, которые подберут современные схемы терапии и проконтролируют эффективность лечения на каждом этапе. Госпитализация или дневной стационарвозможность пройти лечение в комфортных условиях ведущих онкологических центров Санкт-Петербурга.
Госпитализация или дневной стационарвозможность пройти лечение в комфортных условиях ведущих онкологических центров Санкт-Петербурга. Персональный протокол леченияразработка индивидуальной стратегии терапии с учётом типа опухоли, стадии заболевания, генетических особенностей, сопутствующих состояний и истории предыдущего лечения.
Персональный протокол леченияразработка индивидуальной стратегии терапии с учётом типа опухоли, стадии заболевания, генетических особенностей, сопутствующих состояний и истории предыдущего лечения. Второе независимое мнениеэкспертная оценка диагноза и лечебной тактики от ведущих онкологов, позволяющая подтвердить правильность выбранной стратегии, получить дополнительные варианты терапии, избежать ошибок и повысить шансы на успешный результат благодаря объективному профессиональному взгляду стороннего специалиста.
Второе независимое мнениеэкспертная оценка диагноза и лечебной тактики от ведущих онкологов, позволяющая подтвердить правильность выбранной стратегии, получить дополнительные варианты терапии, избежать ошибок и повысить шансы на успешный результат благодаря объективному профессиональному взгляду стороннего специалиста.
Лучшие специалисты в Санкт-Петербурге с рейтингом 4.5+
Последние отзывы
Что такое цитогенетическая терапия?
Цитогенетическая терапия при лечении рака представляет собой группу высокотехнологичных методов, при которых в лечебный процесс включаются клетки или лекарственные подходы, основанные на точном воздействии на генетический и хромосомный аппарат опухолевых и иммунных клеток, чаще всего речь идёт о введении собственных лимфоцитов, модифицированных в лаборатории для распознавания опухолевых мишеней, либо о применении программ, построенных на учёте выявленных цитогенетических аномалий при выборе лекарств и трансплантационных стратегий.
Показания
Цитокинотерапия рассматривается как вариант онколечения при:
- отдельных формах лейкозов, лимфом и множества миеломы с неблагоприятным течением для стандартных схем
- в рамках специализированных программ при солидных опухолях, когда выявляются чётко определённые мишени и имеется доступ к центру клеточной терапии.
Решение о целесообразности терапии принимается на консилиуме врачей после анализа цитогенетического и молекулярного профиля, предшествующего лечения, общего состояния и сопутствующих заболеваний, при этом оцениваются как потенциальные преимущества, так и риски интенсивных и пока ещё ограниченно доступных методик.
Виды цитокинотерапии
Цитогенетическая терапия на основе CAR-T-клеток при В-клеточных лимфобластных лейкозах и диффузной В-крупноклеточной лимфоме строится на предварительном иммунoфенотипировании и цитогенетическом анализе с подтверждением В-клеточной природы опухоли и сопутствующих хромосомных аномалий, затем выполняется лейкаферез для заготовки лимфоцитов, в лаборатории проводится генетическая модификация Т-клеток с введением гена химерного антигенного рецептора, ориентированного на CD19 или другой В-клеточный маркёр, после размножения модифицированные клетки возвращаются пациенту на фоне лимфодеплетирующей химиотерапии, весь протокол сопровождается строгим мониторингом признаков цитокинового высвобождения и нейротоксичности.
Цитокинотерапия на основе CAR-T-клеток при множественной миеломе ориентирована на экспрессию антигенов, таких как BCMA, что подтверждается иммуногистохимически и молекулярно-генетически, после подтверждения пригодности мишени проводится лейкаферез, генетическая модификация Т-клеток и их экспансия, перед инфузией назначается лимфодеплетирующий режим, затем целевой клеточный продукт вводится внутривенно, дальнейшее ведение основано на динамике парапротеина, минимально остаточной болезни и развитии специфических токсичностей, включая цитокиновый синдром, инфекции и гипогаммаглобулинемию.
Цитокиногенетическая терапия с использованием CAR-T-клеток, ориентированных на редкие или индивидуализированные мишени, применяется в рамках специализированных программ при наличии уникальных антигенов, связанных с конкретными хромосомными перестройками или экспрессией неоантигенов, по результатам расширенного генетического профилирования выбираются кандидаты для индивидуального конструирования рецептора, разрабатывается персонализированный производственный протокол, в котором учитываются как цитогенетические особенности опухоли, так и риск перекрёстного поражения нормальных тканей, после инфузии проводится длительное наблюдение за персистенцией модифицированных клеток и возможными отдалёнными осложнениями.
Цитогенетически-ориентированная Т-клеточная терапия с модифицированным Т-клеточным рецептором предполагает создание Т-лимфоцитов, узнающих специфические пептиды на комплексе HLA, кодируемые опухоль-ассоциированными или фьюзионными генами, выявляемыми по результатам цитогенетики и секвенирования, отбор кандидатов включает подтверждение экспрессии мишени и соответствующего HLA-аллеля, после лейкафереза Т-клетки модифицируются, размножаются и возвращаются внутривенно, протокол особенно строг по части оценки риска перекрёстных реакций с нормальными тканями и требует тонкой дозиметрии клеточного продукта.
Цитогенетически-направленная терапия с использованием модифицированных гемопоэтических стволовых клеток разрабатывается при отдельных лейкозах и наследственных предрасположенностях, когда задача состоит в замене патологического клона генетически скорректированным, на этапе подготовки выполняется детальный цитогенетический и молекулярный анализ, затем в аутологичных стволовых клетках проводится коррекция определённой мутации или фьюзионного гена, после миелоаблативного или уменьшенного кондиционирования откорректированный клеточный материал возвращается, дальнейшее наблюдение включает оценку восстановления кроветворения, глубины ремиссии и риска вторичных клонов.
Цитогенетически-стратифицированная трансплантация гемопоэтических стволовых клеток при острых лейкозах и миелодиспластическом синдроме позволяет использовать цитогенетический риск для выбора протокола кондиционирования и типа донора, при неблагоприятных кариотипах трансплантация рассматривается уже на этапе первой ремиссии, подбирается режим с учётом возраста, сопутствующих заболеваний и риска рецидива, проводится аллогенная пересадка с контролем химеризма и минимально остаточной болезни с использованием молекулярно-генетических и цитогенетических методов, по результатам наблюдения принимаются решения о дополнительной иммунной модификации, донорских лимфоцитах или изменении иммуносупрессии.
Цитогенетически-ориентированная лекарственная терапия, включающая ингибиторы тирозинкиназ и другие таргетные препараты, хотя и относится к таргетным подходам, во многих протоколах встроена как цитогенетический компонент, поскольку именно наличие определённых хромосомных перестроек, таких как BCR-ABL, FLT3-ITD или других аномалий, определяет выбор препарата, при этом схемы строятся с учётом кариотипа и динамики цитогенетического ответа, глубина устранения аномальных клонов по методу FISH или ПЦР служит критерием успешности и основанием для деэскалации или интенсификации лечения.
Помощь онкопациентам
Подготовительная лимфодеплетирующая терапия перед введением цитогенетически-модифицированных клеток включает использование комбинаций цитостатиков и иногда антител, которые снижают количество конкурирующих лимфоцитов, создают пространство для приживания введённого клона и уменьшают риск немедленного отторжения, дозы и состав подбираются с учётом предшествующего лечения, функции костного мозга, печени и почек, режим проводится за несколько дней до инфузии клеток, на протяжении этого периода оцениваются показатели крови и состояние слизистых, проводится профилактика инфекций и синдрома лизиса опухоли.
Терапия, направленная на контроль синдрома высвобождения цитокинов, является центральным элементом сопровождения CAR-T и других цитогенетических клеточных подходов, сразу после инфузии начинают регулярный мониторинг температуры, артериального давления, сатурации и лабораторных маркёров воспаления, при первых признаках синдрома лёгкой степени применяются антипиретики и инфузионная поддержка, при нарастании симптомов используются блокаторы интерлейкина-6, такие как тоцилизумаб, и глюкокортикостероиды в тщательно выверенных дозах, при тяжёлых формах организуется перевод в отделение интенсивной терапии с вазопрессорной поддержкой и контролем органной функции.
Профилактика и лечение нейротоксичности проводится параллельно с наблюдением за цитокиновым синдромом, ежедневно оцениваются сознание, речь, координация, возможные судорожные проявления, при лёгких когнитивных нарушениях ограничиваются наблюдением и коррекцией электролитных и метаболических параметров, при появлении спутанности сознания, выраженной дезориентации или судорог назначаются глюкокортикостероиды, противосудорожные препараты и, при необходимости, проводится нейровизуализация, режим введения модифицированных клеток и последующих курсов корректируется с учётом перенесённой нейротоксичности.
Инфекционная профилактика и терапия при цитогенетических подходах усиливаются из-за комбинации глубокой лимфопении, нейтропении и функционального дефицита В- и Т-клеток, ещё до старта вмешательства проводится санация хронических очагов инфекции, скрининг на вирусные гепатиты, ВИЧ-инфекцию и латентный туберкулёз, в период тяжёлой цитопении применяются антибактериальные и противогрибковые препараты по профилактическим схемам, при выраженном В-клеточном истощении и гипогаммаглобулинемии проводится заместительная терапия внутривенным иммуноглобулином, при появлении лихорадки немедленно начинают диагностический поиск и эмпирическое лечение.
Гематологическая поддерживающая терапия при цитогенетической терапии включает регулярный контроль общего анализа крови, при тяжёлой нейтропении использование колониестимулирующих факторов, при выраженной анемии и тромбоцитопении трансфузии эритроцитарной и тромбоцитарной массы, при длительной аплазии костного мозга тщательный баланс между интенсивностью антиинфекционной профилактики и риском токсичности, решение о повторных вмешательствах или изменении программы принимается на основе скорости восстановления кроветворения и устойчивости ремиссии.
Нутритивная поддержка ориентирована на пациентов с тяжёлым предшествующим лечением и выраженной кахексией, до начала курса оцениваются индекс массы тела, альбумин, преальбумин, выраженность саркопении и функциональный статус, формируется программа высокобелкового и высококалорийного питания с использованием специализированных смесей, при необходимости рассматривается зондовое или парентеральное питание, параллельно контролируются электролиты, гликемия и показатели почечной и печёночной функции, что особенно важно на фоне цитокинового ответа и интенсивной поддерживающей терапии.
Тромбоэмболическая профилактика осуществляется с учётом сочетания онкологического процесса, вынужденной малоподвижности, катетеров и системного воспалительного ответа, по шкалам оценивается индивидуальный риск венозных тромбозов, при высоком уровне риска назначаются профилактические дозы антикоагулянтов и компрессионный трикотаж, при появлении одностороннего отёка конечности, боли в икроножной мышце или внезапной одышки организуется срочная диагностика и коррекция тактики, при этом сохраняется баланс между риском кровотечений на фоне тромбоцитопении и необходимостью предотвращать тромботические события.
Психоонкологическая поддержка особенно значима из-за экспериментального или высокотехнологичного характера вмешательства, пациенту заранее подробно объясняются цели, этапы, возможные осложнения и неопределённость отдалённых результатов, после завершения активной фазы проводится оценка когнитивного статуса, эмоционального фона и уровня повседневной активности, формируется программа мягкой физической реабилитации, поддержки сна и настроения, привлекаются родственники, что помогает пройти через сложный этап интенсивной терапии и адаптироваться к жизни после высокотехнологичного лечения.
Какие врачи могут быть вовлечены
- Гематолог при гемобластозах выполняет первичную оценку заболевания, интерпретирует цитогенетические и молекулярные данные, определяет показания к цитогенетической терапии, координирует этапы лейкафереза, лимфодеплетирующей подготовки и последующего наблюдения, принимает решения о сопутствующих химиопротоколах и трансфузионной поддержке.
- Онколог при солидных опухолях и сложных клинических ситуациях оценивает общее состояние, стадию и предшествующее лечение, инициирует направление в центр клеточной и цитогенетической терапии, участвует в консилиумном обсуждении целесообразности вмешательства и планирует дальнейшую лекарственную тактику после проведения высокотехнологичного этапа.
- Врач по клеточной терапии или трансплантолог курирует весь путь цитогенетического продукта, отвечает за выбор платформы (CAR-T, модифицированные Т-клеточные рецепторы, генетически скорректированные стволовые клетки), контролирует производство, хранение и введение, организует мониторинг цитокинового синдрома, нейротоксичности и отдалённой безопасности.
- Генетик и цитогенетик проводят кариотипирование, FISH-исследования и молекулярные тесты, определяют наличие мишеней и неблагоприятных аномалий, оценивают минимально остаточную болезнь и динамику клонов после терапии, предоставляют данные для стратификации риска и корректировки программы.
- Специалист по аферезу и трансфузиолог отвечают за проведение лейкафереза, заготовку и криоконсервирование клеточного материала, планирование и выполнение переливаний эритроцитарных и тромбоцитарных компонентов, контроль совместимости и профилактику трансфузионных реакций.
- Врач реаниматолог и специалист по интенсивной терапии обеспечивают ведение пациентов с тяжёлым цитокиновым синдромом, гемодинамической нестабильностью и полиорганной дисфункцией, организуют мониторинг жизненно важных функций, вазоактивную поддержку, респираторную терапию и коррекцию метаболических нарушений.
- Невролог ведёт пациентов с признаками нейротоксичности, оценивает когнитивный статус, речь, координацию и наличие судорожных проявлений, назначает нейровизуализацию и противосудорожную терапию, участвует в решении вопроса о модификации программы при выраженных неврологических осложнениях.
- Инфекционист формирует схемы первичной и вторичной профилактики бактериальных, вирусных и грибковых осложнений, ведёт пациентов с лихорадкой неясного генеза и тяжёлыми инфекциями на фоне иммунодефицита, выбирает противомикробные препараты с учётом предшествующей терапии и местного профиля резистентности.
- Психоонколог и специалист по реабилитации помогают пациенту и семье подготовиться к этапу высокотехнологичного лечения, снижают уровень тревоги, формируют стратегии адаптации и восстановительные программы, поддерживают качество жизни в период длительного наблюдения после цитогенетической терапии.
Какие обследования назначаются
- Лабораторные обследования перед цитогенетической терапией включают общий анализ крови с лейкоцитарной формулой и тромбоцитами, развёрнутый биохимический профиль с оценкой функции печени и почек, уровня электролитов, глюкозы, альбумина, ферритина, лактатдегидрогеназы и маркёров воспаления, коагулограмму с международным нормализованным отношением и фибриногеном, по этим данным оцениваются резервы костного мозга, риск кровотечений, вероятность синдрома лизиса и переносимость последующих этапов.
- Цитогенетические и молекулярно-генетические исследования включают классическое кариотипирование, FISH-диагностику ключевых хромосомных перестроек, ПЦР и высокопроизводительное секвенирование для выявления драйверных мутаций и отслеживания минимально остаточной болезни, результаты используются для отбора на цитогенетическую терапию и для оценки глубины ответа.
- Иммунoфенотипирование костного мозга и периферической крови методом проточной цитометрии подтверждает принадлежность опухолевого клона к определённой линии, определяет уровни экспрессии целевых антигенов, служит основой для выбора CAR-конструкции или модифицированного Т-клеточного рецептора, а также используется для динамического мониторинга после инфузии.
- Исследование костного мозга в виде миелограммы и трепанобиопсии позволяет оценить степень инфильтрации, резерв нормального кроветворения и сопутствующие изменения стромы, по этим данным планируется интенсивность лимфодеплетирующей терапии и объём поддерживающих мероприятий.
- Скрининг инфекций включает тесты на вирусные гепатиты B и C, ВИЧ-инфекцию, цитомегаловирус, вирус Эпштейна–Барр и латентный туберкулёз, при необходимости дополнительные серологические и ПЦР-исследования, результаты определяют необходимость противовирусной профилактики и тактику при возможной реактивации.
- Кардиологическое и респираторное обследование включает электрокардиографию, эхокардиографию, оценку функции внешнего дыхания, иногда тесты с нагрузкой, данные используются для стратификации риска на фоне цитокинового ответа, выбора стратегии инфузионной терапии и определения допустимой интенсивности сопутствующей медикации.
- Визуализационные методы - КТ, МРТ и ПЭТ-КТ применяются для стадирования и оценки объёма опухолевого процесса, выявления очагов вне костного мозга, контроля возможных инфекционных осложнений и оценки динамики после лечения, результаты влияют на интерпретацию маркёров и план последующих обследований.
- В период наблюдения онкобольному выполняются повторные лабораторные и генетические исследования для контроля минимально остаточной болезни, оценки химеризма при трансплантации и раннего выявления вторичных клонов или поздних осложнений.
Что важно знать пациентам
Как подбирается препарат?
Путь от отбора до введения цитогенетического продукта включает подтверждение диагноза с детальным цитогенетическим и молекулярным исследованием, принятие консилиумного решения о целесообразности цитогенетической терапии, проведение лейкафереза и заготовку клеточного материала, лабораторную модификацию и экспансию клеток, период ожидания с поддерживающим или «мостовым» лечением, затем проведение лимфодеплетирующей терапии и внутривенную инфузию подготовленного продукта с последующим этапом интенсивного наблюдения в стационаре, где регулярно оцениваются жизненно важные показатели, лабораторные параметры и признаки специфической токсичности.
Какие риски и побочные эффекты?
Для терапии характерны риски синдрома высвобождения цитокинов с лихорадкой, падением артериального давления, одышкой и нарушением функции органов, нейротоксичности с изменением речи, поведения, сознания и возможными судорожными приступами, выраженной цитопении с высоким риском инфекций и кровотечений, а также гипогаммаглобулинемии и поздних иммунных нарушений, немедленного обращения требуют высокая стойкая лихорадка, одышка, чувство нехватки воздуха, выраженная слабость с головокружением, любые внезапные изменения речи, ориентации, поведения, судорожные эпизоды, кровотечения, резкое уменьшение объёма мочи и интенсивные боли в грудной клетке или животе.
Как увеличить безопасность и эффективность лечения?
Безопасность и эффективность цитокиногенетической терапии повышаются при строгом выполнении рекомендаций по пребыванию в стационаре и амбулаторному наблюдению, точном приходе на все обследования и процедуры, полном указании перенесённых заболеваний, внимательном отношении к любым изменениям самочувствия и незамедлительном информировании лечащей команды о настораживающих симптомах, соблюдении рекомендованного питьевого режима и гигиенических мер, участии членов семьи в наблюдении и поддержке, готовности к временным ограничениям в контактах и поездках, а также при принятии необходимости длительного наблюдения даже после завершения активной фазы лечения, поскольку отдалённая безопасность и устойчивость эффекта требуют регулярного контроля.






































































