- ДИАГНОСТИКА
- МРТ
- КТ
- КТ ГОЛОВЫ
- КТ ШЕИ
- КТ ГРУДНОЙ КЛЕТКИ
- КТ БРЮШНОЙ ПОЛОСТИ
- КТ МАЛОГО ТАЗА
- КТ ПОЗВОНОЧНИКА
- КТ СУСТАВОВ
- КТ КОСТЕЙ
- КТ АНГИОГРАФИЯ
- КТ ЗУБОВ
- УЗИ
- УЗИ ОРГАНОВ МАЛОГО ТАЗА
- УЗИ БРЮШНОЙ ПОЛОСТИ
- УЗИ ЗАБРЮШИННОГО ПРОСТРАНСТВА
- УЗИ СЕРДЦА
- УЗИ СОСУДОВ
- УЗИ МЯГКИХ ТКАНЕЙ, НЕРВОВ И ЖЕЛЕЗ
- УЗИ СУСТАВОВ
- УЗИ ГОЛОВЫ
- УЗИ ЛИМФОУЗЛОВ
- УЗИ ПРИ БЕРЕМЕННОСТИ
- УЗИ ПЛОДА
- УЗИ НОВРОЖДЕННОМУ РЕБЕНКУ
- УЗИ ПОСЛЕ АБОРТА
- РЕНТГЕН
- ВРАЧИ
- КАКОЙ ВРАЧ ЛЕЧИТ
- АКУШЕР-ГИНЕКОЛОГ
- АЛЛЕРГОЛОГ
- ВЕРТЕБРОЛОГ
- ВЕСТИБУЛОЛОГ
- ГАСТРОЭНТЕРОЛОГ
- ГЕМАТОЛОГ
- ГИНЕКОЛОГ
- ДЕРМАТОЛОГ
- ДИЕТОЛОГ
- ИГЛОТЕРАПЕВТ
- ИММУНОЛОГ
- ИНФЕКЦИОНИСТ
- КАРДИОЛОГ
- ВРАЧ ЛЕЧЕБНОЙ ФИЗКУЛЬТУРЫ
- МАММОЛОГ
- НЕВРОЛОГ
- НЕЙРОХИРУРГ
- НЕОНАТОЛОГ
- НЕФРОЛОГ
- ОНКОЛОГ
- ОНКОЛОГ-МАММОЛОГ
- ОРТОПЕД
- ОРТОПЕД-ХИРУРГ
- ОТОЛАРИНГОЛОГ
- ОФТАЛЬМОЛОГ
- ОСТЕОПАТ
- ПЕДИАТР
- ПРОКТОЛОГ
- ПСИХИАТР
- ПСИХОТЕРАПЕВТ
- ПУЛЬМОНОЛОГ
- РЕВМАТОЛОГ
- РЕФЛЕКСОТЕРАПЕВТ
- СЕКСОЛОГ
- СОМНОЛОГ
- СОСУДИСТЫЙ ХИРУРГ
- СПОРТИВНЫЙ ВРАЧ
- ТЕРАПЕВТ
- ТРАВМАТОЛОГ
- ТРИХОЛОГ
- УРОЛОГ
- ФИЗИОТЕРАПЕВТ
- ФЛЕБОЛОГ
- ФТИЗИАТР
- ВРАЧ ФУНКЦИОНАЛЬНОЙ ДИАГНОСТИКИ
- ХИРУРГ
- ЭНДОКРИНОЛОГ
- ЭНДОСКОПИСТ
- ЭПИЛЕПТОЛОГ
- СПОРТИВНЫЙ МАССАЖИСТ
- ГЕПАТОЛОГ
- ПАРАЗИТОЛОГ
- МАНУАЛЬНЫЙ ТЕРАПЕВТ
- СЕМЕЙНЫЙ ПСИХОЛОГ
- ВРАЧ ОБЩЕЙ ПРАКТИКИ
- ПРОФПАТОЛОГ-ТЕРАПЕВТ
- АНДРОЛОГ
- АНГИОЛОГ
- АРИТМОЛОГ
- АРТРОЛОГ
- БРОНХОЛОГ
- ВЕНЕРОЛОГ
- ГЕМОСТАЗИОЛОГ
- ГИРУДОТЕРАПЕВТ
- ДИАБЕТОЛОГ
- КИНЕЗИОЛОГ
- РАДИОТЕРАПЕВТ
- РЕПРОДУКТОЛОГ
- СУРДОЛОГ
- ФОНИАТР
- ХИМИОТЕРАПЕВТ
- СКИДКИ
- НА КАРТЕ
- МРТ РЯДОМ (поиск по району)
- АДМИРАЛТЕЙСКИЙ РАЙОН
- ВАСИЛЕОСТРОВСКИЙ РАЙОН
- ВЫБОРГСКИЙ РАЙОН
- КАЛИНИНСКИЙ РАЙОН
- КИРОВСКИЙ РАЙОН
- КОЛПИНСКИЙ РАЙОН
- КРАСНОГВАРДЕЙСКИЙ РАЙОН
- КРАСНОСЕЛЬСКИЙ РАЙОН
- КРОНШТАДТСКИЙ РАЙОН
- КУРОРТНЫЙ РАЙОН
- МОСКОВСКИЙ РАЙОН
- НЕВСКИЙ РАЙОН
- ПЕТРОГРАДСКИЙ РАЙОН
- ПЕТРОДВОРЦОВЫЙ РАЙОН
- ПРИМОРСКИЙ РАЙОН
- ПУШКИНСКИЙ РАЙОН
- ФРУНЗЕНСКИЙ РАЙОН
- ЦЕНТРАЛЬНЫЙ РАЙОН
- ЛЕН. ОБЛАСТЬ
- КТ и МСКТ РЯДОМ (поиск по району)
- АДМИРАЛТЕЙСКИЙ РАЙОН
- ВАСИЛЕОСТРОВСКИЙ РАЙОН
- ВЫБОРГСКИЙ РАЙОН
- КАЛИНИНСКИЙ РАЙОН
- КИРОВСКИЙ РАЙОН
- КОЛПИНСКИЙ РАЙОН
- КРАСНОГВАРДЕЙСКИЙ РАЙОН
- КРАСНОСЕЛЬСКИЙ РАЙОН
- КРОНШТАДТСКИЙ РАЙОН
- КУРОРТНЫЙ РАЙОН
- МОСКОВСКИЙ РАЙОН
- НЕВСКИЙ РАЙОН
- ПЕТРОГРАДСКИЙ РАЙОН
- ПЕТРОДВОРЦОВЫЙ РАЙОН
- ПРИМОРСКИЙ РАЙОН
- ПУШКИНСКИЙ РАЙОН
- ФРУНЗЕНСКИЙ РАЙОН
- ЦЕНТРАЛЬНЫЙ РАЙОН
- ЛЕН. ОБЛАСТЬ
- МРТ АДРЕСА БОЛЬНИЦ В СПБ
- МРТ РЯДОМ (поиск по району)
Адреса и стоимость лучевой терапии в СПБ
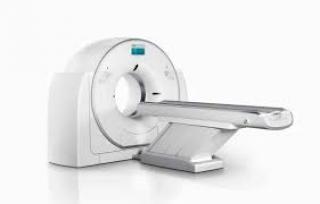
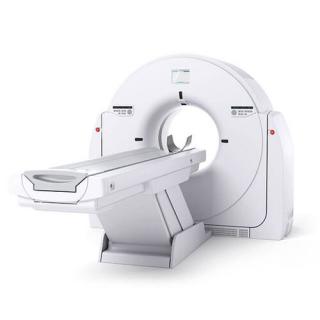
Услуга лечения онкологии
Услуга лечебного сопровождения для пациентов с онкологией — это индивидуальная комплексная помощь, которая может включать:
 Лучшиие онкологидоступ к ведущим специалистам Санкт-Петербурга, которые подберут современные схемы терапии и проконтролируют эффективность лечения на каждом этапе.
Лучшиие онкологидоступ к ведущим специалистам Санкт-Петербурга, которые подберут современные схемы терапии и проконтролируют эффективность лечения на каждом этапе. Госпитализация или дневной стационарвозможность пройти лечение в комфортных условиях ведущих онкологических центров Санкт-Петербурга.
Госпитализация или дневной стационарвозможность пройти лечение в комфортных условиях ведущих онкологических центров Санкт-Петербурга. Персональный протокол леченияразработка индивидуальной стратегии терапии с учётом типа опухоли, стадии заболевания, генетических особенностей, сопутствующих состояний и истории предыдущего лечения.
Персональный протокол леченияразработка индивидуальной стратегии терапии с учётом типа опухоли, стадии заболевания, генетических особенностей, сопутствующих состояний и истории предыдущего лечения. Второе независимое мнениеэкспертная оценка диагноза и лечебной тактики от ведущих онкологов, позволяющая подтвердить правильность выбранной стратегии, получить дополнительные варианты терапии, избежать ошибок и повысить шансы на успешный результат благодаря объективному профессиональному взгляду стороннего специалиста.
Второе независимое мнениеэкспертная оценка диагноза и лечебной тактики от ведущих онкологов, позволяющая подтвердить правильность выбранной стратегии, получить дополнительные варианты терапии, избежать ошибок и повысить шансы на успешный результат благодаря объективному профессиональному взгляду стороннего специалиста.
Лучшие специалисты в Санкт-Петербурге с рейтингом 4.5+
Последние отзывы
Что такое лучевая терапия при раке брюшной полости?
Лучевая терапия при раке брюшной полости представляет собой локальное воздействие ионизирующим излучением на опухолевые очаги желудка, поджелудочной железы, печени, толстого кишечника, забрюшинных лимфоузлов либо перитонеальных имплантатов. План лечения формируют на основании КТ, МРТ, ПЭТ-КТ с учётом точного расположения опухоли, соседних органов и уже перенесённых операций. Цели различаются: у одних пациентов добиваются максимального местного контроля и уменьшения опухолевой массы, у других — прежде всего уменьшения боли, кровотечений, асцита и улучшения повседневного функционирования.
Варианты радиотерапии карциномы брюшной полости
Трёхмерно-конформная лучевая терапия послеоперационного ложа при раке желудка и раке кардии назначается как адъювантный этап у пациентов с высоким риском местного рецидива, например при поражении регионарных лимфоузлов или минимально-позитивных краях резекции. По данным КТ-планирования очерчивается зона анастомоза, ложе удалённого желудка или кардии, парагастральные и парааортальные лимфоколлекторы, а также критические органы – печень, почки, спинной мозг, тонкая кишка. Суммарная доза обычно составляет 45–50 Гр по 1,8–2 Гр на поле брюшной полости с возможным локальным усилением до 54 Гр на зону наибольшего риска, при этом дозовые ограничения для печени и почек выдерживаются максимально строго, чтобы снизить вероятность лучевого гепатита и нефропатии.
Интенсивно-модулированная лучевая терапия и VMAT при локально-распространённом раке поджелудочной железы головки или тела брюшной локализации используется для формирования сложного распределения дозы излучения вокруг двенадцатиперстной кишки, желудка, печени и крупных сосудов. На этапе планирования по КТ и МРТ очерчивается опухолевый массив, вовлечение чревного ствола, верхней брыжеечной артерии, портальной вены и регионарных лимфоузлов, после чего создаются дуговые поля с модуляцией интенсивности. Суммарные дозы обычно составляют 50–54 Гр при стандартном фракционировании, а при одновременной химиотерапии часть схем ограничивается 45–50 Гр, что позволяет улучшить местный контроль при нерезектабельном раке поджелудочной железы и удержать токсичность со стороны тонкой кишки и желудка на приемлемом уровне.
Химиолучевая терапия брюшной полости при раке желудка, кардии и раке поджелудочной железы нерезектабельных или гранично-резектабельных стадий выстраивается как комплексный протокол, в котором наружное облучение сочетается с системной химиотерапией. Лучевая часть ориентируется на первичную опухоль и регионарные лимфоколлекторы, суммарные дозы чаще составляют 45–50 Гр, а фоновое введение фторпиримидинов или других препаратов усиливает радиочувствительность опухолевых клеток. Данная схема используется для уменьшения объёма опухоли до операций, для усиления локального контроля при невозможности радикального вмешательства, а также при воспалительном компоненте или выраженном лимфогенном распространении в пределах брюшной полости.
Стереотаксическая лучевая терапия (SBRT) при ограниченных метастазах в печени, надпочечниках или забрюшинных лимфоузлах при раке желудка, раке поджелудочной железы и раке толстой кишки брюшной локализации формируется как высокодозный режим с малым числом фракций. Планирование выполняется по КТ с возможным слиянием ПЭТ/КТ и МРТ, очаги очерчиваются с минимальной маржой, а вокруг создаются стереотаксические поля, позволяющие подвести 30–50 Гр за 3–5 фракций. Подобный протокол эффективен при олигометастатическом варианте, когда необходимо добиться длительного местного контроля отдельных очагов в брюшной полости при сохранении достаточного объёма не вовлечённой печёночной паренхимы и защите тонкой кишки.
Протонная радиотерапия верхнего отдела брюшной полости при раке поджелудочной железы, раке желудка с прорастанием в малый сальник и при отдельных вариантах рака печени используется в центрах, где доступна протонная технология, для снижения нагрузки на тонкую кишку, желудок и почки. При планировании создаются протонные пучки с заданной глубиной и формой пика Брэгга, в который попадает опухолевый объём в зоне поджелудочной железы, ворот печени или малой кривизны желудка, а дистальная доза в направлении позвоночника и почек резко падает. Суммарные дозы сопоставимы с фотонной терапией – порядка 50–60 Гр(экв), однако за счёт особенностей распределения удаётся расширить объём облучения и повысить эскалацию дозы на опухоль при более мягкой токсичности со стороны органов брюшной полости.
Облучение брюшной полости при перитонеальном канцероматозе, например при раке желудка или раке яичников с множественными имплантатами по брюшине, используется ограниченно и чаще в рамках паллиативных протоколов или клинических исследований. План формируется на всю брюшную полость с захватом куполов диафрагмы, латеральных каналов и малого таза, при этом критически важен контроль дозы на почки, печень и костный мозг. Суммарные дозы обычно невысоки – порядка 20–30 Гр в фракционированном режиме, задача подобных схем состоит в уменьшении объёма опухолевых имплантатов, облегчении асцита и болевого синдрома без выраженного усиления системной токсичности.
Паллиативные фракционированные схемы облучения ограниченных зон брюшной полости при раке желудка, раке поджелудочной железы, раке толстой кишки и при массивных лимфоузловых конгломератах используются для контроля боли, кровотечения, частичной обструкции и компрессии нервных структур. На этапе планирования выбирается симптомная зона – опухоль желудка, поджелудочной железы, крупный мезентериальный или парааортальный узел, создаётся поле с охватом очага и небольшим запасом по длине и ширине. Суммарные дозы варьируют от однократных 8 Гр до курсов 20–30 Гр за 5–10 фракций, а цель подобных протоколов заключается в быстром облегчении симптомов и улучшении качества жизни при распространённом раке брюшной полости.
Помощь онкобольным
Обезболивание и контроль абдоминального болевого синдрома при облучении брюшной полости выстраиваются вокруг чёткого понимания источника боли: опухолевая инфильтрация, спазм кишечника, панкреатический компонент, постоперационный рубец. Подбирается ступенчатая схема анальгетиков с учётом уже получаемой терапии, оценивается необходимость добавления спазмолитиков, нейропатических средств при вовлечении нервных сплетений. При раке поджелудочной железы обсуждается блокада чревного сплетения, что позволяет снизить дозы системных опиоидов, а при выраженном метеоризме и кишечных коликах корректируется питание и назначаются средства, уменьшающие газообразование и стимуляцию перистальтики.
Нутритивная поддержка строится не на абстрактных советах «питаться правильно», а на конкретной адаптации рациона к типу поражения – желудок, поджелудочная железа, тонкая кишка, толстая кишка. После гастрэктомии или субтотальной резекции требуется дробное питание малыми порциями, ограничение простых сахаров для профилактики «дампинг»-симптомов, иногда добавление специализированных смесей между приёмами пищи. При раке поджелудочной железы оценивается стеаторея, при её наличии вводятся ферментные препараты и жиры перераспределяются в течение дня, а при выраженной анорексии рассматривается краткосрочное зондовое питание или высококалорийные напитки с контролем электролитов и массы тела.
Профилактика и коррекция лучевого энтерита требуют продуманного режима питания и медикаментозной поддержки, а не только рекомендаций «не переедать». За несколько дней до старта курса и в процессе лечения пересматривается рацион: уменьшается грубая клетчатка, ограничиваются бобовые, газированные напитки, избыток молочных продуктов при лактозной недостаточности, острые и сильно жареные блюда. При появлении учащённого стула подключаются противодиарейные препараты по согласованной схеме, пациент обучается восполнять потери жидкости и электролитов с помощью солевых растворов, а при кровянистых примесях или лихорадке обследование не откладывается, чтобы не пропустить осложнённый колит.
Контроль тошноты, рвоты и диспепсии при лучевой терапии верхних отделов брюшной полости решается заранее, а не по факту выраженных жалоб. Перед сеансами при раке желудка и поджелудочной железы назначаются противорвотные препараты с учётом параллельной химиотерапии, уточняется интервал между приёмом пищи и облучением, иногда вводится правило: «лёгкий приём пищи за 2–3 часа до процедуры и небольшой объём жидкости за час». Дополнительно используются ингибиторы протонной помпы или другие антисекреторные средства при выраженной изжоге и ночной боли, а при застойных явлениях в желудке добавляются прокинетики, что уменьшает риск рвоты во время или сразу после сеанса.
Профилактика тромбоэмболических осложнений особенно актуальна у малоподвижных пациентов с асцитом, ожирением, предшествующими операциями и длительными курсами системной терапии. Оценивается индивидуальный риск по стандартным шкалам, при высоких значениях обсуждается назначение низкомолекулярных гепаринов или пероральных антикоагулянтов с учётом функции печени и почек, параллельно подбирается компрессионный трикотаж. Пациента обучают простым упражнениям для стоп и голеней, рекомендуют короткие прогулки по квартире или коридору, объясняют, какие симптомы – односторонний отёк ноги, внезапная одышка, боль в груди – требуют немедленного обращения, даже если курс облучения ещё продолжается.
Уход за кожей и послеоперационными рубцами на передней брюшной стенке направлен на снижение риска лучевого дерматита и замедленного заживления. Заранее оговаривается, что область разметки не трётся жёсткими мочалками, не обрабатывается спиртом и агрессивными антисептиками, для душа выбираются мягкие моющие средства без сильных ароматизаторов. При наличии стомы или дренажей корректируются схемы ухода с учётом облучения: подбираются пластины и мешки, которые меньше травмируют кожу, мониторируется герметичность, при первых признаках мацерации или эрозий подключается специалист по стомам, чтобы избежать инфицирования и проблем с фиксацией систем.
Психологическая и практическая поддержка при лучевой терапии онкологии касается не только страха перед опухолью, но и очень приземлённых вопросов – боли, стула, запахов, усталости, изменения роли в семье. Психоонколог помогает проговорить страхи, связанные с асцитом, худобой, возможной стомой, объясняет, как обсуждать происходящее с близкими, чтобы попросить о помощи без чувства вины. Социальный специалист помогает организовать транспорт на процедуры, оформить уход на дому, подобрать вспомогательные средства (опоры, кресло, специальную подушку), а команда даёт понятные инструкции на случай усиления симптомов между сеансами, чтобы человек не оставался один на один с внезапной болью, рвотой или диареей.
Какие врачи могут быть вовлечены
- Радиотерапевт-онколог выстраивает структуру лучевого лечения при раке желудка, поджелудочной железы, толстой кишки и перитонеальном канцероматозе, соединяя анатомию брюшной полости с реальными симптомами пациента. На этапе планирования именно он решает, ограничиться ли адъювантным облучением ложа опухоли и регионарных лимфоузлов при раке желудка, перейти ли к химиолучевому режиму при нерезектабельном раке поджелудочной железы или выбрать стереотаксический курс на отдельные метастазы в печени. В процессе лечения радиотерапевт отслеживает реакции со стороны кишечника, печени, желудка, ежедневно сравнивает план с фактическим состоянием, меняет объём поля или схему фракционирования, если диарея, боли, снижение массы тела начинают перевешивать пользу от дальнейшей эскалации дозы.
- Клинический онколог формирует общий маршрут: от первых курсов системной терапии до момента, когда лучевая нагрузка на брюшную полость действительно даёт выигрыш, а не добавляет хаотичную токсичность. При местно-распространённом раке поджелудочной железы он оценивает, удаётся ли химиотерапией «подсушить» опухоль и сосудистую инвазию настолько, чтобы синхронное облучение стало шансом на стабильный контроль, а не только на краткий эффект. При раке желудка и толстой кишки специалист решает, ограничиться ли паллиативными курсами на отдельные болезненные конгломераты лимфоузлов, или есть смысл в более агрессивном химиолучевом подходе, и именно он прекращает или меняет лекарственную схему, если на фоне облучения нарастают гематологические или печёночные осложнения.
- Абдоминальный хирург оценивает возможности хирургического лечения: где ещё реальна радикальная операция, а где остаётся только комбинация лекарственного и лучевого лечения. При раке желудка и толстой кишки он обозначает зоны потенциально «грязных» краёв резекции, где лучевая терапия способна «добрать» микроскопический остаток, а при раке поджелудочной железы объясняет, насколько плотно опухоль спаяна с чревным стволом и верхней брыжеечной артерией и имеет ли смысл надеяться на конверсию в операбельное состояние. При перитонеальном канцероматозе хирург оценивает возможность циторедуктивного вмешательства с HIPEC и вместе с радиотерапевтом решает, нужны ли локальные паллиативные поля на отдельные болезненные зоны, чтобы не разрушить хрупкий баланс после обширной операции.
- Консультации гастроэнтеролога и гепатолога особенно важны, когда облучение захватывает зону желудка, тонкой кишки, печени или желчных протоков, а системная терапия уже нанесла удар по слизистым и паренхиме. Гастроэнтеролог помогает выстроить схему профилактики лучевого энтерита и колита, подбирает дозы противодиарейных средств, определяет момент, когда диарея становится не ожидаемым побочным эффектом, а угрозой обезвоживания и электролитных сдвигов. Гепатолог оценивает суммарную нагрузку на печень при сочетании облучения с цитостатиками, таргетными препаратами и возможными метастазами, вовремя вводит гепатопротективные режимы и ограничивает дальнейшую агрессию, если риск лучевого гепатита становится слишком высок.
- Диетолог встраивает рацион в конкретный анатомический и функциональный контекст. После гастрэктомии или резекции поджелудочной железы диетолог вместе с онкологом и гастроэнтерологом решает, какой объём питания реально удержится без постоянной рвоты и болей, сколько калорий можно безопасно переложить на специализированные смеси, а когда уже нужен зонд или парентеральная поддержка. На фоне облучения брюшной полости именно он контролирует, чтобы отказ от грубой клетчатки и тяжёлой пищи не превратился в обеднение рациона до сухарей и чая, и подсказывает, как разместить небольшие порции еды в те промежутки между сеансами, когда тошнота минимальна.
- Анестезиолог-реаниматолог и специалист по лечению боли подключаются там, где обычная таблетка анальгетика не в состоянии удержать сложный абдоминальный болевой синдром. При раке поджелудочной железы они оценивают целесообразность блокады чревного сплетения до или на фоне лучевой терапии, подбирают эпидуральные или системные схемы анальгезии, которые позволят пациенту хотя бы лежать на столе во время длительных сеансов. При тяжёлых осложнениях облучения брюшной полости, таких как кровотечение, перфорация, септическое состояние, реаниматолог берёт на себя короткий, но критический этап стабилизации с параллельным вопросом к онкологам: где граница между продолжением агрессивного лечения и переходом к максимально честному паллиативному подходу.
- Психоонколог помогает онкобольному, когда лечение часто сопровождается выраженной слабостью, нарушением питания, асцитом и зависимостью от помощи окружающих. Врач дает возможность проговорить страх потери контроля над телом, стыда из-за стомы или частой диареи, ощущение «бесконечного» лечения с операциями, химиотерапией и облучением, обучает техникам совладания с приступами паники и ночными страхами. Социальный работник решает конкретные вопросы: как организовать дорогу на сеансы для человека, который с трудом ходит из-за асцита, где взять удобное кресло или функциональную кровать, как оформить уход на дому и разгрузить родственников, чтобы пациент не чувствовал себя «обузой» именно в тот момент, когда главное — выжить и выдержать курс до конца.
Какие обследования назначаются
- Клинический осмотр и сбор анамнеза назначаются перед началом лучевой терапии, затем повторяются по ходу курса и в периоде наблюдения. Специалист уточняет характер болей, стула, наличие тошноты, рвоты, метеоризма, оценивает выраженность слабости, снижение массы тела, наличие асцита и периферических отёков. Во время облучения осмотр помогает вовремя заметить нарастание болевого синдрома, обезвоживание, признаки кишечной непроходимости или кровотечения, а после завершения лечения используется для оценки реального эффекта на симптомы и планирования дальнейшей реабилитации.
- Анализы крови назначаются всем пациентам до старта облучения и в динамике, особенно при одновременной химиотерапии. В стандартный набор входит общий анализ крови с оценкой гемоглобина, лейкоцитов и тромбоцитов, а также базовая биохимия для контроля функции печени, почек и электролитного баланса. До курса формируется исходный профиль, по ходу лечения исследования повторяют при усилении слабости, появлении кровоточивости, лихорадки, а после завершения лучевой терапии анализы помогают оценить восстановление кроветворения и метаболического статуса.
- Общий анализ мочи выполняется перед началом облучения и затем по показаниям, особенно при сочетании лучевой и системной терапии. Исследование позволяет судить о работе почек, наличии протеинурии, скрытого воспаления мочевыводящих путей, что критично при использовании нефротоксичных препаратов и при планировании дозовой нагрузки на почки. В процессе лечения анализ мочи повторяют при появлении отёков, изменении суточного диуреза, повышении артериального давления, а в последующем периоде наблюдения используют для оценки отдалённых эффектов комбинированного лечения.
- ЭКГ и при необходимости консультация кардиолога назначаются большинству онкопациентов перед облучением брюшной полости, так как значительная часть схем сочетает лучевую терапию с кардиотоксичными цитостатиками или таргетными препаратами. До курса оценивается ритм, проводимость, наличие ишемических изменений, формируется отправная точка для дальнейшего сравнения. При появлении одышки, болей в грудной клетке, сердцебиений во время лечения ЭКГ повторяют, а после завершения программы кардиологическое наблюдение позволяет вовремя уловить нарушения, влияющие на переносимость дальнейшей противоопухолевой терапии.
- Ультразвуковое исследование органов брюшной полости назначается до планирования лучевой терапии при раке желудка, поджелудочной железы, печени, толстой кишки и при перитонеальном канцероматозе. По данным УЗИ оценивают размеры печени, наличие метастатических очагов, объём асцита, состояние желчных протоков, селезёнки, крупных сосудов, что помогает ориентироваться в распространённости процесса и симптомных причинах болей или желтухи. В период лечения исследование повторяют при нарастании асцита, появлении новых болей в правом подреберье, изменении биохимических показателей, а после облучения используют для простой динамической оценки без лишней лучевой нагрузки.
- Компьютерная томография органов брюшной полости с контрастированием назначается, как основной метод детальной визуализации до планирования лучевой терапии при раке желудка, поджелудочной железы, толстой кишки, печени и забрюшинных лимфоузлах. МСКТ позволяет оценить размеры и контуры опухоли, степень вовлечения прилежащих органов, сосудистых структур, лимфатических коллекторов, выявить дополнительные очаги, влияющие на объём поля. По результатам исследования выполняется КТ-симуляция в лечебном положении, а при выраженной динамике по клинике или анализам по ходу курса может назначаться повторное сканирование для адаптации плана.
- Магнитно-резонансная томография брюшной полости и МРТ малого таза с контрастом проводится при раке поджелудочной железы, первичном раке печени, раке прямой кишки и при спорных находках по КТ. МРТ даёт более точное представление о связи опухоли с сосудами, желчными протоками, жировой клетчаткой, фасциями, тазовой диафрагмой, что помогает ограничить объём облучаемого блока и сохранить максимальное количество функционирующей паренхимы. В период наблюдения МРТ используется для уточнения характера остаточных масс в зоне облучения, когда по КТ трудно отличить фиброз и спаечный конгломерат от сохраняющейся опухолевой ткани.
- ПЭТ-КТ с онкологическим радиофармпрепаратом назначается при онкологии с подозрением на множественные метастазы, при неясной картине по стандартной КТ или при планировании стереотаксического облучения отдельных очагов в печени, надпочечниках, забрюшинных лимфоузлах. До начала лучевой терапии исследование помогает выявить метаболически активные участки в пределах брюшной полости и за её пределами, скорректировать стадирование и объём локального воздействия. После завершения курса ПЭТ-КТ используют для оценки метаболического ответа и раннего выявления рецидива, особенно если по анатомическим методам визуализации сохраняются сомнительные изменения.
- КТ-симуляция брюшной полости для планирования лучевой терапии выполняется непосредственно перед началом курса и служит основой всех расчётов. Исследование проводится в фиксированном положении, часто с использованием иммобилизационных матрасов и контролем наполнения желудка, кишечника, мочевого пузыря, при необходимости в режиме четырёхмерной КТ для учёта дыхательных смещений верхних отделов. На полученных срезах контурируется опухолевый объём, ложа резекции, зоны лимфооттока и критические структуры, а в дальнейшем симуляция может повторяться при заметном изменении веса, выраженном уменьшении опухолевого массива или появлении значимого асцита.
- Эндоскопические исследования – эзофагогастродуоденоскопия и колоноскопия – назначаются до начала облучения брюшной полости при раке желудка, двенадцатиперстной кишки, толстой кишки, преимущественно для уточнения местных условий и подготовки к лечению. Перед курсом эндоскопист оценивает состояние слизистой, диаметр просвета, наличие язв, кровоточивости, определяет участки, где лучевая нагрузка может усиливать риск перфорации или кровотечения. В период наблюдения после облучения те же методы используются при появлении кровянистого стула, выраженной анемии, стойких болей в проекции облученного сегмента, чтобы различить лучевой колит или гастрит и рецидив опухоли.
Что важно знать пациентам
Как подготовиться к курсу радиотерапии?
Перед началом радиолечения выполняется комплекс обследований крови, ультразвуковых и рентгенологических методов, при необходимости эндоскопия, оцениваются функции печени, почек, сердечно-сосудистой системы. На этапе КТ-симуляции подбирают удобное и воспроизводимое положение тела, наносят разметку на кожу, обсуждают режим питания и наполнения кишечника и мочевого пузыря перед сеансами. Пациенту важно заранее уточнить список текущих препаратов, согласовать приём антикоагулянтов, не экспериментировать с диетами без согласования и прийти на первую разметку с запасом времени, без спешки и тяжёлого приёма пищи непосредственно перед процедурой.
Какие побочные эффекты?
На фоне облучения у онкобольному нередко появляются тошнота, снижение аппетита, более мягкий или учащённый стул, усиление метеоризма, утомляемость, иногда умеренные боли в животе. Неблагоприятными признаками считают многократную рвоту, невозможность удерживать жидкость, кровь в стуле или чёрный дегтеобразный стул, нарастающую схваткообразную боль, полное отсутствие стула и газов, высокую температуру. При появлении подобных симптомов важно не ждать очередного планового визита, а сразу сообщить в отделение лучевой терапии или дежурной службе, чтобы исключить кровотечение, тяжёлый энтероколит, непроходимость или инфекционные осложнения.
Режим питания и активности во время облучения
Полный отказ от еды не нужен, но рацион обычно корректируют: уменьшают объём порций, убирают грубую клетчатку, избыток жирной, сильно острой пищи, газированные напитки, подбирают продукты, которые переносятся без усиления боли и вздутия. Частые небольшие приёмы пищи и достаточное количество жидкости помогают легче переносить тошноту и диарею, при стойкой потере веса диетолог может предложить питательные смеси. Двигательная активность приветствуется в мягком варианте: короткие прогулки, простые движения по квартире, избегание подъёма тяжестей и длительного напряжения мышц брюшной стенки, особенно при выраженном болевом синдроме или асците.
Что делать после завершения курса радиотерапии?
После окончания лучевой терапии составляется план контроля: визиты к онкологу, периодические анализы крови, УЗИ или КТ брюшной полости, при необходимости эндоскопия, оценка массы тела и выраженности симптомов. На приёмах уточняются характер болей, стул, аппетит, наличие асцита, желтушности кожи и склер, выраженность слабости, по результатам корректируется питание, лекарственная поддержка, решается вопрос о дальнейшей системной терапии. Поводом для внепланового обращения служат усиливающиеся боли, новая рвота, задержка стула и газов, быстро растущий живот за счёт скопления жидкости, выраженная желтуха, стойкая лихорадка или резкое падение веса — откладывать оценку подобных изменений небезопасно.