- ДИАГНОСТИКА
- МРТ
- КТ
- КТ ГОЛОВЫ
- КТ ШЕИ
- КТ ГРУДНОЙ КЛЕТКИ
- КТ БРЮШНОЙ ПОЛОСТИ
- КТ МАЛОГО ТАЗА
- КТ ПОЗВОНОЧНИКА
- КТ СУСТАВОВ
- КТ КОСТЕЙ
- КТ АНГИОГРАФИЯ
- КТ ЗУБОВ
- УЗИ
- УЗИ ОРГАНОВ МАЛОГО ТАЗА
- УЗИ БРЮШНОЙ ПОЛОСТИ
- УЗИ ЗАБРЮШИННОГО ПРОСТРАНСТВА
- УЗИ СЕРДЦА
- УЗИ СОСУДОВ
- УЗИ МЯГКИХ ТКАНЕЙ, НЕРВОВ И ЖЕЛЕЗ
- УЗИ СУСТАВОВ
- УЗИ ГОЛОВЫ
- УЗИ ЛИМФОУЗЛОВ
- УЗИ ПРИ БЕРЕМЕННОСТИ
- УЗИ ПЛОДА
- УЗИ НОВРОЖДЕННОМУ РЕБЕНКУ
- УЗИ ПОСЛЕ АБОРТА
- РЕНТГЕН
- ВРАЧИ
- КАКОЙ ВРАЧ ЛЕЧИТ
- АКУШЕР-ГИНЕКОЛОГ
- АЛЛЕРГОЛОГ
- ВЕРТЕБРОЛОГ
- ВЕСТИБУЛОЛОГ
- ГАСТРОЭНТЕРОЛОГ
- ГЕМАТОЛОГ
- ГИНЕКОЛОГ
- ДЕРМАТОЛОГ
- ДИЕТОЛОГ
- ИГЛОТЕРАПЕВТ
- ИММУНОЛОГ
- ИНФЕКЦИОНИСТ
- КАРДИОЛОГ
- ВРАЧ ЛЕЧЕБНОЙ ФИЗКУЛЬТУРЫ
- МАММОЛОГ
- НЕВРОЛОГ
- НЕЙРОХИРУРГ
- НЕОНАТОЛОГ
- НЕФРОЛОГ
- ОНКОЛОГ
- ОНКОЛОГ-МАММОЛОГ
- ОРТОПЕД
- ОРТОПЕД-ХИРУРГ
- ОТОЛАРИНГОЛОГ
- ОФТАЛЬМОЛОГ
- ОСТЕОПАТ
- ПЕДИАТР
- ПРОКТОЛОГ
- ПСИХИАТР
- ПСИХОТЕРАПЕВТ
- ПУЛЬМОНОЛОГ
- РЕВМАТОЛОГ
- РЕФЛЕКСОТЕРАПЕВТ
- СЕКСОЛОГ
- СОМНОЛОГ
- СОСУДИСТЫЙ ХИРУРГ
- СПОРТИВНЫЙ ВРАЧ
- ТЕРАПЕВТ
- ТРАВМАТОЛОГ
- ТРИХОЛОГ
- УРОЛОГ
- ФИЗИОТЕРАПЕВТ
- ФЛЕБОЛОГ
- ФТИЗИАТР
- ВРАЧ ФУНКЦИОНАЛЬНОЙ ДИАГНОСТИКИ
- ХИРУРГ
- ЭНДОКРИНОЛОГ
- ЭНДОСКОПИСТ
- ЭПИЛЕПТОЛОГ
- СПОРТИВНЫЙ МАССАЖИСТ
- ГЕПАТОЛОГ
- ПАРАЗИТОЛОГ
- МАНУАЛЬНЫЙ ТЕРАПЕВТ
- СЕМЕЙНЫЙ ПСИХОЛОГ
- ВРАЧ ОБЩЕЙ ПРАКТИКИ
- ПРОФПАТОЛОГ-ТЕРАПЕВТ
- АНДРОЛОГ
- АНГИОЛОГ
- АРИТМОЛОГ
- АРТРОЛОГ
- БРОНХОЛОГ
- ВЕНЕРОЛОГ
- ГЕМОСТАЗИОЛОГ
- ГИРУДОТЕРАПЕВТ
- ДИАБЕТОЛОГ
- КИНЕЗИОЛОГ
- РАДИОТЕРАПЕВТ
- РЕПРОДУКТОЛОГ
- СУРДОЛОГ
- ФОНИАТР
- ХИМИОТЕРАПЕВТ
- СКИДКИ
- НА КАРТЕ
- МРТ РЯДОМ (поиск по району)
- АДМИРАЛТЕЙСКИЙ РАЙОН
- ВАСИЛЕОСТРОВСКИЙ РАЙОН
- ВЫБОРГСКИЙ РАЙОН
- КАЛИНИНСКИЙ РАЙОН
- КИРОВСКИЙ РАЙОН
- КОЛПИНСКИЙ РАЙОН
- КРАСНОГВАРДЕЙСКИЙ РАЙОН
- КРАСНОСЕЛЬСКИЙ РАЙОН
- КРОНШТАДТСКИЙ РАЙОН
- КУРОРТНЫЙ РАЙОН
- МОСКОВСКИЙ РАЙОН
- НЕВСКИЙ РАЙОН
- ПЕТРОГРАДСКИЙ РАЙОН
- ПЕТРОДВОРЦОВЫЙ РАЙОН
- ПРИМОРСКИЙ РАЙОН
- ПУШКИНСКИЙ РАЙОН
- ФРУНЗЕНСКИЙ РАЙОН
- ЦЕНТРАЛЬНЫЙ РАЙОН
- ЛЕН. ОБЛАСТЬ
- КТ и МСКТ РЯДОМ (поиск по району)
- АДМИРАЛТЕЙСКИЙ РАЙОН
- ВАСИЛЕОСТРОВСКИЙ РАЙОН
- ВЫБОРГСКИЙ РАЙОН
- КАЛИНИНСКИЙ РАЙОН
- КИРОВСКИЙ РАЙОН
- КОЛПИНСКИЙ РАЙОН
- КРАСНОГВАРДЕЙСКИЙ РАЙОН
- КРАСНОСЕЛЬСКИЙ РАЙОН
- КРОНШТАДТСКИЙ РАЙОН
- КУРОРТНЫЙ РАЙОН
- МОСКОВСКИЙ РАЙОН
- НЕВСКИЙ РАЙОН
- ПЕТРОГРАДСКИЙ РАЙОН
- ПЕТРОДВОРЦОВЫЙ РАЙОН
- ПРИМОРСКИЙ РАЙОН
- ПУШКИНСКИЙ РАЙОН
- ФРУНЗЕНСКИЙ РАЙОН
- ЦЕНТРАЛЬНЫЙ РАЙОН
- ЛЕН. ОБЛАСТЬ
- МРТ АДРЕСА БОЛЬНИЦ В СПБ
- МРТ РЯДОМ (поиск по району)
Адреса и стоимость брахитерапии в СПБ
Цена указана с учетом льгот и акции
Услуга лечения онкологии
Услуга лечебного сопровождения для пациентов с онкологией — это индивидуальная комплексная помощь, которая может включать:
 Лучшиие онкологидоступ к ведущим специалистам Санкт-Петербурга, которые подберут современные схемы терапии и проконтролируют эффективность лечения на каждом этапе.
Лучшиие онкологидоступ к ведущим специалистам Санкт-Петербурга, которые подберут современные схемы терапии и проконтролируют эффективность лечения на каждом этапе. Госпитализация или дневной стационарвозможность пройти лечение в комфортных условиях ведущих онкологических центров Санкт-Петербурга.
Госпитализация или дневной стационарвозможность пройти лечение в комфортных условиях ведущих онкологических центров Санкт-Петербурга. Персональный протокол леченияразработка индивидуальной стратегии терапии с учётом типа опухоли, стадии заболевания, генетических особенностей, сопутствующих состояний и истории предыдущего лечения.
Персональный протокол леченияразработка индивидуальной стратегии терапии с учётом типа опухоли, стадии заболевания, генетических особенностей, сопутствующих состояний и истории предыдущего лечения. Второе независимое мнениеэкспертная оценка диагноза и лечебной тактики от ведущих онкологов, позволяющая подтвердить правильность выбранной стратегии, получить дополнительные варианты терапии, избежать ошибок и повысить шансы на успешный результат благодаря объективному профессиональному взгляду стороннего специалиста.
Второе независимое мнениеэкспертная оценка диагноза и лечебной тактики от ведущих онкологов, позволяющая подтвердить правильность выбранной стратегии, получить дополнительные варианты терапии, избежать ошибок и повысить шансы на успешный результат благодаря объективному профессиональному взгляду стороннего специалиста.
Лучшие специалисты в Санкт-Петербурге с рейтингом 4.5+
Последние отзывы
Что такое брахитерапия?
Брахитерапия – это вид лучевого лечения, при котором источник излучения подводят максимально близко к опухоли или вводят внутрь неё с помощью специальных аппликаторов или игл, за счёт чего высокая доза концентрируется в зоне опухоли, а окружающие ткани получают относительно меньшую нагрузку. Онкопациенту важно понимать, что это плановое, тщательно рассчитанное лечение, которое проводится поэтапно, под контролем визуализирующих методов и с учётом суммарной дозы, уже полученной при дистанционной радиотерапии.
Виды брахитерапии
Внутриполостная брахитерапия при раке шейки и тела матки включают размещение аппликаторов в полости матки и сводах влагалища с последующим подключением высокодозного источника, расчёт фракционной и суммарной дозы с учётом уже проведённой дистанционной лучевой терапии, поэтапное проведение нескольких сеансов с фиксированным интервалом, контролем положения аппликаторов перед каждой фракцией и обязательным ограничением дозы на прямую кишку, мочевой пузырь и сигмовидную кишку, что позволяет сформировать высокую дозу в опухолевом объёме при щадящем воздействии на окружающие органы.
Протоколы интерстициальной брахитерапии применяются при опухолях предстательной железы, мягких тканей, головы и шеи и включают введение игл или катетеров непосредственно в опухолевый очаг или ложе опухоли под визуальным контролем, подключение источников высокодозной или низкодозной мощности по расчётной схеме, фракционирование экспозиции с учётом неоднородности тканей и близости критических структур, а также контроль распределения дозы по данным планирующей системы, что обеспечивает формирование дозового «контура», повторяющего форму мишени и минимизирующего нагрузку на соседние органы.
Низкодозная брахитерапия с постоянной имплантацией применяется преимущественно при раке предстательной железы и предусматривает размещение радиоактивных зерен в паренхиме органа по заранее рассчитанной сетке, с учётом размеров и конфигурации железы, характеристик опухоли и анатомии мочеиспускательного канала и прямой кишки, контроль распределения имплантов по данным послеоперационной визуализации и оценку фактически полученной дозы в мишени и органах риска, что позволяет реализовать длительное локальное облучение с плавным спадом активности без повторных процедур.
Высокодозная фракционированная брахитерапия предусматривает кратковременное введение высокоактивного источника в аппликаторы или катетеры с последующим автоматическим извлечением после достижения расчётной дозы, проведение нескольких коротких сеансов в амбулаторном или стационарном режиме, точную фиксацию положения аппликаторов на время процедуры и постоянный контроль дозового вклада в органы риска, что даёт возможность сочетать выраженный локальный эффект с удобным для онкобольного режимом лечения и минимальной радиационной нагрузкой на персонал.
Протоколы поверхностной и аппликационной брахитерапии используются при опухолях кожи и слизистых оболочек и включают наложение специальных аппликаторов или индивидуальных масок с подведением источника на строго заданное расстояние от поверхности, расчёт дозы с учётом толщины поражённого слоя и подлежащих структур, выполнение серий коротких сеансов с непрерывным контролем положения аппликатора, что позволяет ограничить высокую дозу поверхностным слоям и снизить риск глубокого тканевого повреждения.
Комбинированная брахитерапия с дистанционной лучевой терапией применяется при местнораспространённых опухолях и предусматривают проведение основного объёма дозы дистанционно с последующим локальным «бустом» с помощью брахитерапии, согласование суммарной дозы и распределения по мишени и органам риска между двумя методами, временное разделение этапов лечения и оценку суммарного биологического эквивалента, что позволяет усилить дозу в критической зоне опухолевого роста без неприемлемого увеличения нагрузки на окружающие ткани.
Протоколы паллиативной брахитерапии используются при неоперабельных или далеко зашедших процессах и включают укороченные схемы с меньшим числом фракций и прицельным подведением дозы к симптомным очагам, таким как кровоточащие, болевые или обтурирующие опухоли, с акцентом на быстрое уменьшение локальных проявлений при допустимом риске поздних осложнений, что позволяет улучшать качество жизни и контролировать наиболее тяжёлые местные симптомы у онкопациентов с ограниченным прогнозом.
Помощь онкопациентам
Сопутствующая дистанционная лучевая терапия проводится для формирования суммарной очаговой дозы, распределённой между объёмом первичной опухоли и регионарными зонами, включает курс наружного облучения до или между сеансами подведения внутренних источников, позволяет обработать лимфоколлекторы и зоны возможного микроскопического распространения, уменьшить объём опухолевой массы перед локальным «бустом» и снизить риск рецидива за пределами области непосредственного подведения источника.
Системная лекарственная терапия проводится пациентам с высоким риском микрометастатического процесса и включает химиотерапию, таргетные или гормональные препараты в зависимости от типа опухоли, применяется в виде курсов до, между или после этапов локального облучения, направлена на контроль системного компонента заболевания, уменьшение вероятности отдалённых метастазов и усиление общего противоопухолевого эффекта при сочетании локального и системного воздействия.
Обезболивание проводится для контроля боли, возникающей при установке аппликаторов, интерстициальных имплантациях и в ранний постпроцедурный период, включает применение анальгетиков ступенчато от нестероидных до опиоидных по показаниям, при необходимости локальные анестезирующие методы, а также препараты, уменьшающие отёк и воспалительную реакцию в зоне облучения, что позволяет проводить повторные процедуры без выраженного болевого синдрома и поддерживать удовлетворительное качество жизни.
Противоинфекционное лечение осуществляется при риске инфицирования по ходу введённых катетеров или в зонах слизистых, подвергшихся травматизации, включает профилактическое или лечебное назначение антибактериальных препаратов по показаниям, местную антисептическую обработку, наблюдение за температурой и анализами крови, особенно при интерстициальных вмешательствах в малом тазу или области головы и шеи, что снижает вероятность формирования локальных гнойно-воспалительных осложнений и необходимости прерывания курса.
Противоотёчная и органосохраняющая терапия назначается для уменьшения отёка тканей, прилежащих к зоне облучения, и профилактики функциональных нарушений, включает назначение диуретиков по показаниям, препаратов, улучшающих микроциркуляцию, местные средства для защиты слизистых оболочек полости рта, влагалища, мочевого пузыря или прямой кишки, рекомендации по режиму нагрузки и уходу за облучённой областью, что помогает снизить выраженность дизурии, проктита, мукозитов и других функциональных расстройств.
Нутритивная и метаболическая поддержка проводится онкобольным с исходным истощением или снижением аппетита на фоне сочетанного лечения, включает коррекцию рациона с повышенным содержанием белка и энергии, использование специализированных смесей, при необходимости энтеральную или частичную парентеральную поддержку, контроль массы тела и лабораторных показателей, что позволяет поддерживать восстановительные процессы в облучённых тканях и переносимость как самих сеансов брахитерапии, так и параллельной системной терапии.
Реабилитационная поддержка осуществляется в зависимости от локализации очага и характера вмешательства, включает упражнения для сохранения подвижности тазовых структур и мышц промежности, рекомендации по тренировке мочевого пузыря и кишечника, мероприятия по профилактике стриктур и фиброзных изменений, а при локализации в области головы и шеи — логопедическую и глотательную реабилитацию, что позволяет уменьшить долгосрочные функциональные последствия брахитерапии и сохранить максимально возможный уровень повседневной активности.
Какие врачи могут быть вовлечены
- Радиотерапевт-онколог отвечает за планирование и проведение брахитерапии, выбирает тип внутриполостного или интерстициального облучения, определяет объём мишени и допустимые дозы на органы риска, контролирует каждую фракцию по данным планирующей системы, оценивает переносимость лечения и принимает решения о продолжении, изменении или завершении курса.
- Онкогинеколог участвует в брахитерапии при раке шейки и тела матки, оценивает стадию и анатомические особенности малого таза, выполняет установку внутриполостных аппликаторов, контролирует их положение по данным визуализации, сочетает брахитерапию с хирургическим этапом и системным лечением и отвечает за ведение пациентки с учётом гинекологических последствий облучения.
- Онкоуролог вовлекается при брахитерапии рака предстательной железы, оценивает объём и конфигурацию железы, выраженность симптомов со стороны мочевыводящих путей, участвует в выборе между интерстициальной высокодозной или постоянной низкодозной имплантацией, контролирует мочеиспускание и риск стриктур уретры после лечения и определяет необходимость дополнительного хирургического или медикаментозного вмешательства.
- Хирург-онколог участвует при интерстициальной брахитерапии мягких тканей, головы и шеи, желудочно-кишечного тракта, выполняет доступ и размещение катетеров или игл в ложе опухоли или в сам очаг, ориентируясь на анатомические структуры, обеспечивает адекватную фиксацию имплантов на время курса и совместно с радиотерапевтом-онкологом оценивает локальный контроль и возможность последующих реконструктивных вмешательств.
- Анестезиолог-реаниматолог обеспечивает обезболивание и безопасность при установке аппликаторов и интерстициальных имплантов, выбирает вид анестезии или седации в зависимости от локализации и объёма вмешательства, контролирует дыхание, гемодинамику и реакцию на позиционирование пациента, ведёт больного в раннем послеоперационном периоде при выраженном болевом синдроме и сопутствующей соматической патологии.
- Онколог-химиотерапевт ведёт больных, которым брахитерапия проводится в составе комбинированного лечения, подбирает схемы лекарственной терапии до или после локального облучения, оценивает общую противоопухолевую динамику, координирует сроки курсов с радиотерапевтом, учитывая кроветворение и переносимость, и решает вопрос о продолжении системного лечения при развитии лучевых и общих осложнений.
- Паллиативный врач участвует в принятии решения о брахитерапии при распространённых и неоперабельных процессах, оценивает ожидаемое влияние локального облучения на боль, кровотечение, обструкцию органа и качество жизни, подбирает параллельную симптоматическую терапию, контролирует баланс пользы и риска для ослабленного пациента и помогает выстраивать дальнейшую тактику наблюдения после завершения курса.
Какие обследования назначаются
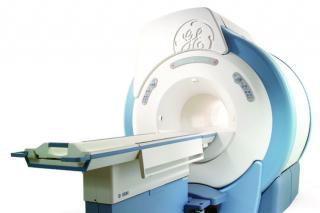
- Компьютерная томография области предполагаемого облучения назначается для точного определения размеров и локализации опухолевого узла, оценки отношения опухоли к костным структурам, мочевому пузырю, прямой кишке, кишке и другим органам риска, используется как основа для планирующей системы брахитерапии, где по КТ-данным строятся объём мишени и дозовое распределение, а также контролируется правильность расположения аппликаторов или интерстициальных катетеров перед началом фракций.
- Магнитно-резонансная томография с контрастированием назначается при анатомически сложной локализации, позволяет более чётко, чем КТ, визуализировать мягкотканные структуры, границы опухоли, инфильтрацию параметрия, стенки органов и нервно-сосудистые пучки, её данные нередко совмещаются с КТ при планировании, что даёт возможность точнее очертить клинический и планируемый объёмы мишени и снизить нагрузку на критические органы при расчёте дозы брахитерапии.
- Ультразвуковое исследование используется при брахитерапии органов малого таза и предстательной железы для оценки размеров и конфигурации органа, выявления сопутствующих кист, узлов, объёма остаточной мочи, определяется взаиморасположение простаты, шейки матки, мочевого пузыря и прямой кишки, УЗИ применяют и интраоперационно при интерстициальной имплантации зерён или игл для уточнения глубины и направления их введения, что снижает риск перфорации и неправильного позиционирования источников.
- Рентгенологический и КТ-контроль введение аппликаторов или катетеров проводится непосредственно перед расчётом и проведением фракций брахитерапии, выполняются снимки в двух проекциях или короткая КТ-серия с установленными аппликаторами, оценивается глубина введения, симметричность расположения, расстояние до стенки органов риска, при необходимости аппликаторы или иглы корректируют, после чего данные фиксируются в планирующей системе, что обеспечивает соответствие реального расположения источника рассчитанному дозовому полю.
- Гинекологическое, урологическое или проктологическое обследование осуществляется для оценки местного статуса перед брахитерапией, уточнения протяжённости и стадии опухоли, состояния слизистых, наличия язв, стриктур или кровоточивости, сопоставляется клиническая картина с данными визуализации, определяется техническая возможность введения внутриполостных аппликаторов или интерстициальных игл и выбирается оптимальный тип вмешательства.
- Эндоскопические обследования, такие как цистоскопия, ректороманоскопия или колоноскопия, назначаются по показаниям при близком расположении опухоли или зоны облучения к мочевому пузырю и кишечнику, позволяют визуально оценить состояние слизистой, наличие инфильтрации, язв, свищей, включить эти данные в расчёт допустимой дозы на органы риска и своевременно выявить изменения, которые могут повлиять на выбор схемы брахитерапии или необходимость её ограничения.
- Общий анализ крови и биохимический анализ крови назначаются перед началом и в процессе брахитерапии, позволяют оценить уровень гемоглобина, лейкоцитов, тромбоцитов, показатели функции печени и почек, электролитный состав, белковый и воспалительный профиль, на основании этих данных решается вопрос о безопасности повторных анестезиологических пособий, возможности сочетания брахитерапии с системной терапией и необходимости коррекции сопутствующего лечения.
- Коагулограмма выполняется для оценки свёртывающей системы перед установкой аппликаторов или интерстициальных игл, особенно при планировании многократных вмешательств в условиях анемии и возможного контакта с сосудистыми структурами, по результатам исследования корректируются антикоагулянты и антиагреганты, при необходимости проводится их временная отмена или замена, что уменьшает риск кровотечения во время манипуляций и в раннем послеоперационном периоде.
- Электрокардиография и, при показаниях, эхокардиография назначаются онкологическим пациентам с сердечно-сосудистой патологией или подозрением на неё, позволяют оценить ритм, признаки ишемии, сократительную способность миокарда и наличие сердечной недостаточности, на основании этих данных анестезиолог выбирает вид анестезии или седации, допустимый объём инфузии и режим наблюдения во время процедур брахитерапии, что снижает риск кардиальных осложнений.
Что важно знать пациентам
Почему брахитерапию назначают не всем онкопациентам?
Решение о проведении брахитерапии зависит от размеров и расположения опухоли, её отношения к соседним органам, общей распространённости процесса и состояния пациента, поэтому даже при одинаковом диагнозе не у всех есть техническая возможность безопасно установить аппликаторы или интерстициальные иглы. Врач учитывает анатомию, риск осложнений, уже проведённое лечение и прогноз, и если ожидаемая польза от локального усиления дозы превышает потенциальные риски, брахитерапия включается в план, а при неблагоприятных условиях могут быть предложены только дистанционное облучение или другие методы.
Что я буду чувствовать вво время брахитерапии?
После внутриполостных или интерстициальных процедур возможны тянущие или ноющие боли в зоне вмешательства, чувство давления или инородного тела, умеренные кровянистые выделения со слизистых, учащённое мочеиспускание, дискомфорт при дефекации или половом контакте в ближайшее время после лечения. Обычно эти симптомы постепенно уменьшаются по мере заживления тканей, при необходимости назначаются обезболивающие, противовоспалительные и местные защитные средства, а пациент получает подробные рекомендации по гигиене, нагрузкам и временным ограничениям.
Какие осложнения?
Срочного обращения требуют усиливающаяся боль, которая не снимается обычными назначенными обезболивающими, высокая температура с ознобом, выраженные кровянистые или гнойные выделения, резкая боль при мочеиспускании или невозможность помочиться, частый жидкий стул с кровью, внезапная сильная боль в малом тазу или промежности. Такие симптомы могут говорить о кровотечении, инфекционном осложнении, выраженном отёке или повреждении соседних структур, поэтому важно не пытаться «перетерпеть», а как можно скорее связаться с лечащим учреждением или обратиться за неотложной помощью.
Что делать после курса брахитерапии?
После брахитерапии изменения в облучённых тканях развиваются постепенно, часть поздних лучевых реакций и функциональных нарушений может проявиться через месяцы, поэтому пациенту необходимо регулярно приходить на контрольные осмотры, выполнять назначенные исследования и сообщать о новых симптомах. Соблюдение рекомендаций по режиму, уходу за слизистыми и кожей, питанию, сексуальной и физической активности помогает снизить риск поздних осложнений, а плановые визиты позволяют врачу оценивать устойчивость локального эффекта, вовремя выявлять возможный рецидив и при необходимости дополнять лечение или усиливать реабилитацию.











