- ДИАГНОСТИКА
- МРТ
- КТ
- КТ ГОЛОВЫ
- КТ ШЕИ
- КТ ГРУДНОЙ КЛЕТКИ
- КТ БРЮШНОЙ ПОЛОСТИ
- КТ МАЛОГО ТАЗА
- КТ ПОЗВОНОЧНИКА
- КТ СУСТАВОВ
- КТ КОСТЕЙ
- КТ АНГИОГРАФИЯ
- КТ ЗУБОВ
- УЗИ
- УЗИ ОРГАНОВ МАЛОГО ТАЗА
- УЗИ БРЮШНОЙ ПОЛОСТИ
- УЗИ ЗАБРЮШИННОГО ПРОСТРАНСТВА
- УЗИ СЕРДЦА
- УЗИ СОСУДОВ
- УЗИ МЯГКИХ ТКАНЕЙ, НЕРВОВ И ЖЕЛЕЗ
- УЗИ СУСТАВОВ
- УЗИ ГОЛОВЫ
- УЗИ ЛИМФОУЗЛОВ
- УЗИ ПРИ БЕРЕМЕННОСТИ
- УЗИ ПЛОДА
- УЗИ НОВРОЖДЕННОМУ РЕБЕНКУ
- УЗИ ПОСЛЕ АБОРТА
- РЕНТГЕН
- ВРАЧИ
- КАКОЙ ВРАЧ ЛЕЧИТ
- АКУШЕР-ГИНЕКОЛОГ
- АЛЛЕРГОЛОГ
- ВЕРТЕБРОЛОГ
- ВЕСТИБУЛОЛОГ
- ГАСТРОЭНТЕРОЛОГ
- ГЕМАТОЛОГ
- ГИНЕКОЛОГ
- ДЕРМАТОЛОГ
- ДИЕТОЛОГ
- ИГЛОТЕРАПЕВТ
- ИММУНОЛОГ
- ИНФЕКЦИОНИСТ
- КАРДИОЛОГ
- ВРАЧ ЛЕЧЕБНОЙ ФИЗКУЛЬТУРЫ
- МАММОЛОГ
- НЕВРОЛОГ
- НЕЙРОХИРУРГ
- НЕОНАТОЛОГ
- НЕФРОЛОГ
- ОНКОЛОГ
- ОНКОЛОГ-МАММОЛОГ
- ОРТОПЕД
- ОРТОПЕД-ХИРУРГ
- ОТОЛАРИНГОЛОГ
- ОФТАЛЬМОЛОГ
- ОСТЕОПАТ
- ПЕДИАТР
- ПРОКТОЛОГ
- ПСИХИАТР
- ПСИХОТЕРАПЕВТ
- ПУЛЬМОНОЛОГ
- РЕВМАТОЛОГ
- РЕФЛЕКСОТЕРАПЕВТ
- СЕКСОЛОГ
- СОМНОЛОГ
- СОСУДИСТЫЙ ХИРУРГ
- СПОРТИВНЫЙ ВРАЧ
- ТЕРАПЕВТ
- ТРАВМАТОЛОГ
- ТРИХОЛОГ
- УРОЛОГ
- ФИЗИОТЕРАПЕВТ
- ФЛЕБОЛОГ
- ФТИЗИАТР
- ВРАЧ ФУНКЦИОНАЛЬНОЙ ДИАГНОСТИКИ
- ХИРУРГ
- ЭНДОКРИНОЛОГ
- ЭНДОСКОПИСТ
- ЭПИЛЕПТОЛОГ
- СПОРТИВНЫЙ МАССАЖИСТ
- ГЕПАТОЛОГ
- ПАРАЗИТОЛОГ
- МАНУАЛЬНЫЙ ТЕРАПЕВТ
- СЕМЕЙНЫЙ ПСИХОЛОГ
- ВРАЧ ОБЩЕЙ ПРАКТИКИ
- ПРОФПАТОЛОГ-ТЕРАПЕВТ
- АНДРОЛОГ
- АНГИОЛОГ
- АРИТМОЛОГ
- АРТРОЛОГ
- БРОНХОЛОГ
- ВЕНЕРОЛОГ
- ГЕМОСТАЗИОЛОГ
- ГИРУДОТЕРАПЕВТ
- ДИАБЕТОЛОГ
- КИНЕЗИОЛОГ
- РАДИОТЕРАПЕВТ
- РЕПРОДУКТОЛОГ
- СУРДОЛОГ
- ФОНИАТР
- ХИМИОТЕРАПЕВТ
- СКИДКИ
- НА КАРТЕ
- МРТ РЯДОМ (поиск по району)
- АДМИРАЛТЕЙСКИЙ РАЙОН
- ВАСИЛЕОСТРОВСКИЙ РАЙОН
- ВЫБОРГСКИЙ РАЙОН
- КАЛИНИНСКИЙ РАЙОН
- КИРОВСКИЙ РАЙОН
- КОЛПИНСКИЙ РАЙОН
- КРАСНОГВАРДЕЙСКИЙ РАЙОН
- КРАСНОСЕЛЬСКИЙ РАЙОН
- КРОНШТАДТСКИЙ РАЙОН
- КУРОРТНЫЙ РАЙОН
- МОСКОВСКИЙ РАЙОН
- НЕВСКИЙ РАЙОН
- ПЕТРОГРАДСКИЙ РАЙОН
- ПЕТРОДВОРЦОВЫЙ РАЙОН
- ПРИМОРСКИЙ РАЙОН
- ПУШКИНСКИЙ РАЙОН
- ФРУНЗЕНСКИЙ РАЙОН
- ЦЕНТРАЛЬНЫЙ РАЙОН
- ЛЕН. ОБЛАСТЬ
- КТ и МСКТ РЯДОМ (поиск по району)
- АДМИРАЛТЕЙСКИЙ РАЙОН
- ВАСИЛЕОСТРОВСКИЙ РАЙОН
- ВЫБОРГСКИЙ РАЙОН
- КАЛИНИНСКИЙ РАЙОН
- КИРОВСКИЙ РАЙОН
- КОЛПИНСКИЙ РАЙОН
- КРАСНОГВАРДЕЙСКИЙ РАЙОН
- КРАСНОСЕЛЬСКИЙ РАЙОН
- КРОНШТАДТСКИЙ РАЙОН
- КУРОРТНЫЙ РАЙОН
- МОСКОВСКИЙ РАЙОН
- НЕВСКИЙ РАЙОН
- ПЕТРОГРАДСКИЙ РАЙОН
- ПЕТРОДВОРЦОВЫЙ РАЙОН
- ПРИМОРСКИЙ РАЙОН
- ПУШКИНСКИЙ РАЙОН
- ФРУНЗЕНСКИЙ РАЙОН
- ЦЕНТРАЛЬНЫЙ РАЙОН
- ЛЕН. ОБЛАСТЬ
- МРТ АДРЕСА БОЛЬНИЦ В СПБ
- МРТ РЯДОМ (поиск по району)
Адреса онкоцентров для лечения рака костного мозга в СПБ
Цена указана с учетом льгот и акции
Цена указана с учетом льгот и акции
Цена указана с учетом льгот и акции
Цена указана с учетом льгот и акции
Цена указана с учетом льгот и акции
Цена указана с учетом льгот и акции
Цена указана с учетом льгот и акции
Цена указана с учетом льгот и акции
Цена указана с учетом льгот и акции
Цена указана с учетом льгот и акции
Цена указана с учетом льгот и акции
Цена указана с учетом льгот и акции

Цена указана с учетом льгот и акции
Цена указана с учетом льгот и акции
Цена указана с учетом льгот и акции
Цена указана с учетом льгот и акции
Цена указана с учетом льгот и акции
Цена указана с учетом льгот и акции
Цена указана с учетом льгот и акции
Цена указана с учетом льгот и акции
Цена указана с учетом льгот и акции
Цена указана с учетом льгот и акции
Цена указана с учетом льгот и акции

Цена указана с учетом льгот и акции
Цена указана с учетом льгот и акции
Цена указана с учетом льгот и акции
Цена указана с учетом льгот и акции
Цена указана с учетом льгот и акции
Цена указана с учетом льгот и акции
Цена указана с учетом льгот и акции
Цена указана с учетом льгот и акции
Цена указана с учетом льгот и акции
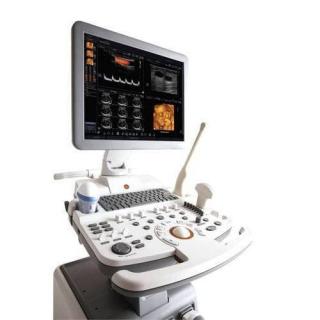
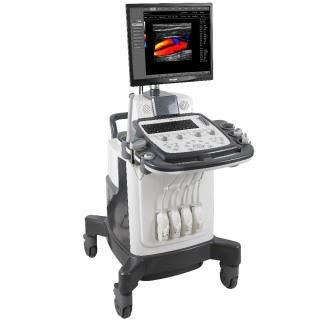
Услуга лечения онкологии
Услуга лечебного сопровождения для пациентов с онкологией — это индивидуальная комплексная помощь, которая может включать:
 Лучшиие онкологидоступ к ведущим специалистам Санкт-Петербурга, которые подберут современные схемы терапии и проконтролируют эффективность лечения на каждом этапе.
Лучшиие онкологидоступ к ведущим специалистам Санкт-Петербурга, которые подберут современные схемы терапии и проконтролируют эффективность лечения на каждом этапе. Госпитализация или дневной стационарвозможность пройти лечение в комфортных условиях ведущих онкологических центров Санкт-Петербурга.
Госпитализация или дневной стационарвозможность пройти лечение в комфортных условиях ведущих онкологических центров Санкт-Петербурга. Персональный протокол леченияразработка индивидуальной стратегии терапии с учётом типа опухоли, стадии заболевания, генетических особенностей, сопутствующих состояний и истории предыдущего лечения.
Персональный протокол леченияразработка индивидуальной стратегии терапии с учётом типа опухоли, стадии заболевания, генетических особенностей, сопутствующих состояний и истории предыдущего лечения. Второе независимое мнениеэкспертная оценка диагноза и лечебной тактики от ведущих онкологов, позволяющая подтвердить правильность выбранной стратегии, получить дополнительные варианты терапии, избежать ошибок и повысить шансы на успешный результат благодаря объективному профессиональному взгляду стороннего специалиста.
Второе независимое мнениеэкспертная оценка диагноза и лечебной тактики от ведущих онкологов, позволяющая подтвердить правильность выбранной стратегии, получить дополнительные варианты терапии, избежать ошибок и повысить шансы на успешный результат благодаря объективному профессиональному взгляду стороннего специалиста.
Лучшие специалисты в Санкт-Петербурге с рейтингом 4.5+
Последние отзывы
Что такое рак костного мозга?
Под раком костного мозга понимают группу злокачественных заболеваний кроветворной системы, при которых опухолевые клетки заполняют костномозговое пространство и вытесняют нормальное образование эритроцитов, лейкоцитов и тромбоцитов, из-за чего развиваются анемия, склонность к инфекциям, кровоточивость и могут наблюдаться поражения костей, лимфоузлов, селезёнки и центральной нервной системы.
Виды рак костного мозга
К данной группе относят острые лейкозы (острый миелобластный и острый лимфобластный лейкоз), при которых в костном мозге накапливаются бласты и быстро развивается тяжёлая анемия, тромбоцитопения и инфекционные осложнения. К хроническим процессам относятся хронический миелоидный лейкоз и хронический лимфоцитарный лейкоз, характеризующиеся более постепенным течением, длительной фазой избыточного размножения зрелых клеток и последующим истощением кроветворения.
Отдельную группу образуют плазмоклеточные неоплазии во главе с множественной миеломой и солитарной плазмоцитомой кости, при которых клональные плазматические клетки продуцируют моноклональный иммуноглобулин или его фрагменты и формируют очаги разрушения костей.
К раку костного мозга в широком понимании относят также миелодиспластические синдромы, при которых патологический клон вызывает неэффективный гемопоэз и цитопении с риском трансформации в острый лейкоз, и хронические миелопролиферативные неоплазии, прежде всего первичный миелофиброз с развитием фиброза костного мозга, экстрамедуллярного кроветворения и тяжёлых нарушений крови.
Дополнительно к данной группе причисляют системные лимфопролиферативные процессы с выраженной инфильтрацией костного мозга, в том числе отдельные варианты лимфом, при которых поражение костномозгового пространства становится важной частью клинической картины и влияет на выбор терапии.
Варианты онколечение карциномы костного мозга
Стернальная пункция костного мозга описывает морфологическую картину кроветворения и степень опухолевого замещения, поэтому выполняется для первичной диагностики поражения костного мозга, уточнения варианта лейкоза, миелодиспластического синдрома, миеломной болезни и оценки ответа на лечение. По аспирату судят о бластном пуле, созревании клеток, наличии плазматических и лимфоидных клонов, что определяет выбор схем системной терапии и целесообразность высокодозных подходов с трансплантацией стволовых клеток. Повторные пункции используют для контроля ремиссии, документирования минимальной остаточной болезни и принятия решений о смене протокола.
Трепанобиопсия костного мозга дополняет данные аспирата за счёт оценки архитектоники костномозгового пространства и степени фиброза, что критично при апластических состояниях, миелофиброзе, инфильтрации лимфомой или солидной опухолью. По биоптату судят о равномерности поражения, плотности опухолевого субстрата, сохранности нормальных ростков кроветворения, а также выполняют иммуногистохимические и молекулярные исследования. Результаты помогают различать разные варианты миелопролиферативных и лимфопролиферативных заболеваний и определяют, насколько оправданы трансплантационные и таргетные программы.
Люмбальная пункция с интратекальным введением препаратов по показаниям используется для профилактики и лечения нейролейкоза и других форм поражения центральной нервной системы при лейкозах и агрессивных лимфомах, когда опухолевые клетки проникают в ликвор. Во время процедуры отбирают спинномозговую жидкость для цитологического анализа, после чего вводят цитостатики в субарахноидальное пространство, создавая высокую локальную концентрацию препарата. Частота и длительность интратекальных введений зависят от протокола, группы риска по нейролейкозу и ответа на терапию.
Системная противоопухолевая лекарственная терапия (внутривенная и пероральная) формирует основу лечения большинства злокачественных заболеваний костного мозга, включая острые и хронические лейкозы, миелодиспластические синдромы, миелому, лимфомы с медуллярным поражением. В схему входят цитостатики, иммунохимиотерапевтические комбинации, иногда пероральные ингибиторы тирозинкиназ и другие препараты, которые подавляют патологический клон и восстанавливают нормальное кроветворение. Интенсивность, длительность и последовательность циклов зависят от возраста, соматического статуса, варианта заболевания и целей лечения.
Высокодозная лекарственная терапия с последующей поддержкой стволовыми клетками по показаниям применяется при агрессивных вариантах лейкозов, лимфом, миеломной болезни, когда требуется максимально глубокое уничтожение опухолевого клона. На начальном этапе пациент получает высокие дозы цитостатиков, которые практически полностью подавляют костномозговое кроветворение, затем ранее подготовленные гемопоэтические стволовые клетки возвращают в кровоток для восстановления функции костного мозга. Данный подход повышает шанс длительной ремиссии, но требует пребывания пациента в специализированном отделении, строгого контроля инфекций и токсичности.
Таргетная терапия при наличии молекулярной мишени используется в протоколах лечения лейкозов, лимфом и других злокачественных процессов костного мозга, когда выявлена конкретная генетическая перестройка, мутация или поверхностный рецептор. Ингибиторы тирозинкиназ, препараты против определённых сигнальных путей или анти-CD мишеней избирательно подавляют опухолевые клетки, снижая нагрузку на нормальное кроветворение. Решение о включении таргетного препарата принимают по результатам молекулярно-генетического и иммунологического обследования, а эффективность оценивают по глубине молекулярного ответа.
Иммунотерапия моноклональными антителами по показаниям дополняет химиотерапевтические схемы при лимфомах, хронических лимфолейкозах, отдельных вариантах миеломы и других заболеваниях, где опухолевые клетки экспрессируют специфические антигены. Антитело связывается с мишенью и запускает разрушение опухолевой клетки через иммунные механизмы или доставку токсического компонента, усиливая цитотоксический эффект базовой терапии, что помогает углубить ремиссию, уменьшить минимальную остаточную болезнь и в ряде случаев подготовить почву для трансплантации стволовых клеток.
Клеточная терапия CAR-T по показаниям представляет собой применение собственных Т-лимфоцитов пациента, которые в лаборатории модифицируют так, чтобы они распознавали специфический опухолевый антиген, например CD19 при некоторых В-клеточных лимфопролиферативных заболеваниях. После размножения и проверки безопасности модифицированные клетки возвращают пациенту, где они находят и уничтожают опухолевые клетки, формируя живое лекарство с потенциально длительным эффектом. Протокол применяют при рефрактерных и рецидивных формах, которые не отвечают на стандартные схемы, при условии соответствия строгим критериям отбора.
Очаговая лучевая терапия при локальных поражениях или компрессии актуальна при солитарных очагах в костях, при сдавлении спинного мозга, корешков, крупных сосудов или органов, а также при болезненных костных поражениях. Облучение уменьшает опухолевую массу в конкретной зоне, снимает боль, предупреждает патологические переломы и неврологический дефицит, улучшает качество жизни. В общую стратегию протокол вписывается так, чтобы не усиливать избыточно миелосупрессию на фоне системной химиотерапии и трансплантационных подходов.
Аутологичная трансплантация гемопоэтических стволовых клеток рассматривается при миеломе, некоторых лимфомах и других заболеваниях костного мозга, если собственные стволовые клетки пациента сохраняют способность к нормальному кроветворению. Перед высокодозной терапией стволовые клетки собирают из периферической крови после стимуляции, замораживают, а затем возвращают после проведения миелоаблатирующей химиотерапии. Метод позволяет применять более интенсивные режимы, чем без поддержки стволовыми клетками, и увеличивает вероятность глубокой и длительной ремиссии.
Аллогенную трансплантацию гемопоэтических стволовых клеток используют при острых лейкозах, миелодиспластических синдромах, некоторых миелопролиферативных заболеваниях и рефрактерных лимфомах, когда требуется не только восстановление кроветворения, но и иммунный эффект против опухолевого клона. Стволовые клетки получают от совместимого донора, после чего проводят миелоаблатирующий или редуцированный по интенсивности кондиционирующий режим и вводят донорский трансплантант. Донорская иммунная система способна распознавать остаточные опухолевые клетки, что создаёт эффект «трансплантант против лейкоза», однако требует строгого контроля реакции «трансплантант против хозяина».
Инфузия трансплантанта стволовых клеток завершает трансплантационный протокол и по технике аналогична переливанию крови, хотя по сути возвращает организму источник нового кроветворения. Клеточную взвесь из донорских или аутологичных стволовых клеток вводят внутривенно через центральный катетер в асептических условиях, контролируя гемодинамику, дыхание и возможные аллергические реакции. После инфузии наступает период аплазии костного мозга, в течение которого ведут интенсивную поддерживающую терапию до приживления трансплантанта и восстановления собственных клеточных линий.
Лейкаферез применяется при выраженном лейкоцитозе, когда избыточное количество лейкозных клеток повышает риск тромбозов, лёгочной или церебральной лейкостазы, а также перед заготовкой стволовых клеток из периферической крови. Во время процедуры кровь проходит через аппарат, который селективно удаляет необходимую фракцию клеток, а остальной объём возвращается пациенту. Метод быстро снижает опухолевую нагрузку в кровотоке или позволяет собрать нужное количество стволовых клеток для последующей трансплантации.
Плазмаферез используют при парапротеинемических состояниях, таких как миелома с высоким уровнем моноклонального белка, криоглобулинемии и других иммунокомплексных проявлениях, связанных с заболеваниями костного мозга. Во время процедуры плазму с патологическими белками удаляют и заменяют растворами или донорской плазмой, что уменьшает вязкость крови, снижает риск тромбозов и поражения органов. Плазмаферез сочетают с системной противоопухолевой терапией, так как сам по себе он не устраняет опухолевый клон, а только уменьшает последствия его активности.
Переливание эритроцитарной массы требуется при анемии, связанной с замещением костного мозга опухолью, миелосупрессией от химиотерапии или кровопотерей. Концентрат эритроцитов вводят по строгим показаниям с учётом уровня гемоглобина, симптомов гипоксии, сопутствующей кардиальной патологии, подбирают компоненты крови по группе и резус-фактору, что улучшает переносимость лечения, уменьшает одышку, слабость, головокружение и позволяет проводить запланированные курсы терапии без опасной задержки.
Переливание тромбоцитарного концентрата выполняют при выраженной тромбоцитопении, особенно на фоне индукционной и консолидационной терапии лейкозов, высокодозных режимов и трансплантации стволовых клеток, когда возрастает риск спонтанных кровотечений. Тромбоциты вводят профилактически при критических значениях или при наличии клинических признаков кровоточивости, подбирают по системе совместимости, оценивают прирост уровня после трансфузии. Своевременная трансфузионная поддержка позволяет безопаснее проводить агрессивные протоколы, не прерывая их из-за осложнений.
Введение колониестимулирующих факторов по показаниям используют для ускорения восстановления нейтрофильного ряда после миелосупрессивной химиотерапии, высокодозных режимов и трансплантации, а также при тяжёлой нейтропении с высоким риском инфекций. Препараты вводят подкожно по индивидуально подобранной схеме, ориентируясь на динамику абсолютного числа нейтрофилов и общую клиническую картину. Данная поддержка сокращает длительность периода глубокой нейтропении, уменьшает частоту тяжёлых инфекций и позволяет поддерживать интенсивность противоопухолевого лечения.
Антибактериальная, противогрибковая и противовирусная терапия и профилактика на фоне нейтропении являются обязательной частью протоколов лечения рака костного мозга, так как подавление иммунитета создаёт высокий риск тяжёлых инфекций. При появлении лихорадки на фоне нейтропении стартуют эмпирические антибиотики широкого спектра, при длительной нейтропении добавляют противогрибковые препараты, а при специфических вирусных рисках используют противовирусные средства и профилактику. Выбор схем основывается на локальных эпидемиологических данных, предыдущей антибактериальной нагрузке и сопутствующих поражениях органов, а сам контроль инфекций определяет безопасность проведения агрессивных химиотерапевтических и трансплантационных протоколов.
Помощь онкобольным
Помощь при нейтропении и риске инфекций при раке костного мозга опирается на чёткие правила гигиены, контролируемый контакт с окружающими и рациональное использование антибактериальной, противогрибковой и противовирусной профилактики. Пациенту заранее объясняют, что лихорадка на фоне нейтропении рассматривается, как неотложное состояние, поэтому при повышении температуры выше согласованного порога требуется немедленный выезд в стационар без попыток лечиться самостоятельно. В отделении используют маски, антисептики для рук, иногда боксы с фильтрацией воздуха, контролируют очаги хронической инфекции в полости рта, коже, а при длительном падении нейтрофилов назначают поддерживающие курсы антиинфекционных препаратов и колониестимулирующих факторов, чтобы сократить период глубокого иммунного дефицита.
Поддержка при анемии и тромбоцитопении связана с трансфузионной терапией и профилактикой кровотечений, поэтому заранее проговаривается, при каких значениях гемоглобина и тромбоцитов необходимы переливания. Пациент получает рекомендации по ограничению травмоопасной активности, отказу от внутримышечных инъекций и приёма лекарств, повышающих риск кровотечений. В стационаре подбирают эритроцитарную массу и тромбоцитарный концентрат с учётом группы, резус-принадлежности и степени совместимости, контролируют реакцию на трансфузию, динамику уровня клеток крови и при необходимости корректируют график химиотерапии, чтобы избежать опасной глубины цитопений.
Контроль боли, костных поражений и общих симптомов при раке костного мозга включает ступенчатую анальгезию, использование противоопухолевых и поддерживающих средств, укрепляющих костную ткань. При миеломе и метастатическом поражении костей применяют препараты, влияющие на ремоделирование кости, локальное облучение болезненных очагов, ортопедические вмешательства для профилактики патологических переломов, подбор ортезов и средств разгрузки. Схема обезболивания формируется так, чтобы ночной сон был полноценным, повседневная активность оставалась по возможности сохранённой, а пациент не боялся своевременно сообщать об усилении боли, чтобы пересмотр доз и препаратов происходил до развития тяжёлого болевого кризиса.
Профилактика и коррекция осложнений со стороны слизистых и желудочно-кишечного тракта особенно важны на фоне высокодозной химиотерапии, интратекального лечения и трансплантационных протоколов. Перед курсами терапии стоматолог и гематолог очищают полость рта от очагов хронической инфекции, обучают мягкой гигиене, применению ополаскивателей без спирта, местных средств при признаках мукозита. Для уменьшения тошноты и рвоты используют современные противорвотные препараты по заранее составленной схеме, при диарее и болях в животе подбирают щадящий рацион, сорбенты и регидратацию, а при запорах на фоне приема опиоидов — мягкие слабительные и режим питья, чтобы не допустить тяжёлых осложнений со стороны кишечника.
Нутритивная поддержка и физическая реабилитация при раке костного мозга направлены на сохранение массы тела, мышечной силы и переносимости лечения. Диетолог оценивает исходное состояние питания, при выраженной слабости и снижении аппетита предлагает высококалорийные смеси, частое дробное питание, при невозможности достаточного приёма через рот обсуждаются зондовые методы и парентеральное питание. Реабилитолог формирует индивидуальный план ЛФК с учётом анемии, риска переломов и ограничений по активности: короткие прогулки, дыхательные упражнения, работа с мелкой моторикой, постепенное расширение нагрузки после трансплантации и интенсивных курсов, чтобы уменьшить выраженность астении и ускорить возвращение к самостоятельности.
Психологическая и социальная помощь при заболеваниях костного мозга имеет самостоятельное значение, так как лечение длительное, часто связанное с изоляцией, потерей привычной роли в семье и работе, страхом рецидива. Психоонколог помогает преодалеть тревогу, страх боли и возможных изменений внешности и образа жизни, предлагает техники расслабления, дыхательные практики, когнитивные подходы к работе с навязчивыми тревожными мыслями, при необходимости совместно с гематологом подбирает медикаментозную поддержку.
Какие врачи могут быть вовлечены
- Гематолог организует всю лечебную стратегию при раке костного мозга, выбирает протоколы системной химиотерапии, таргетной и иммунотерапии, планирует очередность курсов и объём обследований для оценки ремиссии. Через гематолога проходят решения о необходимости стернальной пункции, трепанобиопсии, люмбальных пункций, обсуждение высокодозных режимов и подготовки к трансплантации стволовых клеток, именно он интерпретирует результаты морфологии и молекулярных тестов и переводит их в конкретный план лечения.
- Трансплантолог-гематолог отвечает за этапы высокодозной терапии и трансплантации гемопоэтических стволовых клеток, определяет показания к аутологичной или аллогенной трансплантации с учётом риска рецидива, возраста и сопутствующей патологии. Врач планирует заготовку стволовых клеток, выбирает донорскую стратегию, назначает кондиционирующие режимы, ведёт пациента в период аплазии костного мозга и контролирует приживление трансплантата и проявления реакции «трансплантант против хозяина».
- Врач клеточной терапии участвует в отборе пациентов для CAR-T, организует забор Т-лимфоцитов, координирует этап лабораторной модификации и возвращение клеточного продукта. На враче лежит ответственность за оценку риска синдрома высвобождения цитокинов, нейротоксичности, подготовку премедикации и план мониторинга в первые недели после инфузии, когда эффекты клеточного препарата наиболее выражены.
- Анестезиолог-реаниматолог необходим при тяжёлых состояниях, связанных с агрессивными протоколами, сепсисом, тяжёлой дыхательной недостаточностью или выраженной полиорганной токсичностью. Данный врач обеспечивает безопасное проведение инвазивных процедур, контролирует гемодинамику и дыхание в реанимации, подбирает инфузионную терапию, респираторную поддержку и анальгезию, создаёт условия для выхода из критического состояния и продолжения противоопухолевого лечения.
- Инфекционист подключается при длительной нейтропении, повторных эпизодах лихорадки неясного генеза, тяжёлых бактериальных, грибковых или вирусных инфекциях на фоне химиотерапии и трансплантации. Также инфекционист помогает выстроить рациональную схему антибактериальной, противогрибковой и противовирусной терапии, учитывая локальную резистентность флоры, предшествующие курсы и поражение органов, определяет объём профилактики на период глубокой иммуносупрессии.
- Трансфузиолог курирует трансфузионную поддержку при анемии и тромбоцитопении, подбирает эритроцитарную массу и тромбоцитарный концентрат, проводит иммунологическое типирование и решает вопросы при сложных вариантах несовместимости. От решений врача зависят безопасность переливаний, риск гемолитических реакций и эффективность подъёма уровня гемоглобина и тромбоцитов, что позволяет без задержек проводить интенсивные химиотерапевтические и трансплантационные протоколы.
- Радиотерапевт участвует в лечении при локальных поражениях костей, очагах в позвоночнике с угрозой компрессии спинного мозга, болезненных метастатических инфильтратах и очаговой устойчивости к системной терапии. Радиотерапевт планирует поля облучения, дозу и режим фракционирования, стремясь добиться уменьшения опухолевой массы в проблемной зоне, снять болевой синдром и предупредить неврологические осложнения при минимально возможной дополнительной нагрузке на костный мозг.
- Кардиолог и нефролог вовлекаются при кардиотоксичности и нефротоксичности, которые возникают на фоне антрациклинов, платиносодержащих препаратов, ингибиторов тирозинкиназ и интенсивной инфузионной терапии. Кардиолог оценивает исходное состояние сердца, корректирует терапию при сердечной недостаточности, аритмиях и ишемии, адаптирует объём нагрузок и инфузий, а нефролог контролирует функцию почек, подбирает режимы коррекции электролитных нарушений, решает вопрос о необходимости заместительной почечной терапии и влияет на выбор доз лекарств.
- Диетолог и реабилитолог помогают пациенту с раком костного мозга сохранять функциональность на протяжении длительного лечения, формируя основу нутритивной и физической поддержки. Диетолог оценивает дефицит массы тела, аппетит, переносимость пищи, подбирает высокобелковый и высококалорийный рацион, при необходимости рекомендует зондовые смеси и варианты парентерального питания, а реабилитолог создаёт программу щадящей физической активности, направленную на борьбу с астенией, профилактику тромбозов и восстановление мышечной силы после интенсивных курсов и трансплантации.
- Психоонколог и клинический психолог необходимы из-за высокой эмоциональной нагрузки пациента, связанной с диагнозом, длительными госпитализациями, изоляцией и риском рецидива. Данные специалисты помогают справляться с тревогой перед пункциями костного мозга и высокодозной терапией, учат техникам совладания с бессонницей и навязчивыми мыслями, поддерживают в период ожидания результатов и при смене линий лечения. Параллельно выстраивается работа с семьёй, чтобы близкие понимали реальные ограничения и могли оказывать поддержку без давления и обесценивания переживаний.
Какие обследования назначаются
- Общий анализ крови относится к базовым обследованиям при раке костного мозга, по нему судят о степени анемии, выраженности лейкоцитоза или лейкопении, уровне тромбоцитов, появлении бластных клеток в периферической крови. Динамика показателей отражает ответ на химиотерапию и таргетные режимы, помогает вовремя заметить глубокую цитопению, скорректировать дозы препаратов и сроки очередного цикла лечения. При подозрении на прогрессирование или рецидив настораживают повторное появление бластов, рост лейкоцитов или внезапное падение тромбоцитов.
- Биохимические исследования крови и коагулограмма позволяют оценить функцию печени и почек, электролитный баланс, уровень белка, кальция, ЛДГ, а также состояние свёртывающей системы. Полученные данные важны для подбора схем химиотерапии и таргетной терапии, расчёта доз при нарушениях функции органов, раннего выявления синдрома лизиса опухоли и риска кровотечений. При миеломе особое внимание уделяется уровням креатинина, кальция, общего белка и фракциям белков, при агрессивных лейкозах и лимфомах — ЛДГ и показателям свёртывания.
- Серологические и молекулярные тесты на инфекции используют для выявления и контроля вирусных и бактериальных агентов, способных осложнять лечение рака костного мозга. Обследование на вирусные гепатиты, ВИЧ, ЦМВ, вирус Эпштейна–Барра, герпес-группу, а также на некоторые бактериальные инфекции необходимо перед высокодозной терапией и трансплантацией стволовых клеток. Результаты определяют выбор противовирусной и антибактериальной профилактики, объём наблюдения и допустимую интенсивность иммуносупрессивных режимов.
- Электрокардиография и УЗИ сердца относятся к обязательным обследованиям перед интенсивной химиотерапией, высокодозными режимами и трансплантацией гемопоэтических стволовых клеток. По ЭКГ выявляют нарушения ритма, проводимости, признаки ишемии, а по эхокардиографии оценивают сократимость миокарда и состояние клапанов, что влияет на выбор антрациклинов, объём инфузионной терапии и уровень допустимой нагрузки. При длительном лечении и появлении одышки, отёков или болей в груди исследования повторяют, чтобы вовремя диагностировать кардиотоксичность и скорректировать протокол.
- Ультразвуковое исследование органов брюшной полости и почек и УЗИ лимфоузлов помогает оценить состояние печени и селезёнки, выявить лимфаденопатию, инфильтрацию органов и осложнения химиотерапии. По УЗИ судят о наличии гепатоспленомегалии, изменении структуры печени и почек, скоплении жидкости в брюшной полости, что бывает при лимфомах, лейкозах и миеломе. При изменении клинической картины и подозрении на осложнения (тромбозы, инфаркты органов, лекарственное поражение) исследование повторяют.
- Компьютерная томография с контрастированием назначается при лимфомах и системных процессах с вовлечением костного мозга, а также при осложнениях у пациентов с лейкозами и миеломой. КТ позволяет увидеть медиастинальные и абдоминальные лимфоузлы, инфильтрацию органов, очаги в лёгких, плевральные выпоты, зоны пневмонии или кровоизлияний. Результаты учитывают при стадировании, оценке ответа на терапию и выборе тактики интервенционных вмешательств.
- Рентгенографии костей используются для выявления очагов разрушения, остеолиза, патологических переломов, характерных для миеломы и некоторых лимфопролиферативных процессов. При подозрении на множественные очаги и при планировании ортопедических вмешательств информативнее МСКТ, которая показывает степень истончения кортикального слоя и прогнозирует риск перелома. На фоне лечения повторные исследования позволяют оценить стабилизацию или прогрессирование костных изменений и определить необходимость локальной лучевой терапии или хирургической фиксации.
- Магнитно-резонансная томография всего позвоночника помогает оценить протяжённость поражения, компрессию спинного мозга и корешков, а также выявить субклинические очаги, не видимые по рентгенографии. МРТ особенно востребована при подозрении на эпидуральную компрессию, инфильтрацию тел позвонков, ранние изменения в костном мозге при миеломе и лейкозах. Результаты определяют срочность начала стероидной терапии, лучевого вмешательства и объём нейрохирургической помощи.
- ПЭТ-КТ используют при некоторых лимфомах и других системных опухолях, поражающих костный мозг, для точного стадирования и контроля ответа. Исследование показывает метаболически-активные очаги в костях, лимфоузлах и органах, помогает отличить остаточную фиброзную ткань от живой опухоли. В динамике по ПЭТ-КТ судят о глубине ремиссии и необходимости смены протокола при недостаточном снижении метаболической активности.
- Миелограмма по результатам стернальной пункции костного мозга относится к ключевым обследованиям при раке костного мозга, так как отражает клеточный состав, процент бластов и состояние отдельных ростков кроветворения. По миелограмме различают острые и хронические лейкозы, миелодиспластические синдромы, миелопролиферативные заболевания, фиксируют ответ на индукционную и консолидационную терапию. Повторные исследования позволяют документировать полную ремиссию, минимальную остаточную болезнь и момент гематологического рецидива.
- Гистологическое и иммуногистохимическое исследование трепанобиоптата костного мозга дополняет миелограмму за счёт оценки пространственной архитектуры и степени опухолевой инфильтрации. В биоптате определяют наличие фиброза, плотность и характер опухолевого роста, распределение нормальных и патологических клеточных клонов, экспрессию ключевых маркеров. Эти данные критичны при миелофиброзе, инфильтрации костного мозга лимфомой, солидной опухолью, а также при вариантах лейкозов и миелодиспластических синдромов с неоднозначной картиной аспирата.
- Иммунофенотипирование опухолевых клеток методом проточной цитометрии используют для уточнения варианта лейкозов и лимфом, определения линии дифференцировки, стадии созревания и наличия специфических антигенов. По панели маркеров устанавливают, относится ли процесс к В- или Т-клеточной линии, миелоидному или смешанному варианту, выделяют отдельные подтипы с особыми протоколами лечения. На основе иммунофенотипа подбирают моноклональные антитела, решают вопрос о возможности применения CAR-T и формируют схему мониторинга минимальной остаточной болезни.
- Цитогенетические исследования и молекулярно-генетический анализ (кариотипирование, ФИШ, ПЦР, панели NGS) выявляют хромосомные аномалии и мутации, определяющие прогноз и выбор таргетной терапии. Обнаружение транслокаций, делеций, инверсий и точечных мутаций позволяет отнести заболевание к определённой группе риска, подобрать ингибиторы тирозинкиназ, другие таргетные препараты и оценить глубину молекулярного ответа. Мониторинг данных показателей в динамике служит критерием эффективности лечения и поводом к смене протокола при потере ответа.
- Исследование ликвора после люмбальной пункции применяется при лейкозах и агрессивных лимфомах для диагностики и контроля поражения центральной нервной системы. В образце ищут бластные клетки, проводят цитологический и иногда иммунологический анализ, оценивают эффект интратекальной терапии. Результаты влияют на интенсивность профилактики нейролейкоза, частоту повторных пункций и решение о дополнительном системном или лучевом воздействии на ЦНС.
Что важно знать пациентам
Излечима ли онкология костного мозга?
При острых лейкозах и части агрессивных лимфом целью терапии зачастую является именно излечение, когда с помощью нескольких этапов химиотерапии, таргетных и иммунных препаратов и при показаниях аллогенной трансплантации удаётся добиться глубокой ремиссии без признаков болезни на протяжении многих лет. При миеломе, некоторых хронических лейкозах и миелодиспластических синдромах чаще говорят о длительном контроле, когда болезнь удерживается под воздействием последовательных линий лечения.
Какая длительность онколечения?
Схема обследований и курсов выстраивается так, чтобы удар по опухолевому клону был последовательным и не давал ему времени восстановиться, при этом токсичность оставалась управляемой, поэтому перенос или самовольное «растягивание» лечения может уменьшать шанс глубокой ремиссии. Регулярные анализы крови, стернальные пункции, трепанобиопсии и молекулярные тесты нужны, чтобы вовремя заметить минимальную остаточную активность, начальные признаки рецидива или опасную токсичность и успеть скорректировать протокол, пока клиническое состояние пациента остаётся стабильным.
Какие осложнения?
Срочного обследования требуют лихорадка на фоне низких нейтрофилов, озноб, резкая слабость, одышка, боль в груди, спутанность сознания, появление крови в моче, стуле или при чистке зубов, а также любые необычные кровоизлияния на коже и слизистых. Опасными признаками являются сильная головная боль с рвотой, внезапное ухудшение зрения, выраженная одышка или ощущение перебоев в работе сердца, потому что за ними могут стоять тяжёлые инфекции, кровотечения, тромбозы, эмболии или синдром лизиса, которые поддаются контролю только при раннем начале интенсивной терапии в стационаре.
Как легче перенести онкотерапию?
Очень важно, чтобы онкопациент и его близкие хорошо понимали смысл каждого этапа — от индукционной терапии до возможной трансплантации и последующего наблюдения, поэтому на приёме имеет смысл задавать конкретные вопросы и записывать ответы, а не стесняться уточнять непонятные моменты. Существенно облегчает онкотерапию заранее организованный быт: помощь с поездками в онкоцентр, приготовлением пищи, соблюдением гигиенических мер, уходом за центральным катетером и приёмом препаратов, а психологическая поддержка, работа с психоонкологом и открытый разговор в семье о страхах и ожиданиях снижают чувство одиночества и делают лечение общей задачей, а не личной изоляцией пациента с диагнозом.