- ДИАГНОСТИКА
- МРТ
- КТ
- КТ ГОЛОВЫ
- КТ ШЕИ
- КТ ГРУДНОЙ КЛЕТКИ
- КТ БРЮШНОЙ ПОЛОСТИ
- КТ МАЛОГО ТАЗА
- КТ ПОЗВОНОЧНИКА
- КТ СУСТАВОВ
- КТ КОСТЕЙ
- КТ АНГИОГРАФИЯ
- КТ ЗУБОВ
- УЗИ
- УЗИ ОРГАНОВ МАЛОГО ТАЗА
- УЗИ БРЮШНОЙ ПОЛОСТИ
- УЗИ ЗАБРЮШИННОГО ПРОСТРАНСТВА
- УЗИ СЕРДЦА
- УЗИ СОСУДОВ
- УЗИ МЯГКИХ ТКАНЕЙ, НЕРВОВ И ЖЕЛЕЗ
- УЗИ СУСТАВОВ
- УЗИ ГОЛОВЫ
- УЗИ ЛИМФОУЗЛОВ
- УЗИ ПРИ БЕРЕМЕННОСТИ
- УЗИ ПЛОДА
- УЗИ НОВРОЖДЕННОМУ РЕБЕНКУ
- УЗИ ПОСЛЕ АБОРТА
- РЕНТГЕН
- ВРАЧИ
- КАКОЙ ВРАЧ ЛЕЧИТ
- АКУШЕР-ГИНЕКОЛОГ
- АЛЛЕРГОЛОГ
- ВЕРТЕБРОЛОГ
- ВЕСТИБУЛОЛОГ
- ГАСТРОЭНТЕРОЛОГ
- ГЕМАТОЛОГ
- ГИНЕКОЛОГ
- ДЕРМАТОЛОГ
- ДИЕТОЛОГ
- ИГЛОТЕРАПЕВТ
- ИММУНОЛОГ
- ИНФЕКЦИОНИСТ
- КАРДИОЛОГ
- ВРАЧ ЛЕЧЕБНОЙ ФИЗКУЛЬТУРЫ
- МАММОЛОГ
- НЕВРОЛОГ
- НЕЙРОХИРУРГ
- НЕОНАТОЛОГ
- НЕФРОЛОГ
- ОНКОЛОГ
- ОНКОЛОГ-МАММОЛОГ
- ОРТОПЕД
- ОРТОПЕД-ХИРУРГ
- ОТОЛАРИНГОЛОГ
- ОФТАЛЬМОЛОГ
- ОСТЕОПАТ
- ПЕДИАТР
- ПРОКТОЛОГ
- ПСИХИАТР
- ПСИХОТЕРАПЕВТ
- ПУЛЬМОНОЛОГ
- РЕВМАТОЛОГ
- РЕФЛЕКСОТЕРАПЕВТ
- СЕКСОЛОГ
- СОМНОЛОГ
- СОСУДИСТЫЙ ХИРУРГ
- СПОРТИВНЫЙ ВРАЧ
- ТЕРАПЕВТ
- ТРАВМАТОЛОГ
- ТРИХОЛОГ
- УРОЛОГ
- ФИЗИОТЕРАПЕВТ
- ФЛЕБОЛОГ
- ФТИЗИАТР
- ВРАЧ ФУНКЦИОНАЛЬНОЙ ДИАГНОСТИКИ
- ХИРУРГ
- ЭНДОКРИНОЛОГ
- ЭНДОСКОПИСТ
- ЭПИЛЕПТОЛОГ
- СПОРТИВНЫЙ МАССАЖИСТ
- ГЕПАТОЛОГ
- ПАРАЗИТОЛОГ
- МАНУАЛЬНЫЙ ТЕРАПЕВТ
- СЕМЕЙНЫЙ ПСИХОЛОГ
- ВРАЧ ОБЩЕЙ ПРАКТИКИ
- ПРОФПАТОЛОГ-ТЕРАПЕВТ
- АНДРОЛОГ
- АНГИОЛОГ
- АРИТМОЛОГ
- АРТРОЛОГ
- БРОНХОЛОГ
- ВЕНЕРОЛОГ
- ГЕМОСТАЗИОЛОГ
- ГИРУДОТЕРАПЕВТ
- ДИАБЕТОЛОГ
- КИНЕЗИОЛОГ
- РАДИОТЕРАПЕВТ
- РЕПРОДУКТОЛОГ
- СУРДОЛОГ
- ФОНИАТР
- ХИМИОТЕРАПЕВТ
- СКИДКИ
- НА КАРТЕ
- МРТ РЯДОМ (поиск по району)
- АДМИРАЛТЕЙСКИЙ РАЙОН
- ВАСИЛЕОСТРОВСКИЙ РАЙОН
- ВЫБОРГСКИЙ РАЙОН
- КАЛИНИНСКИЙ РАЙОН
- КИРОВСКИЙ РАЙОН
- КОЛПИНСКИЙ РАЙОН
- КРАСНОГВАРДЕЙСКИЙ РАЙОН
- КРАСНОСЕЛЬСКИЙ РАЙОН
- КРОНШТАДТСКИЙ РАЙОН
- КУРОРТНЫЙ РАЙОН
- МОСКОВСКИЙ РАЙОН
- НЕВСКИЙ РАЙОН
- ПЕТРОГРАДСКИЙ РАЙОН
- ПЕТРОДВОРЦОВЫЙ РАЙОН
- ПРИМОРСКИЙ РАЙОН
- ПУШКИНСКИЙ РАЙОН
- ФРУНЗЕНСКИЙ РАЙОН
- ЦЕНТРАЛЬНЫЙ РАЙОН
- ЛЕН. ОБЛАСТЬ
- КТ и МСКТ РЯДОМ (поиск по району)
- АДМИРАЛТЕЙСКИЙ РАЙОН
- ВАСИЛЕОСТРОВСКИЙ РАЙОН
- ВЫБОРГСКИЙ РАЙОН
- КАЛИНИНСКИЙ РАЙОН
- КИРОВСКИЙ РАЙОН
- КОЛПИНСКИЙ РАЙОН
- КРАСНОГВАРДЕЙСКИЙ РАЙОН
- КРАСНОСЕЛЬСКИЙ РАЙОН
- КРОНШТАДТСКИЙ РАЙОН
- КУРОРТНЫЙ РАЙОН
- МОСКОВСКИЙ РАЙОН
- НЕВСКИЙ РАЙОН
- ПЕТРОГРАДСКИЙ РАЙОН
- ПЕТРОДВОРЦОВЫЙ РАЙОН
- ПРИМОРСКИЙ РАЙОН
- ПУШКИНСКИЙ РАЙОН
- ФРУНЗЕНСКИЙ РАЙОН
- ЦЕНТРАЛЬНЫЙ РАЙОН
- ЛЕН. ОБЛАСТЬ
- МРТ АДРЕСА БОЛЬНИЦ В СПБ
- МРТ РЯДОМ (поиск по району)
Адреса и стоимость персонализированной онкотерапии в СПБ
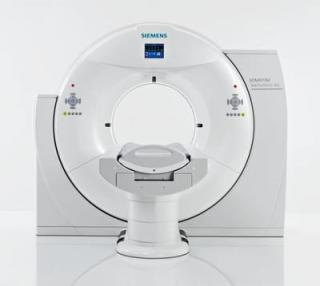
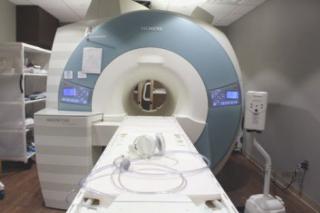
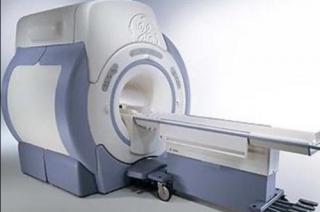
Услуга лечения онкологии
Услуга лечебного сопровождения для пациентов с онкологией — это индивидуальная комплексная помощь, которая может включать:
 Лучшиие онкологидоступ к ведущим специалистам Санкт-Петербурга, которые подберут современные схемы терапии и проконтролируют эффективность лечения на каждом этапе.
Лучшиие онкологидоступ к ведущим специалистам Санкт-Петербурга, которые подберут современные схемы терапии и проконтролируют эффективность лечения на каждом этапе. Госпитализация или дневной стационарвозможность пройти лечение в комфортных условиях ведущих онкологических центров Санкт-Петербурга.
Госпитализация или дневной стационарвозможность пройти лечение в комфортных условиях ведущих онкологических центров Санкт-Петербурга. Персональный протокол леченияразработка индивидуальной стратегии терапии с учётом типа опухоли, стадии заболевания, генетических особенностей, сопутствующих состояний и истории предыдущего лечения.
Персональный протокол леченияразработка индивидуальной стратегии терапии с учётом типа опухоли, стадии заболевания, генетических особенностей, сопутствующих состояний и истории предыдущего лечения. Второе независимое мнениеэкспертная оценка диагноза и лечебной тактики от ведущих онкологов, позволяющая подтвердить правильность выбранной стратегии, получить дополнительные варианты терапии, избежать ошибок и повысить шансы на успешный результат благодаря объективному профессиональному взгляду стороннего специалиста.
Второе независимое мнениеэкспертная оценка диагноза и лечебной тактики от ведущих онкологов, позволяющая подтвердить правильность выбранной стратегии, получить дополнительные варианты терапии, избежать ошибок и повысить шансы на успешный результат благодаря объективному профессиональному взгляду стороннего специалиста.
Лучшие специалисты в Санкт-Петербурге с рейтингом 4.5+
Последние отзывы
Что такое цитогенетическая терапия при раке кожи?
Под цитогенетической терапией понимают подход, при котором выбор лекарств опирается на генетические и молекулярные особенности опухоли кожи, а не только на локализацию и стадию. Исследуются мутации BRAF, KIT, NRAS, изменения в генах пути Hedgehog, перестройки NTRK, уровень микросателлитной нестабильности и другие маркеры, после чего подбираются препараты, действующие на выявленные мишени или усиливающие реакцию иммунной системы. Данный подход в ряде случаев позволяет добиться более длительного контроля заболевания при меньшей общей токсичности по сравнению с одной лишь химиотерапией.
Варианты персонализированной онкотерапии
Схемы с ингибиторами BRAF и MEK эффективны при метастатической и нерезектабельной меланоме с подтверждённой по результатам молекулярного анализа опухолевой ткани или метастаза мутацией BRAF V600. В зависимости от клинической ситуации используются комбинации дабрафениба и траметиниба, вемурафениба и кобиметиниба, энкорафениба и бинметиниба. Препараты выбираются с учётом скорости прогрессии, сопутствующей патологии, риска лихорадочных реакций и кожных осложнений. На практике подобные комбинации нередко занимают одну из первых линий для пациентов с выраженной опухолевой массой, когда требуется быстрый ответ, а в дальнейшем при стабилизации состояния обсуждается переход к иммунотерапии. Важную роль играет мониторинг побочных эффектов, так как высокая эффективность сочетается с характерной токсичностью, которая вызывает лихорадку, кожные высыпания, фоточувствительность и нарушения функции печени.
Протоколы с таргетным воздействием на KIT и NRAS-ассоциированные сигнальные пути рассматриваются при акральной, слизистой меланоме и ряде редких вариантов, когда в опухоли обнаруживаются мутации или амплификации гена KIT, либо активирующие изменения в NRAS. В подобных ситуациях возможны схемы с использованием иматиниба или других тирозинкиназных ингибиторов при KIT-позитивных опухолях, а также применение MEK-ингибиторов при NRAS-мутациях, чаще в рамках клинических исследований или индивидуальных протоколов. Решение принимается после расширенного молекулярного профилирования, так как вероятность соответствующих нарушений ниже, чем у BRAF-мутаций, а клинический эффект зависит от конкретного типа изменения. Подобные схемы нередко комбинируются с иммунотерапией или химиотерапией, если требуется усилить противоопухолевое действие.
Ингибиторы пути Hedgehog применяют при местнораспространённой и метастатической базальноклеточной карциноме кожи, если хирургическое вмешательство и стандартная лучевая терапия уже не рассматриваются, как оптимальная тактика. В основе терапии лежит знание о частых изменениях в генах PTCH и SMO, приводящих к постоянной активации сигнального пути, поэтому в протокол вводятся препараты типа висмодегиба или сонидегиба. Онколечение ориентировано на длительный приём с регулярной оценкой ответа по клинической картине и результатам визуализирующих исследований, а также контролем побочных эффектов, среди которых часто отмечаются мышечные боли, изменение вкуса, алопеция и потеря массы тела. При хорошем эффекте объём опухоли уменьшается, что в ряде клинических случаев открывает возможность для органосохраняющих хирургических вмешательств.
Иммунотерапевтические схемы с блокадой PD-1/PD-L1 и CTLA-4 формируют отдельное направление, основанное на высокой мутационной нагрузке меланомы и плоскоклеточного рака кожи, что делает опухолевые клетки особенно заметными для иммунной системы. В лечении используют препараты ниволумаб, пембролизумаб, ипилимумаб, а при распространённом плоскоклеточном варианте — также PD-1-ингибиторы. Комбинация PD-1 и CTLA-4-блокады выбирается при агрессивном течении и хорошем функциональном статусе, монотерапия PD-1 предпочтительна при более осторожной тактике. При выборе схемы учитываются сопутствующие аутоиммунные заболевания, риск эндокринных, кишечных и кожных иммунных осложнений, необходимость длительного наблюдения с возможностью ранней коррекции токсичности.
Протоколы, ориентированные на редкие молекулярные мишени, эффективны при выявлении перестроек NTRK, выраженной микросателлитной нестабильности, высокой мутационной нагрузки по результатам широкого геномного тестирования. При обнаружении NTRK-фузий допустима терапия трек-ингибиторами, при MSI-high-профиле и значительной мутационной нагрузке обсуждается назначение иммунных препаратов по принципу тканенезависимого показания. Для ряда редких сарком мягких тканей кожи также рассматриваются схемы, основанные на специфических транслокациях и мутациях. Подобные протоколы зачастую используются после исчерпания стандартных линий, однако при наличии чёткой мишени способны существенно изменить прогноз.
Помощь онкобольным
Генетическое консультирование и анализ семейного анамнеза особенно важны при множественных меланомах, раннем возрасте развития злокачественного поражения, семейных случаях заболевания, когда выявляются мутации CDKN2A, CDK4, BAP1 и других генов предрасположенности. Консультация помогает понять, какие риски связаны с наследственным вариантом, кому из родственников целесообразно проходить тестирование и в каком возрасте, как выстраивать программу наблюдения для носителей. Обсуждаются дерматологические осмотры, дерматоскопия, режим фотозащиты, возможные профилактические вмешательства при диспластических невусах. Психологическая поддержка снижает тревогу, связанную с необходимостью сообщать о рисках детям и другим членам семьи.
Сопровождение при токсичности таргетной терапии и иммунной терапии опирается на раннее распознавание кожных высыпаний, диареи, эндокринных нарушений, поражения печени и лёгких. Пациент получает подробные инструкции, какие симптомы следует считать поводом для немедленного контакта с лечащей командой: нарастающая одышка, упорный кашель, сильная диарея, выраженная сыпь с пузырями, резкое изменение веса или настроения. В схемы поддержки входят местные стероиды и увлажняющие средства при кожных реакциях, антидиарейные препараты и регидратация при поражении кишечника, заместительная гормональная терапия при эндокринопатиях. При тяжёлых осложнениях временно прекращается приём противоопухолевого препарата и вводятся системные глюкокортикоиды под контролем онколога.
Дерматологический уход и фотопротекция занимают центральное место в повседневной жизни пациента с кожной формой рака, особенно при длительном приёме таргетных препаратов, усиливающих чувствительность к ультрафиолету. Врач подробно объясняет принципы использования солнцезащитных средств с высоким фактором, выбора одежды, головных уборов, поведения на солнце, а также осмотра кожи в домашних условиях. Регулярные визиты к дерматологу позволяют оценивать новые пигментные образования, контролировать состояние рубцов после операций, вовремя выявлять подозрительные изменения. Важна и гигиена поражённых участков с использованием мягких средств без агрессивных добавок, чтобы не усиливать раздражение.
Психологическая и социальная поддержка особенно значима при выраженной косметической деформации, локализации опухоли на лице, открытых участках тела, кистях, когда меняется восприятие собственного внешнего вида и возникают сложности в общении. Психоонколог помогает пациенту сформировать новые способы адаптации, снизить уровень стыда и самообвинений, научиться говорить о своём состоянии с близкими и коллегами. При необходимости подключается социальный работник, который помогает решить вопросы оформления инвалидности, временной утраты трудоспособности, подбора подходящих условий труда. Группы взаимопомощи дают возможность обмениваться практическими советами и получать эмоциональную поддержку от людей с похожим опытом.
Нутритивная поддержка и коррекция образа жизни направлены на сохранение сил в условиях длительной цитогенетически-ориентированной терапии и возможных ограничений физической активности. Диетолог помогает подобрать рацион с учётом снижения аппетита, вкусовых изменений, эпизодов тошноты или диареи. Отдельно обсуждаются отказ от курения, ограничение алкоголя, посильная аэробная нагрузка и упражнения на растяжку, которые улучшают общее самочувствие и уменьшают усталость. Чёткий, но гибкий план дня с чередованием активности и отдыха снижает чувство беспомощности и помогает пациентам лучше переносить длительное лечение.
Какие врачи могут быть вовлечены
- Онколог формирует общую стратегию лекарственного лечения при меланоме, плоскоклеточном и базальноклеточном раке кожи, сопоставляя стадию процесса, локализацию метастазов, результаты молекулярных тестов и общее состояние пациента. На консилиуме именно данный специалист предлагает, в какой последовательности использовать таргетные комбинации BRAF/MEK, иммунотерапию, ингибиторы пути Hedgehog и другие препараты, ориентированные на генетические изменения. В ходе терапии оценивается динамика очагов по данным визуализирующих исследований, переносимость схем, необходимость коррекции доз и интервалов, а при прогрессии подбирается следующая линия с учётом обновлённого профиля опухоли.
- Дерматоонколог отвечает за оценку кожных проявлений заболевания и побочных эффектов цитогенетически-ориентированной терапии. На до-терапевтическом этапе тщательно осматривается кожа, фиксируются исходные очаги, рубцы, невусы, участки хронического повреждения, формируется базовая фотодокументация. В процессе лечения дерматоонколог наблюдает за изменением цвета, размеров и структуры опухолевых очагов, а также за характером высыпаний, сухостью, трещинами и признаками инфекции, возникающими на фоне BRAF/MEK-блокады или иммунотерапии. По результатам осмотров корректируется местная терапия кожи, решается вопрос о необходимости временного перерыва или смены системной схемы.
- Генетик интерпретирует результаты исследований на наследственные мутации и соматические изменения, влияющие на выбор протоколов лечения рака кожи. При семейных формах меланомы или множественных первичных опухолях специалист анализирует данные о мутациях CDKN2A, CDK4, BAP1 и других генов предрасположенности, обсуждает риски для пациента и родственников, формирует рекомендации по дальнейшему тестированию семьи. При соматических анализах генетик помогает клиническому онкологу правильно оценить значение мутаций BRAF, KIT, NRAS, перестроек NTRK, микросателлитной нестабильности и других маркеров, указывая, какие из них действительно открывают доступ к конкретным препаратам или клиническим исследованиям.
- Патоморфолог и молекулярный патоморфолог обеспечивают точность диагноза и детальное описание биологического профиля опухоли кожи. В классическом гистологическом заключении уточняется тип опухоли (меланома, плоскоклеточный рак, базальноклеточная карцинома, саркома кожи), степень злокачественности, глубина инвазии, состояние краёв резекции и лимфососудистое распространение. Молекулярный блок дополнительно даёт информацию о наличии мутаций BRAF, KIT, NRAS, об изменениях в генах PTCH и SMO, о перестройках NTRK и других драйверных событиях. На основании этих данных консилиум выбирает, будут ли использованы BRAF/MEK-ингибиторы, Hedgehog-блокада, трек-ингибиторы или иммунотерапия с тканенезависимым показанием.
- Иммунолог, ревматолог и эндокринолог участвуют в ведении пациента при развитии иммунных побочных эффектов на фоне применения блокаторов PD-1, PD-L1 и CTLA-4, а также при сочетании таргетных препаратов с иммунотерапией. Иммунолог и ревматолог оценивают выраженность артритов, васкулитов, аутоиммунных поражений кожи и соединительной ткани, подбирают системные и местные схемы глюкокортикоидов и других иммуносупрессоров, помогая сдержать воспаление без полного отказа от противоопухолевого лечения. Эндокринолог контролирует функцию щитовидной железы, коры надпочечников, поджелудочной железы, выявляет иммунные тиреоидиты, гипофизиты и сахарный диабет, формирует план заместительной терапии и динамического наблюдения.
- Психотерапевт оказывает онкопациенту помощь в адаптации к длительной цитогенетической терапии рака кожи, особенно при видимых изменениях внешности, хронической усталости и страхе прогрессии. На приёмах разбираются переживания, связанные с рубцами, депигментацией, вынужденными ограничениями в работе и общении, а также с результатами генетических тестов и рисками для родственников. При необходимости подбираются медикаментозные средства для коррекции тревоги и депрессивных симптомов, совместимые с онкологическими препаратами, и планируются регулярные встречи на ключевых этапах лечения.
Какие обследования назначаются
- Клинический осмотр и опрос пациента проводятся до начала цитогенетически-ориентированной терапии рака кожи, на контрольных визитах и в периоде наблюдения, при этом оценивается общее самочувствие, уровень активности, наличие болей, одышки, кашля, нарушений стула, кожного зуда и высыпаний. Осматриваются первичный очаг или рубец, регионарные лимфоузлы, кожа всего тела, слизистые оболочки, обращается внимание на изменения окраски, появление язв и уплотнений. По результатам осмотра уточняется, какие инструментальные и лабораторные исследования нужны в ближайший период и с какой частотой.
- Лабораторные анализы крови и мочи выполняют для оценки переносимости схем и своевременного выявления токсичности, связанной с таргетными препаратами и иммунотерапией. В стандартный комплекс входят общий анализ крови, биохимический профиль с контролем печёночных ферментов, креатинина, электролитов, а также общий анализ мочи для отслеживания воспалительных изменений и возможного поражения почек. На фоне лечения анализы повторяются с заранее оговорённой периодичностью и чаще при появлении жалоб, - по динамике показателей корректируются дозы лекарств, режим гидратации, потребность в дополнительной поддержке.
- ЭКГ и при необходимости УЗИ сердца используются для контроля состояния сердечно-сосудистой системы, особенно при сочетании цитогенетически-ориентированных схем с препаратами, влияющими на ритм и проводимость. Исходная запись ЭКГ фиксирует частоту и ритм, наличие ишемических изменений или нарушений проводимости, по итогам решается вопрос о базовой кардиологической поддержке. В процессе терапии исследования повторяются при появлении одышки, перебоев в работе сердца, отёков и нетипичной усталости, что позволяет своевременно менять схему лечения или направлять к кардиологу.
- Ультразвуковое исследование лимфоузлов и УЗИ органов брюшной полости применяется для оценки распространённости рака кожи и контроля метастатических очагов в динамике на фоне цитогенетической терапии. До начала лечения уточняется состояние шейных, подмышечных, паховых лимфоузлов, печени, селезёнки, при наличии подозрительных узлов измеряются размеры и исследуется их структура. В дальнейшем УЗИ выполняется по согласованному графику, либо при новых жалобах, чтобы выявлять регресс, стабилизацию или рост очагов и оценивать токсическое влияние препаратов на печень и другие органы.
- Компьютерная томография органов грудной клетки и МСКТ брюшной полости служит базовым методом визуализации при системных формах рака кожи, поскольку позволяет чётко оценить размеры и локализацию метастазов в лёгких, печени, надпочечниках и других структурах. Перед стартом терапии формируется исходное исследование, по которому рассчитываются критерии ответа, затем КТ повторяется через несколько циклов, чтобы объективно оценить эффективность цитогенетической терапии.
- Магнитно-резонансная томография головного мозга с контрастированием актуальна при меланоме и агрессивных вариантах плоскоклеточного рака, склонных к метастазированию в центральную нервную систему. Первое исследование проводится до начала системного лечения или при появлении неврологических симптомов, таких как головные боли, нарушение координации, слабость в конечностях, изменения зрения. В динамике МРТ повторяется при подозрении на новые очаги или для оценки ответа присутствующих метастазов на фоне BRAF/MEK-блокады или иммунотерапии.
- Проведение ПЭТ-КТ назначается в сложных случаях, когда требуется уточнить распространённость рака, оценить активность очагов, сомнительных по данным КТ или МРТ, либо подобрать зону для биопсии. Исследование помогает отличить рубцовые изменения после операций и лучевой терапии от жизнеспособной опухолевой ткани, выявить малые метастазы в лимфоузлах и внутренних органах. На фоне цитогенетически-ориентированной схемы ПЭТ-КТ позволяет оценить метаболический ответ, который иногда опережает изменение размеров очагов.
- Дерматоскопия и фотодокументация очагов рака кожи применяются для детального контроля местного статуса, особенно при длительной таргетной терапии и иммунотерапии. Дерматоскопия позволяет исследовать структуру сосудов, пигментного рисунка и поверхности, что позволяет точнее различать активный рост, рубцевание и воспалительные изменения. Фотофиксация с одинаковыми условиями съёмки и разметкой размеров создаёт наглядную хронологию, по которой оценивается ответ на лечение и выявляются новые подозрительные образования.
- Повторная биопсия и молекулярное профилирование метастатических очагов выполняют при прогрессии на фоне цитогенетической терапии, если возникает необходимость уточнить текущий генетический профиль опухоли. В ходе процедуры из активного очага отбирается фрагмент ткани, после чего материал повторно исследуется морфологически и молекулярно: проверяется статус BRAF, KIT, NRAS, анализируются новые мутации и аберрации. Результаты помогают понять, сохраняется ли чувствительность к прежним мишеням, появились ли дополнительные варианты для таргетных препаратов или клинических исследований.
Что важно знать пациентам
Генетические анализы перед началом онколечения
Молекулярные и генетические исследования показывают, какие механизмы роста использует опухоль, и позволяют не тратить время на схемы, к которым клеточный клон изначально нечувствителен. Если обнаружена мутация BRAF V600, открывается путь к комбинациям BRAF/MEK-ингибиторов, при изменениях в генах пути Hedgehog появляются показания к висмодегибу или сонидегибу, а при NTRK-фузиях или высокой микросателлитной нестабильности — к узконаправленным или тканенезависимым препаратам. Отсутствие анализа оставляет онколога с ограниченным набором вариантов, применение которых основывается только на клинической картине, и снижает шанс подобрать эффективную адресную терапию.
Какие побочные эффекты?
Таргетные комбинации BRAF/MEK нередко сопровождаются лихорадкой, кожными высыпаниями, болями в суставах, повышением уровня печёночных ферментов и повышенной чувствительностью к солнечному свету, а ингибиторы пути Hedgehog часто приводят к изменению вкуса, мышечным болям, потере массы тела и алопеции. Иммунотерапия способна вызывать воспаление кожи, кишечника, лёгких, эндокринных желез, что проявляется сыпью, диареей, одышкой, изменением массы тела, усталостью и лабильностью настроения. Важно не пытаться переносить тяжёлые симптомы «до планового приёма», а сразу выходить на связь с лечащей командой, поскольку своевременная коррекция токсичности позволяет продолжить эффективное лечение.
Как легче перенести онколечение, основанное на биомаркерах?
Рекомендуются простые, но систематические действия: строгое соблюдение схемы приёма препаратов, отказ от самовольного снижения доз, ведение дневника симптомов, в котором фиксируются температура, характер стула, высыпания, одышка и боли. Важно приносить на визит список всех актуальных препаратов, включая безрецептурные средства и добавки, чтобы онколог мог оценить риск взаимодействий. Соблюдение рекомендаций по защите кожи от солнца, режиму сна, питанию и физической активности помогает уменьшать выраженность усталости и кожных реакций, а честный разговор о побочных эффектах позволяет вовремя менять поддерживающие схемы.
Наследственный риск онкологии
Информация о наследственных мутациях и семейных случаях меланомы или других опухолей кожи вызывает много тревоги и нередко воспринимается как «приговор» для детей и внуков, хотя на деле речь идёт о повышенном, а не абсолютном риске. Обсуждение лучше начинать после консультации у генетика, когда получено чёткое объяснение, какие гены затронуты, каков ориентировочный риск и какие программы наблюдения реально уменьшают вероятность поздней диагностики. В разговоре с родственниками полезно акцентировать внимание не на угрозе, а на возможности заранее контролировать ситуацию: регулярные осмотры кожи, дерматоскопия, фотопротекция и, при необходимости, генетическое тестирование в рекомендованные сроки. При сильной эмоциональной нагрузке разумно подключить психолога, чтобы обсуждение наследственных вопросов не разрушало доверие в семье.















