- ДИАГНОСТИКА
- МРТ
- КТ
- КТ ГОЛОВЫ
- КТ ШЕИ
- КТ ГРУДНОЙ КЛЕТКИ
- КТ БРЮШНОЙ ПОЛОСТИ
- КТ МАЛОГО ТАЗА
- КТ ПОЗВОНОЧНИКА
- КТ СУСТАВОВ
- КТ КОСТЕЙ
- КТ АНГИОГРАФИЯ
- КТ ЗУБОВ
- УЗИ
- УЗИ ОРГАНОВ МАЛОГО ТАЗА
- УЗИ БРЮШНОЙ ПОЛОСТИ
- УЗИ ЗАБРЮШИННОГО ПРОСТРАНСТВА
- УЗИ СЕРДЦА
- УЗИ СОСУДОВ
- УЗИ МЯГКИХ ТКАНЕЙ, НЕРВОВ И ЖЕЛЕЗ
- УЗИ СУСТАВОВ
- УЗИ ГОЛОВЫ
- УЗИ ЛИМФОУЗЛОВ
- УЗИ ПРИ БЕРЕМЕННОСТИ
- УЗИ ПЛОДА
- УЗИ НОВРОЖДЕННОМУ РЕБЕНКУ
- УЗИ ПОСЛЕ АБОРТА
- РЕНТГЕН
- ВРАЧИ
- КАКОЙ ВРАЧ ЛЕЧИТ
- АКУШЕР-ГИНЕКОЛОГ
- АЛЛЕРГОЛОГ
- ВЕРТЕБРОЛОГ
- ВЕСТИБУЛОЛОГ
- ГАСТРОЭНТЕРОЛОГ
- ГЕМАТОЛОГ
- ГИНЕКОЛОГ
- ДЕРМАТОЛОГ
- ДИЕТОЛОГ
- ИГЛОТЕРАПЕВТ
- ИММУНОЛОГ
- ИНФЕКЦИОНИСТ
- КАРДИОЛОГ
- ВРАЧ ЛЕЧЕБНОЙ ФИЗКУЛЬТУРЫ
- МАММОЛОГ
- НЕВРОЛОГ
- НЕЙРОХИРУРГ
- НЕОНАТОЛОГ
- НЕФРОЛОГ
- ОНКОЛОГ
- ОНКОЛОГ-МАММОЛОГ
- ОРТОПЕД
- ОРТОПЕД-ХИРУРГ
- ОТОЛАРИНГОЛОГ
- ОФТАЛЬМОЛОГ
- ОСТЕОПАТ
- ПЕДИАТР
- ПРОКТОЛОГ
- ПСИХИАТР
- ПСИХОТЕРАПЕВТ
- ПУЛЬМОНОЛОГ
- РЕВМАТОЛОГ
- РЕФЛЕКСОТЕРАПЕВТ
- СЕКСОЛОГ
- СОМНОЛОГ
- СОСУДИСТЫЙ ХИРУРГ
- СПОРТИВНЫЙ ВРАЧ
- ТЕРАПЕВТ
- ТРАВМАТОЛОГ
- ТРИХОЛОГ
- УРОЛОГ
- ФИЗИОТЕРАПЕВТ
- ФЛЕБОЛОГ
- ФТИЗИАТР
- ВРАЧ ФУНКЦИОНАЛЬНОЙ ДИАГНОСТИКИ
- ХИРУРГ
- ЭНДОКРИНОЛОГ
- ЭНДОСКОПИСТ
- ЭПИЛЕПТОЛОГ
- СПОРТИВНЫЙ МАССАЖИСТ
- ГЕПАТОЛОГ
- ПАРАЗИТОЛОГ
- МАНУАЛЬНЫЙ ТЕРАПЕВТ
- СЕМЕЙНЫЙ ПСИХОЛОГ
- ВРАЧ ОБЩЕЙ ПРАКТИКИ
- ПРОФПАТОЛОГ-ТЕРАПЕВТ
- АНДРОЛОГ
- АНГИОЛОГ
- АРИТМОЛОГ
- АРТРОЛОГ
- БРОНХОЛОГ
- ВЕНЕРОЛОГ
- ГЕМОСТАЗИОЛОГ
- ГИРУДОТЕРАПЕВТ
- ДИАБЕТОЛОГ
- КИНЕЗИОЛОГ
- РАДИОТЕРАПЕВТ
- РЕПРОДУКТОЛОГ
- СУРДОЛОГ
- ФОНИАТР
- ХИМИОТЕРАПЕВТ
- СКИДКИ
- НА КАРТЕ
- МРТ РЯДОМ (поиск по району)
- АДМИРАЛТЕЙСКИЙ РАЙОН
- ВАСИЛЕОСТРОВСКИЙ РАЙОН
- ВЫБОРГСКИЙ РАЙОН
- КАЛИНИНСКИЙ РАЙОН
- КИРОВСКИЙ РАЙОН
- КОЛПИНСКИЙ РАЙОН
- КРАСНОГВАРДЕЙСКИЙ РАЙОН
- КРАСНОСЕЛЬСКИЙ РАЙОН
- КРОНШТАДТСКИЙ РАЙОН
- КУРОРТНЫЙ РАЙОН
- МОСКОВСКИЙ РАЙОН
- НЕВСКИЙ РАЙОН
- ПЕТРОГРАДСКИЙ РАЙОН
- ПЕТРОДВОРЦОВЫЙ РАЙОН
- ПРИМОРСКИЙ РАЙОН
- ПУШКИНСКИЙ РАЙОН
- ФРУНЗЕНСКИЙ РАЙОН
- ЦЕНТРАЛЬНЫЙ РАЙОН
- ЛЕН. ОБЛАСТЬ
- КТ и МСКТ РЯДОМ (поиск по району)
- АДМИРАЛТЕЙСКИЙ РАЙОН
- ВАСИЛЕОСТРОВСКИЙ РАЙОН
- ВЫБОРГСКИЙ РАЙОН
- КАЛИНИНСКИЙ РАЙОН
- КИРОВСКИЙ РАЙОН
- КОЛПИНСКИЙ РАЙОН
- КРАСНОГВАРДЕЙСКИЙ РАЙОН
- КРАСНОСЕЛЬСКИЙ РАЙОН
- КРОНШТАДТСКИЙ РАЙОН
- КУРОРТНЫЙ РАЙОН
- МОСКОВСКИЙ РАЙОН
- НЕВСКИЙ РАЙОН
- ПЕТРОГРАДСКИЙ РАЙОН
- ПЕТРОДВОРЦОВЫЙ РАЙОН
- ПРИМОРСКИЙ РАЙОН
- ПУШКИНСКИЙ РАЙОН
- ФРУНЗЕНСКИЙ РАЙОН
- ЦЕНТРАЛЬНЫЙ РАЙОН
- ЛЕН. ОБЛАСТЬ
- МРТ АДРЕСА БОЛЬНИЦ В СПБ
- МРТ РЯДОМ (поиск по району)
Адреса онкоцентров для лечения карциномы брюшной полости в СПБ
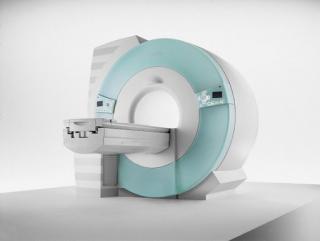
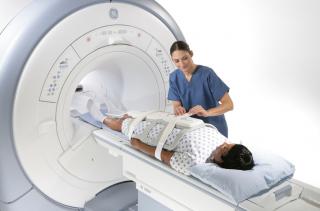
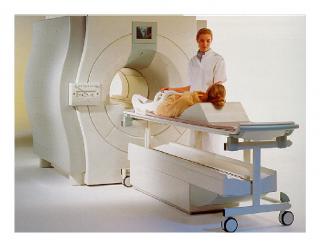
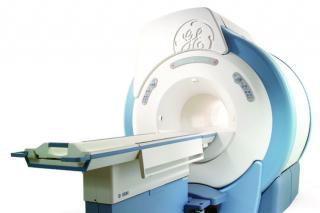
Услуга лечения онкологии
Услуга лечебного сопровождения для пациентов с онкологией — это индивидуальная комплексная помощь, которая может включать:
 Лучшиие онкологидоступ к ведущим специалистам Санкт-Петербурга, которые подберут современные схемы терапии и проконтролируют эффективность лечения на каждом этапе.
Лучшиие онкологидоступ к ведущим специалистам Санкт-Петербурга, которые подберут современные схемы терапии и проконтролируют эффективность лечения на каждом этапе. Госпитализация или дневной стационарвозможность пройти лечение в комфортных условиях ведущих онкологических центров Санкт-Петербурга.
Госпитализация или дневной стационарвозможность пройти лечение в комфортных условиях ведущих онкологических центров Санкт-Петербурга. Персональный протокол леченияразработка индивидуальной стратегии терапии с учётом типа опухоли, стадии заболевания, генетических особенностей, сопутствующих состояний и истории предыдущего лечения.
Персональный протокол леченияразработка индивидуальной стратегии терапии с учётом типа опухоли, стадии заболевания, генетических особенностей, сопутствующих состояний и истории предыдущего лечения. Второе независимое мнениеэкспертная оценка диагноза и лечебной тактики от ведущих онкологов, позволяющая подтвердить правильность выбранной стратегии, получить дополнительные варианты терапии, избежать ошибок и повысить шансы на успешный результат благодаря объективному профессиональному взгляду стороннего специалиста.
Второе независимое мнениеэкспертная оценка диагноза и лечебной тактики от ведущих онкологов, позволяющая подтвердить правильность выбранной стратегии, получить дополнительные варианты терапии, избежать ошибок и повысить шансы на успешный результат благодаря объективному профессиональному взгляду стороннего специалиста.
Лучшие специалисты в Санкт-Петербурге с рейтингом 4.5+
Последние отзывы
Что такое рак брюшной полости?
Под выражением «рак брюшной полости» понимают группу различных опухолей: аденокарциномы желудка и толстой кишки, опухоли тонкой кишки, гепатоцеллюлярную карциному и внутрипечёночную холангиокарциному, рак желчного пузыря и желчных протоков, аденокарциному поджелудочной железы, опухоли брюшины в виде перитонеального канцероматоза, псевдомиксомы брюшины и злокачественной мезотелиомы. Каждая из нозологий имеет свои пути распространения, чувствительность к операциям, химиотерапии, таргетным и иммунным препаратам, поэтому общий термин используется только для удобства, а реальное лечение всегда выстраивается под конкретный орган и морфологический вариант.
Виды онкологии брюшной полости
Рак брюшной полости в клинико-морфологическом смысле представляет собой группу злокачественных новообразований, преимущественно эпителиальных (аденокарцином и других типов карцином), исходящих из органов и анатомических структур, расположенных в абдоминальной полости, с потенциалом местной инвазии, перитонеального распространения и отдалённого метастазирования. К данной группе относят карциномы желудка и отделов толстой и тонкой кишки, при которых злокачественные клетки формируются в слизистой оболочке и по мере роста проникают через все слои стенки с выходом на серозу и брюшину, аденокарциномы поджелудочной железы с ранним поражением регионарных лимфоузлов и магистральных сосудов, первичные карциномы печени и внутрипечёночных желчных протоков, карциномы желчного пузыря и внепечёночных желчных путей с типичным распространением на печёночную паренхиму и париетальную брюшину правого подреберья. В структуру рака брюшной полости у женщин включают эпителиальные опухоли яичников, первичную перитонеальную карциному и опухоли маточных труб, которые характеризуются выраженной склонностью к перитонеальному канцероматозу и асциту, муцинозные процессы по типу псевдомиксомы брюшины, злокачественную мезотелиому брюшины, развивающуюся из мезотелиальных клеток серозной выстилки.
Отдельный вид онкопатологий составляют ретроперитонеальные и внутрибрюшные саркомы мягких тканей, формирующие крупные опухолевые конгломераты без чётких капсульных границ, а также лимфомы с преимущественной абдоминальной локализацией, при которых наблюдается массивное поражение лимфатических узлов, кишечной стенки и брыжейки. Объединяющим признаком служит первичное расположение процесса в пределах брюшинной и ретроперитонеальной областей, общие закономерности распространения по серозным листкам и лимфатическим путям, а также необходимость комплексного подхода к лечению с точной морфологической верификацией, стадированием и сочетанием хирургических, лекарственных и лучевых методов.
Виды протоколов терапии карцином брюшной полости
Тактика онколечения злокачественных новообразований зоны брюшнойп олости складывается из сочетания хирургии, системной лекарственной терапии и локальных методов. Для рака желудка и колоректального рака на локализованных стадиях опорой служат радикальные резекции с лимфодиссекцией и периоперационные схемы химиотерапии, при метастатических стадиях добавляются таргетные и иммуноонкологические препараты по результатам молекулярного анализа. Гепатоцеллюлярная карцинома и холангиокарцинома требуют сочетаний резекций, локорегионарных процедур (абляций, эмболизаций) и современных системных режимов, опухоли поджелудочной железы чаще ведут через неоадъювантные схемы с последующей резекцией, а при перитонеальном канцероматозе у отобранных пациентов возможна циторедуктивная операция с HIPEC.
При аденокарциноме желудка, включая интестинальный и диффузный варианты, основой онкотерапии служит радикальная дистальная или тотальная гастрэктомия с расширенной лимфодиссекцией, к которой добавляют периоперационные схемы на основе платиновых производных и фторпиримидинов, ориентируясь на стадии T2–T4 и поражение лимфоузлов. При раннем раке слизистой и ограниченном перстневидноклеточном варианте возможны эндоскопическая резекция слизистой или подслизистого слоя по строгим критериям. Для HER2-позитивной метастатической аденокарциномы применяют комбинации системной химиотерапии с анти-HER2-таргетной терапией, а при MSI-H или высоком уровне PD-L1 рассматривают иммунотерапевтические протоколы. GIST желудка, относящиеся к стромальным опухолям, лечат хирургическим удалением без широких лимфодиссекций и при высоком риске дополнительно назначают длительный курс иматиниба как таргетный компонент.
При аденокарциноме ободочной кишки стандартом онколечения служит сегментарная колэктомия с регионарной лимфодиссекцией и последующая адъювантная химиотерапия при стадиях III и части стадий II, для чего используют схемы на основе оксалиплатина и фторпиримидинов, а при RAS/BRAF-мутационном статусе в метастатическом процессе добавляют анти-EGFR или анти-VEGF терапию. Для аденокарциномы прямой кишки применяют неоадъювантные химиолучевые или короткие лучевые режимы с последующей тотальной мезоректумэктомией, а при полном клиническом ответе иногда реализуют стратегию тщательного наблюдения без немедленной операции. Опухоли тонкой кишки делят на аденокарциномы, GIST и нейроэндокринные новообразования: аденокарциномы лечат резекцией поражённого сегмента с лимфоузлами и системной химиотерапией, GIST — органосохраняющими резекциями с таргетной терапией иматинибом при высоком риске, нейроэндокринные опухоли — комбинацией операции, аналогов соматостатина и при необходимости PRRT-протоколов (пептид-рецепторная радионуклидная терапия).
Для онкотерапии гепатоцеллюлярной карциномы ранних стадий (по BCLC) используют анатомические или клиновидные резекции печени, а у отобранных пациентов с циррозом и ограниченными размерами узлов рассматривают трансплантацию. Слабовыраженные очаги HCC подлежат локальным методикам, таким как радиочастотная абляция или микроволновая абляция, иногда в сочетании со стереотаксическим облучением при сложной анатомии. При промежуточных стадиях онкологи назначают трансартериальные химиоэмболизации или радиоэмболизации, а при распространённом процессе — системные таргетные и иммунные режимы на основе мультикиназных ингибиторов и ингибиторов контрольных точек. Внутрипечёночная холангиокарцинома требует широких резекций с лимфодиссекцией и системной химиотерапии на основе платиновых производных, при наличии IDH- или FGFR-изменений могут дополнительно использоваться таргетные препараты. Метастатическое поражение печени при колоректальном раке часто лечат сочетанием резекций, RFA, стереотаксического облучения и системных схем FOLFOX/FOLFIRI с биологическими агентами.
При аденокарциноме желчного пузыря T1b и выше протокол онколечения основан на расширенной холецистэктомии с резекцией прилежащего печёночного сегмента и регионарной лимфодиссекцией, а при выявлении факторов высокого риска обсуждают адъювантную химиотерапию по схемам на основе гемцитабина и платиновых препаратов. Перихилярная и дистальная холангиокарцинома требует сложных резекций печёночных долей, общего печёночного протока и формирования билиодигестивных анастомозов, после чего при резекции R1 или N+ статусе рассматривают адъювантные лекарственные или химиолучевые режимы. При нерезектабельной холангиокарциноме и запущенном раке желчного пузыря ключом к онкотактике становится эндоскопическое или чрескожное дренирование желчных путей, затем по данным молекулярного профиля (FGFR2, IDH1, HER2 и другие мишени) подбирают системную химиотерапию и, при наличии соответствующих мутаций, таргетную терапию. На отдельных этапах в зону первичной опухоли может добавляться стереотаксическое или протонное облучение для усиления локального контроля.
Аденокарцинома поджелудочной железы в резектабельной стадии лечится панкреатодуоденальной резекцией или дистальной резекцией с лимфодиссекцией и обязательной адъювантной многокомпонентной химиотерапией, чаще по протоколам на основе модифицированного FOLFIRINOX или комбинации гемцитабина с капецитабином. При погранично-резектабельных и местно-распространённых формах используют неоадъювантные схемы FOLFIRINOX или гемцитабин плюс наб-паклитаксел, иногда с последующим химиолучевым этапом, после чего повторно оценивают возможность радикального вмешательства. При наличии герминальных или соматических BRCA-мутаций в метастатической аденокарциноме после ответа на схемы с платиной рассматривают поддерживающую терапию PARP-ингибиторами. Нейроэндокринные опухоли поджелудочной железы лечат в зависимости от степени злокачественности комбинацией хирургии, аналогов соматостатина, таргетных препаратов (сунитиниб, эверолимус) и PRRT-протоколов.
При перитонеальном канцероматозе, связанном с аденокарциномой желудка, колоректальным раком, серозным раком яичников или муцинозными опухолями аппендикса, у тщательно отобранных пациентов используют циторедуктивные вмешательства с максимально полным удалением видимых очагов и гипертермической внутрибрюшной химиотерапией (HIPEC) на основе препаратов, чувствительных к первичному раку. При псевдомиксомe брюшины онкопротокол также опирается на радикальную циторедукцию с HIPEC, так как основную проблему создаёт массивное слизистое наполнение, а не отдельные узлы. Злокачественная перитонеальная мезотелиома требует сочетания циторедуктивной хирургии, внутрибрюшной химиотерапии и системных схем с платиной, в отдельных случаях с добавлением иммунотерапии. Когда радикальные программы невозможны, стратегию строят вокруг системного лечения с учётом первичного очага, лапароскопических паллиативных вмешательств при кишечной непроходимости и установления постоянных дренажей для контроля рефрактерного асцита.
Помощь онкобольным
Поддержка при злокачественных опухолях желудка, кишечника, печени, желчных путей, поджелудочной железы и брюшины начинается с оценки питания и риска истощения, так как боль, тошнота, рвота, раннее насыщение, диарея или синдром мальабсорбции быстро приводят к потере массы тела. Диетолог вместе с онкологом подбирает рацион с повышенной долей белка и энергии, по возможности сохраняет питание через рот с мягкой, легкоусвояемой пищей, при выраженных нарушениях глотания или прохождения содержимого желудка и кишечника вовремя обсуждаются зондовые или гастро-/еюностомические доступы. При частой диарее корректируется структура рациона, по схеме используются вяжущие и противодиарейные средства, при запорах — мягкие слабительные и изменение режима питья, при выраженном вздутии и болевом синдроме подбираются спазмолитики и ферментные препараты.
Обезболивание строится ступенчато, с учётом висцерального, соматического и нейропатического компонентов боли, а также наличия асцита, инфильтрации брюшины и вовлечения нервных сплетений. Сначала онкопациенту назначают ненаркотические анальгетики и спазмолитики, добавляют средства для защиты слизистой желудка и профилактики запоров, затем подключают слабые опиоиды, а при усилении боли — сильные опиоидные препараты с продлённым действием, дополняя их короткодействующими формами на прорыв. При локализованном болевом очаге в печени, поджелудочной железе, костях или тазовых органах рассматриваются локальные методы: лучевая терапия, абляция, блокады чревного или других сплетений, что позволяет уменьшить системную нагрузку анальгетиками и улучшить качество жизни.
Поддержка функций печени, желчных путей и поджелудочной железы особенно актуальна при холангиокарциноме, раке желчного пузыря, метастатическом поражении печени и опухолях головки поджелудочной железы. Для контроля холестаза используются эндоскопические или чрескожные дренажи, стенты в желчные протоки, подбираются урсодезоксихолевая кислота и симптоматические средства от зуда, по биохимическим показателям решается вопрос о возможности интенсивной химиотерапии.
При экзокринной недостаточности поджелудочной железы вводят ферментные препараты с каждым приёмом пищи, что уменьшает стеаторею, вздутие и позволяет лучше усваивать калории, при нарушении углеводного обмена обсуждается коррекция сахара с участием эндокринолога. В случае асцита по результатам осмотра и УЗИ выбирается комбинация диуретиков, альбумина, при напряжённом асците — лечебный парацентез с последующей профилактикой повторного накопления жидкости.
Профилактика тромбозов, инфекций и осложнений со стороны дыхательной системы имеет большое значение, так как опухоли брюшной полости часто сопровождаются обездвиженностью, обезвоживанием и нарушением белкового обмена. При наличии факторов риска венозных тромбозов и во время активных курсов лекарственного лечения назначают антикоагулянты в профилактических или лечебных дозах, обучают распознаванию симптомов тромбоза глубоких вен и тромбоэмболии лёгочной артерии. Для снижения риска инфекций проводится санация хронических очагов, поддерживается гигиена полости рта, объясняются правила безопасной работы с центральными венозными катетерами и портами, по показаниям используется антибактериальная профилактика. Дыхательная гимнастика, ранняя активизация после операций на органах брюшной полости, контроль боли при кашле и дыхании помогают уменьшить вероятность пневмонии и ателектазов.
Реабилитация после обширных операций и комбинированного лечения рака желудка, кишечника, печени и поджелудочной железы опирается на постепенное расширение двигательной активности, восстановление навыков самообслуживания и адаптацию к изменённой анатомии пищеварительного тракта. Специалист по лечебной физкультуре подбирает безопасный комплекс упражнений с акцентом на дыхание, профилактику мышечной атрофии и тромбозов, а при наличии стомы или дренажей обучает безопасным движениям без избыточного натуживания. Медсестра по стомоуходу помогает освоить смену калоприёмников, защиту кожи вокруг стомы, подбор поясов и белья, чтобы человек мог уверенно выходить из дома и возвращаться к социальной активности. При формировании короткого кишечника или синдрома демпинга адаптация идёт через дробное питание, изменение состава блюд и использование специальных смесей.
Психологическая поддержка особенно важна при опухолях брюшины, метастатическом раке печени, поджелудочной железы, распространённых формах рака желудка и кишечника, так как прогноз часто воспринимается как угрожающий и сопровождается страхом боли, истощения и зависимости от окружающих. Психоонколог помогает осмыслить этапы лечения, преодолеть переживание утраты привычного образа жизни, снизить уровень тревоги и депрессии, а также обучает простым техникам управления дыханием и мышечным напряжением, которые можно применять дома и в стационаре. При выраженных симптомах или ограниченном прогнозе паллиативная служба координирует анальгезию, контроль тошноты, одышки, асцита, помогает принимать решения о разумных границах интенсивной терапии и сохранении достоинства на всех этапах заболевания.
Какие врачи могут быть вовлечены
- Онколог координирует общее лечение опухолей желудка, кишечника, печени, желчных путей, поджелудочной железы и брюшины, формирует последовательность линий терапии и подбирает лекарственные схемы под каждую локализацию. Учитываются стадия, морфологический вариант, молекулярный профиль, сопутствующие болезни и предыдущее лечение, на этой основе выбираются химиотерапия, таргетные и иммуноонкологические препараты, а также режимы их чередования. В динамике клинический онколог оценивает ответ по КТ, МРТ, ПЭТ, маркерам и самочувствию, принимает решения о смене протокола, переходе к паллиативной стратегии и подключении поддерживающей терапии.
- Абдоминальный хирург отвечает за радикальные и циторедуктивные вмешательства при раке желудка, толстой и тонкой кишки, печени, желчного пузыря и протоков, поджелудочной железы, а также при перитонеальном канцероматозе. На консилиуме оценивается резектабельность, объём предполагаемой резекции, необходимость расширенной лимфодиссекции, комбинированных резекций соседних органов и возможности последующей реконструкции желчных путей или желудочно-кишечного тракта. После неоадъювантных схем хирург по повторным исследованиям решает, есть ли шанс на R0-резекцию, когда целесообразна циторедукция с HIPEC и какие паллиативные вмешательства уменьшат непроходимость, боль и асцит, если радикальная цель уже недостижима.
- Онколог-радиотерапевт участвует в лечении рака прямой кишки, отдельных вариантов рака желудка, поджелудочной железы, печени, желчных путей и опухолей брюшины, когда требуется локальный контроль или обезболивание. На основе планировочной КТ и других визуализирующих методов формируется мишень: первичный очаг, ложе резекции, поражённые лимфоузлы, импланты на брюшине, при этом задаются ограничения для кишечника, печени, почек и спинного мозга. В арсенале онколога-радиотерапевта находятся радикальные химиолучевые программы, стереотаксические схемы на печень и поджелудочную железу, локальные облучения костных и мягкотканных метастазов, а также короткие паллиативные режимы для контроля боли и кровотечений.
- Интервенционный радиолог играет ключевую роль при гепатоцеллюлярной карциноме, метастазах в печени и дыхательных осложнениях при массивном асците или плеврите. С его помощью выполняются трансартериальные химиоэмболизации, радиоэмболизации, чрескожные абляции опухолевых узлов, установка порт-систем в печёночные сосуды, дренажи абсцессов и жидкостных скоплений. При опухолях желчных путей и поджелудочной железы интервенционный радиолог организует чрескожное дренирование желчных протоков и стентирование, если эндоскопический путь невозможен, что позволяет снизить уровень билирубина и продолжить системное лечение.
- Гастроэнтеролог и эндоскопист особенно важны при опухолях желудка, тонкой и толстой кишки, перитонеальном поражении, сопровождающемся изменениями стула и синдромом мальабсорбции. Эндоскопист выполняет диагностические и лечебные вмешательства: биопсии, эндоскопические резекции раннего рака, стентирование при стенозах пищевода, желудка, двенадцатиперстной кишки и толстой кишки, расширения стриктур. Гастроэнтеролог занимается коррекцией диареи, запоров, метеоризма, подбирает ферментную терапию при панкреатической недостаточности, схемы противорефлюксной и противоязвенной терапии, что повышает переносимость химиотерапии, таргетных препаратов и больших резекций.
- Патоморфолог определяет тип опухоли для каждой локализации: аденокарцинома желудка, колоректальный рак, гепатоцеллюлярная карцинома, холангиокарцинома, аденокарцинома поджелудочной железы, GIST, нейроэндокринные и редкие новообразования, а также степень злокачественности и статус краёв резекции. Дополнительно выполняются иммуногистохимические и молекулярные исследования на HER2, RAS, BRAF, MSI, BRCA, FGFR, IDH и другие маркёры, которые открывают доступ к таргетным и иммуноонкологическим схемам. На повторных операционных материалах патоморфолог оценивает степень лечебного патоморфоза после неоадъювантных протоколов, что влияет на дальнейшую тактику.
- Анестезиолог-реаниматолог участвует во всех этапах крупных абдоминальных вмешательств, интервенционных процедур и интенсивной лекарственной терапии у пациентов с тяжёлым соматическим фоном. Перед операциями на желудке, кишечнике, печени, поджелудочной железе и при циторедукции с HIPEC оцениваются резерв сердечно-сосудистой и дыхательной систем, функция печени и почек, риск осложнений по шкалам, формируется план интраоперационного мониторинга и послеоперационного наблюдения. При развитии полиорганной недостаточности, тяжёлых инфекций, кровотечений и тромбоэмболических осложнений именно анестезиолог-реаниматолог обеспечивает стабилизацию, от которой зависит возможность продолжения онкологического лечения.
- Диетолог и специалист по нутритивной поддержке незаменимы при раке желудка, тонкой и толстой кишки, поджелудочной железы, при перитонеальном канцероматозе и массивном поражении печени. На основании исходного индекса массы тела, лабораторных показателей и реального объёма съедаемой пищи формируется план питания с учётом консистенции, калорийности и содержания белка.
- Психоонколог и паллиативная команда сопровождают пациентов с опухолями брюшной полости на всех стадиях, от момента постановки диагноза до поздних этапов заболевания. Психоонколог помогает справиться со страхом боли, операций, стом, асцита, потерей контроля над собственным телом и зависимостью от близких, обучает техникам снижения тревоги и работы с бессонницей.
Какие обследования назначаются
- Лабораторные анализы крови при опухолях брюшной полости назначаются с учётом локализации и плана лечения, чтобы заранее понять резерв костного мозга и функцию жизненно важных органов. В стандартный набор входят общий анализ, биохимический профиль с оценкой билирубина, трансаминаз, щелочной фосфатазы, креатинина, мочевины, электролитов, при необходимости расширяют панель с учётом риска цитолиза или холестаза. Дополнительно проводят исследование на онкомаркеры: альфа-фетопротеин при гепатоцеллюлярной карциноме, СА 19-9 при раке поджелудочной железы и желчных путей, СЕА и иногда СА 19-9 при колоректальном раке, динамику значений сопоставляют с данными визуализирующих методов и клинической картиной.
- Общий анализ мочи позволяет оценить, как организм переносит лекарственную нагрузку, контрастные исследования и обезвоживание на фоне рвоты, диареи или асцита. По уровню белка, эритроцитов, лейкоцитов и цилиндров ориентируются в состоянии клубочкового аппарата и мочевыводящих путей, фиксируют исходную картину до старта протокола. При появлении отёков, уменьшении объёма мочи, дискомфорта в пояснице и лихорадки анализ повторяют, результаты используют для изменения объёма инфузий, подбора диуретиков и приостановки потенциально нефротоксичных препаратов.
- ЭКГ и при необходимости эхокардиография относятся к обязательным этапам подготовки перед большими операциями на желудке, кишечнике, печени, поджелудочной железе и при назначении интенсивной химио- или таргетной терапии. По ЭКГ оценивают ритм, признаки ишемии, проводимость, по ЭхоКГ получают представление о фракции выброса и состоянии клапанов, что позволяет анестезиологу и онкологу согласовать объём вмешательства и допустимую нагрузку. В дальнейшем при жалобах на одышку, боли за грудиной, резкое падение переносимости нагрузки кардиологическое обследование повторяют, чтобы вовремя скорректировать лечение и не списывать все симптомы на «усталость от химиотерапии».
- Ультразвуковое исследование органов брюшной полости проводится при подозрении на опухоли печени, желчного пузыря, желчных протоков, поджелудочной железы и перитонеальный канцероматоз. На УЗИ оценивают размеры печени, структуру паренхимы, наличие очагов, диаметр внутрипечёночных и внепечёночных протоков, состояние желчного пузыря, контуры поджелудочной железы, объём свободной жидкости в брюшной полости. В процессе лечения ультразвуковой метод визуализации удобен для динамического контроля: по нему отслеживают, как меняется уровень холестаза после стентирования, уменьшается ли асцит на фоне диуретиков и паллиативных вмешательств, появляются ли новые очаги.
- Компьютерная томография с внутривенным контрастированием служит основным инструментом стадирования при раке желудка, толстой и тонкой кишки, печени, поджелудочной железы, желчных путей и опухолях брюшины. Серия аксиальных и реконструированных срезов даёт чёткое представление о толщине стенки полых органов, объёме первичной массы, прорастании в соседние структуры, состоянии лимфоузлов, наличии метастазов в печени, лёгких, брюшине. Сравнение исходных и последующих МСКТ позволяет объективно оценить эффект от системной терапии, решить, готов ли пациент к резекции, HIPEC, локальной абляции либо требуется смена лекарственной линии.
- Магнитно-резонансная томография органов брюшной полости с контрастом с прицелом на печень и поджелудочную железу используется, если требуется более детальная характеристика очагов и сосудистых отношений, чем может дать КТ. При гепатоцеллюлярной карциноме МРТ с контрастом специфических для печени препаратов помогает различать регенераторные узлы, доброкачественные образования и истинные опухолевые очаги, а также оценивает вовлечение воротной и печёночных вен. При опухолях поджелудочной железы и дистальной части общего желчного протока МРТ с MRCP уточняет уровень и протяжённость стриктур, степень контакта с магистральными сосудами, что напрямую влияет на резектабельность и планирование хирургической тактики.
- ПЭТ-КТ с фтордезоксиглюкозой или другими радиофармпрепаратами рассматривается при неясной картине по КТ и МРТ, при подозрении на скрытый перитонеальный канцероматоз или отдалённые метастазы небольшого размера. Исследование выявляет метаболически активные очаги в лимфоузлах, печени, костях, брюшине, помогает отличить фиброзные изменения после операций и облучения от жизнеспособной опухоли. В ходе лечения ПЭТ-КТ используют для оценки глубины ответа при системной терапии и перед повторными хирургическими вмешательствами или стереотаксическим облучением, чтобы не подвергать пациента неоправданному риску.
- Эзофагогастродуоденоскопия и колоноскопия необходимы при раке желудка, двенадцатиперстной кишки, толстой и терминального отдела подвздошной кишки как на этапе диагностики, так и в наблюдении после операций и комбинированного лечения. Эндоскопия позволяет осмотреть слизистую зоны анастомоза или резекции, выявить ранние признаки местного рецидива, кровоточащие участки, воспалительные изменения, прицельно взять биопсии. При стенозах просвета используют дилатации, стентирование, иногда эндоскопическое удаление ограниченных рецидивов, что помогает отсрочить или избежать тяжёлых паллиативных операций и улучшить питание.
- Эндоскопическое ультразвуковое исследование брюшной полости имеет особое значение при раке поджелудочной железы, дистальной холангиокарциноме, опухолях желудка и прямой кишки, когда требуется оценить глубину прорастания и состояние регионарных лимфоузлов. Высокочастотный датчик, расположенный в непосредственной близости от опухоли, визуализирует слои стенки органа, границы инфильтрации, расстояние до сосудистых структур, размеры и характер ближайших узлов. Во время процедуры выполняют тонкоигольную аспирационную биопсию подозрительных зон, материал используют для уточнения морфологии и молекулярного профиля, что важно для подбора таргетных и иммуноонкологических схем.
- Эндоскопическая ретроградная холангиопанкреатография нужна при механической желтухе, вызванной опухолями желчного пузыря, терминального отдела общего желчного протока, ампулярной зоны или головки поджелудочной железы. Во время вмешательства контрастом заполняют желчные и панкреатические протоки, получают информацию об уровне и протяжённости сужения, берут материал для цитологии. Через те же доступы устанавливают пластиковые или металлические стенты, восстанавливая отток желчи, снижая уровень билирубина и позволяя безопаснее проводить системное лечение.
- Диагностическая лапароскопия применяется при раке желудка, поджелудочной железы, колоректальном раке и подозрении на перитонеальное поражение, когда не удаётся однозначно оценить картину по данным КТ и МРТ. Через небольшие разрезы осматривают диафрагмальные купола, печёночную поверхность, петли кишечника, тазовую брюшину, выявляют мелкие импланты, невидимые на стандартных снимках, берут биопсии и образцы асцитической жидкости для цитологического анализа. Полученная информация помогает корректно стадировать процесс, определить оправданность циторедуктивной операции и HIPEC либо отказаться от агрессивного хирургического подхода в пользу системной и паллиативной терапии.
Что важно знать пациентам
Комплексное обследование при раке брюшной полости
Опухолевые очаги в печени, брюшине, лимфоузлах и полых органах могут быстро менять размеры, структуру и количество на фоне терапии, поэтому КТ, МРТ, ПЭТ-КТ, УЗИ и эндоскопия нужны не «для галочки», а для регулярного уточнения реальной картины. По результатам визуализирующих и лабораторных исследований команда решает, возможна ли резекция или циторедукция с HIPEC, есть ли смысл в локальных абляциях, стоит ли продолжать текущую схему или пришло время сменить линию лечения. Пересмотр тактики на консилиуме после очередного обследования является нормальной частью маршрута, а не признаком хаотичности.
Какие осложнения?
Требуют немедленной оценки внезапная интенсивная боль в животе с напряжением мышц, резкая слабость, падение артериального давления, холодный пот, что может говорить о кровотечении или перфорации полого органа. Поводом для срочного осмотра становится стойкая рвота с невозможностью пить, отсутствие газа и стула на фоне вздутого болезненного живота, быстрый рост асцита, внезапное пожелтение кожи и склер, потемнение мочи. Опасными признаками также считаются остро возникшая одышка, боль в груди, односторонний отёк ноги, сильная новая боль в спине или тазу, которая мешает ходить и вставать.
Как легче перенести онкотерапию?
Онкопациенту рекомендуется строгое соблюдение схем приёма лекарств, ведение простого дневника веса, температуры, стула, боли и других симптомов, а также готовность обсуждать любые изменения с лечащей командой, не скрывая трудных тем. Очень важны питание с достаточным количеством белка и энергии, контроль питьевого режима, посильная ежедневная активность, использование рекомендованных средств реабилитации и стомоухода, если они нужны. Близкие могут взять на себя организацию поездок, помощь с документами, оформление технических средств и паллиативной поддержки, а главное — участие в обсуждении решений, чтобы у человека с опухолью брюшной полости сохранялось ощущение опоры и совместного управления ситуацией.