- ДИАГНОСТИКА
- МРТ
- КТ
- КТ ГОЛОВЫ
- КТ ШЕИ
- КТ ГРУДНОЙ КЛЕТКИ
- КТ БРЮШНОЙ ПОЛОСТИ
- КТ МАЛОГО ТАЗА
- КТ ПОЗВОНОЧНИКА
- КТ СУСТАВОВ
- КТ КОСТЕЙ
- КТ АНГИОГРАФИЯ
- КТ ЗУБОВ
- УЗИ
- УЗИ ОРГАНОВ МАЛОГО ТАЗА
- УЗИ БРЮШНОЙ ПОЛОСТИ
- УЗИ ЗАБРЮШИННОГО ПРОСТРАНСТВА
- УЗИ СЕРДЦА
- УЗИ СОСУДОВ
- УЗИ МЯГКИХ ТКАНЕЙ, НЕРВОВ И ЖЕЛЕЗ
- УЗИ СУСТАВОВ
- УЗИ ГОЛОВЫ
- УЗИ ЛИМФОУЗЛОВ
- УЗИ ПРИ БЕРЕМЕННОСТИ
- УЗИ ПЛОДА
- УЗИ НОВРОЖДЕННОМУ РЕБЕНКУ
- УЗИ ПОСЛЕ АБОРТА
- РЕНТГЕН
- ВРАЧИ
- КАКОЙ ВРАЧ ЛЕЧИТ
- АКУШЕР-ГИНЕКОЛОГ
- АЛЛЕРГОЛОГ
- ВЕРТЕБРОЛОГ
- ВЕСТИБУЛОЛОГ
- ГАСТРОЭНТЕРОЛОГ
- ГЕМАТОЛОГ
- ГИНЕКОЛОГ
- ДЕРМАТОЛОГ
- ДИЕТОЛОГ
- ИГЛОТЕРАПЕВТ
- ИММУНОЛОГ
- ИНФЕКЦИОНИСТ
- КАРДИОЛОГ
- ВРАЧ ЛЕЧЕБНОЙ ФИЗКУЛЬТУРЫ
- МАММОЛОГ
- НЕВРОЛОГ
- НЕЙРОХИРУРГ
- НЕОНАТОЛОГ
- НЕФРОЛОГ
- ОНКОЛОГ
- ОНКОЛОГ-МАММОЛОГ
- ОРТОПЕД
- ОРТОПЕД-ХИРУРГ
- ОТОЛАРИНГОЛОГ
- ОФТАЛЬМОЛОГ
- ОСТЕОПАТ
- ПЕДИАТР
- ПРОКТОЛОГ
- ПСИХИАТР
- ПСИХОТЕРАПЕВТ
- ПУЛЬМОНОЛОГ
- РЕВМАТОЛОГ
- РЕФЛЕКСОТЕРАПЕВТ
- СЕКСОЛОГ
- СОМНОЛОГ
- СОСУДИСТЫЙ ХИРУРГ
- СПОРТИВНЫЙ ВРАЧ
- ТЕРАПЕВТ
- ТРАВМАТОЛОГ
- ТРИХОЛОГ
- УРОЛОГ
- ФИЗИОТЕРАПЕВТ
- ФЛЕБОЛОГ
- ФТИЗИАТР
- ВРАЧ ФУНКЦИОНАЛЬНОЙ ДИАГНОСТИКИ
- ХИРУРГ
- ЭНДОКРИНОЛОГ
- ЭНДОСКОПИСТ
- ЭПИЛЕПТОЛОГ
- СПОРТИВНЫЙ МАССАЖИСТ
- ГЕПАТОЛОГ
- ПАРАЗИТОЛОГ
- МАНУАЛЬНЫЙ ТЕРАПЕВТ
- СЕМЕЙНЫЙ ПСИХОЛОГ
- ВРАЧ ОБЩЕЙ ПРАКТИКИ
- ПРОФПАТОЛОГ-ТЕРАПЕВТ
- АНДРОЛОГ
- АНГИОЛОГ
- АРИТМОЛОГ
- АРТРОЛОГ
- БРОНХОЛОГ
- ВЕНЕРОЛОГ
- ГЕМОСТАЗИОЛОГ
- ГИРУДОТЕРАПЕВТ
- ДИАБЕТОЛОГ
- КИНЕЗИОЛОГ
- РАДИОТЕРАПЕВТ
- РЕПРОДУКТОЛОГ
- СУРДОЛОГ
- ФОНИАТР
- ХИМИОТЕРАПЕВТ
- СКИДКИ
- НА КАРТЕ
- МРТ РЯДОМ (поиск по району)
- АДМИРАЛТЕЙСКИЙ РАЙОН
- ВАСИЛЕОСТРОВСКИЙ РАЙОН
- ВЫБОРГСКИЙ РАЙОН
- КАЛИНИНСКИЙ РАЙОН
- КИРОВСКИЙ РАЙОН
- КОЛПИНСКИЙ РАЙОН
- КРАСНОГВАРДЕЙСКИЙ РАЙОН
- КРАСНОСЕЛЬСКИЙ РАЙОН
- КРОНШТАДТСКИЙ РАЙОН
- КУРОРТНЫЙ РАЙОН
- МОСКОВСКИЙ РАЙОН
- НЕВСКИЙ РАЙОН
- ПЕТРОГРАДСКИЙ РАЙОН
- ПЕТРОДВОРЦОВЫЙ РАЙОН
- ПРИМОРСКИЙ РАЙОН
- ПУШКИНСКИЙ РАЙОН
- ФРУНЗЕНСКИЙ РАЙОН
- ЦЕНТРАЛЬНЫЙ РАЙОН
- ЛЕН. ОБЛАСТЬ
- КТ и МСКТ РЯДОМ (поиск по району)
- АДМИРАЛТЕЙСКИЙ РАЙОН
- ВАСИЛЕОСТРОВСКИЙ РАЙОН
- ВЫБОРГСКИЙ РАЙОН
- КАЛИНИНСКИЙ РАЙОН
- КИРОВСКИЙ РАЙОН
- КОЛПИНСКИЙ РАЙОН
- КРАСНОГВАРДЕЙСКИЙ РАЙОН
- КРАСНОСЕЛЬСКИЙ РАЙОН
- КРОНШТАДТСКИЙ РАЙОН
- КУРОРТНЫЙ РАЙОН
- МОСКОВСКИЙ РАЙОН
- НЕВСКИЙ РАЙОН
- ПЕТРОГРАДСКИЙ РАЙОН
- ПЕТРОДВОРЦОВЫЙ РАЙОН
- ПРИМОРСКИЙ РАЙОН
- ПУШКИНСКИЙ РАЙОН
- ФРУНЗЕНСКИЙ РАЙОН
- ЦЕНТРАЛЬНЫЙ РАЙОН
- ЛЕН. ОБЛАСТЬ
- МРТ АДРЕСА БОЛЬНИЦ В СПБ
- МРТ РЯДОМ (поиск по району)
Адреса и стоимость РЧА рака печени в СПБ
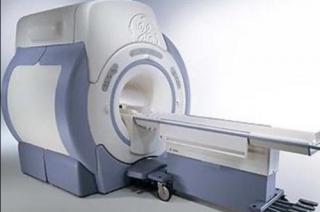
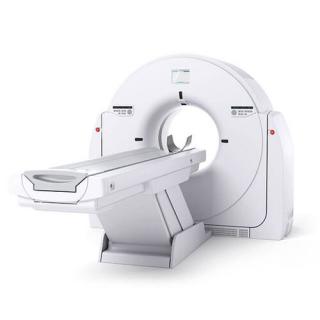
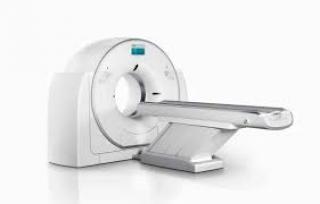
Услуга лечения онкологии
Услуга лечебного сопровождения для пациентов с онкологией — это индивидуальная комплексная помощь, которая может включать:
 Лучшиие онкологидоступ к ведущим специалистам Санкт-Петербурга, которые подберут современные схемы терапии и проконтролируют эффективность лечения на каждом этапе.
Лучшиие онкологидоступ к ведущим специалистам Санкт-Петербурга, которые подберут современные схемы терапии и проконтролируют эффективность лечения на каждом этапе. Госпитализация или дневной стационарвозможность пройти лечение в комфортных условиях ведущих онкологических центров Санкт-Петербурга.
Госпитализация или дневной стационарвозможность пройти лечение в комфортных условиях ведущих онкологических центров Санкт-Петербурга. Персональный протокол леченияразработка индивидуальной стратегии терапии с учётом типа опухоли, стадии заболевания, генетических особенностей, сопутствующих состояний и истории предыдущего лечения.
Персональный протокол леченияразработка индивидуальной стратегии терапии с учётом типа опухоли, стадии заболевания, генетических особенностей, сопутствующих состояний и истории предыдущего лечения. Второе независимое мнениеэкспертная оценка диагноза и лечебной тактики от ведущих онкологов, позволяющая подтвердить правильность выбранной стратегии, получить дополнительные варианты терапии, избежать ошибок и повысить шансы на успешный результат благодаря объективному профессиональному взгляду стороннего специалиста.
Второе независимое мнениеэкспертная оценка диагноза и лечебной тактики от ведущих онкологов, позволяющая подтвердить правильность выбранной стратегии, получить дополнительные варианты терапии, избежать ошибок и повысить шансы на успешный результат благодаря объективному профессиональному взгляду стороннего специалиста.
Лучшие специалисты в Санкт-Петербурге с рейтингом 4.5+
Последние отзывы
Что такое радиочастотная абляция рака печени?
Радиочастотная абляция при раке печени представляет собой метод локального лечения, при котором в опухолевый узел через кожу или во время малоинвазивной операции вводят специальный электрод, по нему подают высокочастотный ток, вокруг кончика создаётся зона повышенной температуры, клетки опухоли теряют жизнеспособность, образуется участок коагуляционного некроза, а окружающая паренхима повреждается в значительно меньшей степени, чем при открытой резекции.
Показания
РЧА обычно рассматривается у пациентов с ограниченным числом очагов небольшого диаметра, расположенных на безопасном расстоянии от крупных сосудов и главных желчных протоков, при удовлетворительном функциональном резерве печени и отсутствии массивного внепечёночного поражения, при крупных множественных узлах, грубом портальном тромбозе или декомпенсированном циррозе эффективность локального нагрева резко снижается, риск осложнений возрастает, поэтому в подобных случаях обсуждаются другие варианты, включая системное лечение, резекцию, трансплантацию или чисто симптоматическую терапию.
Способы радиочастотной абляции рака печени
Чрескожная радиочастотная абляция небольшого очага гепатоцеллюлярного рака рассматривается при одиночном узле примерно до 3 см в диаметре на фоне удовлетворительного функционального резерва печени и отсутствия выраженного портального тромбоза, по данным контрастной КТ или контрастной МРТ уточняется сегмент, глубина залегания и расстояние до капсулы, желчных протоков и крупных сосудов, под ультразвуковым или томографическим контролем игольчатый электрод устанавливают в центр узла и задают режим мощности и экспозиции так, чтобы зона термического некроза охватила опухолевую ткань с равномерным защитным полем по периферии.
РЧА очагов среднего размера с использованием последовательных перекрывающихся абляций применяется при узлах 3–5 см, когда одной сферой нагрева невозможно покрыть весь объём, на предварительном этапе по трёхмерной реконструкции строится схема размещения электродных позиций, интервенционный радиолог поэтапно смещает активную зону внутри опухоли, формируя несколько частично накладывающихся очагов коагуляционного некроза, задача заключается в том, чтобы не оставить внутренних «островков» жизнеспособной ткани и одновременно не выйти термическим воздействием за безопасный контур по отношению к сосудам и протокам.
Лапароскопическая радиочастотная абляция применяется при субдиафрагмальном расположении узла, при экранировании очага кишечными петлями или при выраженном метеоризме, затрудняющем чрескожную навигацию, в операционной создаётся пневмоперитонеум, устанавливаются троакары, с помощью лапароскопа и контактного ультразвукового датчика уточняется топография сегментов печени, через отдельный порт вводится радиочастотный электрод, который погружают в центр очага под визуальным и ультразвуковым контролем, абляция выполняется до достижения заданной температуры и объёма некроза, одновременно осматривается диафрагма и поверхностные сосуды.
Интраоперационная радиочастотная деструкция во время резекции печени используется при сочетании крупных резектабельных узлов с небольшими глубинными очагами, хирург после мобилизации печени и выделения сосудистой ножки резецирует основной массив опухолевой ткани, а затем совместно с интервенционным специалистом по данным интраоперационного ультразвука выявляет дополнительные мелкие очаги и обрабатывает их электродом, при этом формируются локальные зоны некроза на фоне контролируемого кровотока, проводится тщательный визуальный контроль гемостаза и герметичности желчных путей.
Комбинированные схемы ТАХЭ плюс РЧА применяют при промежуточной стадии гепатоцеллюлярного рака, когда опухоль питается за счёт развитой артериальной сети и частично выходит за размеры, оптимальные для одной только абляции, сначала интервенционный рентгенолог выполняет селективную химиоэмболизацию питающих ветвей печёночной артерии с введением эмболизирующего материала и химиопрепарата, что уменьшает кровоток в узле и усиливает терапевтическое воздействие, затем через несколько недель осуществляется РЧА уже ишемизированного очага, в результате формируется более полный некроз с меньшим эффектом теплового «отмывания».
Радиочастотная термоабляция метастатических очагов в печени при раке толстой кишки и других солидных опухолях рассматривается при ограниченном количестве и размере узлов на фоне контролируемого первичного процесса, по данным КТ и ПЭТ-КТ формируется карта локализации метастазов, оценивается расстояние до сосудистых структур и жёлчных протоков, при экранирующих кишечных петлях планируется гидродиссекция или лапароскопический доступ, каждый очаг обрабатывается электродом так, чтобы зона некроза перекрывала границы метастатического узла, а совокупный объём абляции не приводил к значимому снижению функции печени.
РЧА рецидивных очагов по краю резекции или в трансплантированной печени используется при повторном локальном появлении небольших узлов без массивного системного прогрессирования, перед вмешательством сопоставляются старые и новые томографические данные, анализируется состояние сосудистых анастомозов и желчных реконструкций, выбираются максимально щадящие траектории доступа, абляция выполняется в более мягком режиме с постоянным контролем температурных параметров, после формирования некроза выполняется тщательная визуализация области вмешательства для раннего выявления возможных осложнений.
Помощь онкобольным
Предоперационное лечение направлено на стабилизацию функции печени и уменьшение риска декомпенсации после абляции, гепатолог и онколог совместно оценивают класс по Чайлд–Пью, наличие асцита, эпизодов энцефалопатии и варикозного синдрома, при необходимости назначаются диуретики в индивидуально подобранной дозе, препараты, снижающие аммиак, бета-блокаторы при выраженной портальной гипертензии, проводится коррекция питания с ограничением соли и алкоголя, выполняется противовирусная терапия при активных гепатитах по показаниям, только после стабилизации параметров принимается окончательное решение о дате РЧА и объёме планируемого воздействия.
Анестезиологическая и инфузионная поддержка во время РЧА включает подбор обезболивания, мониторинг гемодинамики и объёма циркулирующей крови, при чрескожной абляции чаще используют внутривенную седацию с контролируемым введением анальгетиков и седативных средств, при лапароскопических и комбинированных процедурах применяется эндотрахеальный наркоз, во время вмешательства поддерживается стабильное артериальное давление и адекватная оксигенация, ориентируясь на возраст, сопутствующую кардиологическую патологию и выраженность портальной гипертензии, инфузионная терапия строится так, чтобы избежать как гипергидратации, усиливающей риск кровотечений и отёка, так и гиповолемии.
Коррекция нарушений свёртывания и профилактика кровотечений включают оценку тромбоцитарного звена, протромбинового времени, МНО и фибриногена, при низком уровне тромбоцитов заранее планируется переливание тромбоконцентрата, при гипокоагуляции используется свежезамороженная плазма и концентраты факторов, приём антикоагулянтов и антиагрегантов по возможности временно прекращается или переводится на короткодействующие формы, после РЧА дополнительно контролируется уровень гемоглобина и состояние брюшной полости по ультразвуку, при признаках гематомы или продолжающейся кровопотери выполняется КТ и решается вопрос о повторном гемостазе или эмболизации.
Антибактериальное лечение носит профилактический и лечебный характер, особенно у пациентов с билиарными стентами, анастомозами или перенесёнными эпизодами холангита, перед вмешательством анализируется общий анализ крови и биохимические показатели, при подозрении на инфекцию жёлчных путей или очаги в других органах проводится предварительный курс антибактериальных препаратов, в день РЧА вводится однократная доза антибиотика широкого спектра, после абляции контролируются температура, лейкоцитарная формула и уровни С-реактивного белка, при признаках абсцедирования по данным КТ назначается расширенная антибактериальная схема и выполняется чрескожное дренирование.
Гепатопротективная и метаболическая поддержка в послеабляционном периоде направлена на ограничение лекарственного повреждения печени и поддержание белково-энергетического баланса, после РЧА контролируются трансаминазы, билирубин, щёлочная фосфатаза, альбумин и аммиак, при их кратковременном умеренном повышении достаточно щадящей диеты, адекватного питьевого режима и ограничения потенциально гепатотоксичных лекарств, при более выраженном ухудшении показателей используются инфузионные растворы, препараты альбумина, витамины группы B, средства, нормализующие жёлчный отток, при угрозе энцефалопатии корректируется белковый компонент питания и усиливается терапия, снижающая аммиак.
Лечение постабляционного синдрома и обезболивание включают использование ненаркотических анальгетиков, спазмолитиков и противовоспалительных средств, у многих пациентов в первые двое суток отмечаются субфебрильная температура, слабость и умеренная боль в правом подреберье, врач ориентирует, что подобное состояние связано с резорбцией некротической ткани и обычно носит ограниченный характер, при повышении температуры выше определённого порога или усилении болевого синдрома проводится углублённая оценка на предмет инфекционных осложнений, при необходимости терапия усиливается, добавляются противорвотные препараты и корректируется инфузионный режим для профилактики дегидратации.
Профилактика тромбоэмболических осложнений и реабилитация после РЧА учитывают сочетание онкологического статуса, возможной временной иммобилизации и изменения коагуляции, при отсутствии высокого риска кровотечения назначаются низкомолекулярные гепарины в профилактических дозах, эластические бинты или чулки на нижние конечности, по мере восстановления сознания и стабильности гемодинамики пациент активизируется, рекомендуется ранний подъём, ходьба по палате и простые упражнения для ног, в дальнейшем делается акцент на постепенное расширение бытовой активности при сохранении ограничений по подъёму тяжестей и интенсивным видам спорта в оговорённый срок.
Онкологическая стратегия наблюдения и при необходимости системной терапии после РЧА строится с учётом типа процесса, биологии опухоли и объёма остаточного поражения, при гепатоцеллюлярном раке в ближайшие месяцы выполняются КТ или МРТ с контрастированием для оценки зоны абляции и поиска новых очагов, контролируется уровень альфа-фетопротеина, при метастатическом поражении печени параллельно проводится или возобновляется системное лечение, которое дополняет локальный метод, при появлении новых небольших узлов рассматривается повторная РЧА, резекция или другие локальные варианты, последовательность этапов обсуждается на мультидисциплинарном консилиуме, чтобы сохранить как противоопухолевый контроль, так и функцию органа.
Какие врачи могут быть вовлечены
- Интервенционный радиолог является основным специалистом, выполняющим РЧА, по результатам мультифазной КТ и МРТ с контрастированием оценивает размеры, количество и расположение очагов, анализирует расстояние до воротной вены, печёночных вен, желчных протоков и диафрагмы, выбирает оптимальный доступ через кожу или лапароскопический подход, планирует траекторию иглы, во время манипуляции под контролем ультразвука или КТ позиционирует электроды в опухолевой ткани, задаёт режим мощности и длительность экспозиции, добивается формирования полноценной зоны коагуляционного некроза и по завершении вмешательства оценивает состояние пункционного канала и паренхимы.
- Гепатобилиарный хирург включается при комбинированных операциях, когда резекция печени сочетается с РЧА небольших или глубоко расположенных узлов, по предоперационным данным решает, какие сегменты лучше удалить, а какие очаги допустимо обработать абляцией, во время лапаротомии или лапароскопии ориентируется по интраоперационному УЗИ, выполняет резекционный этап с сохранением максимального объёма функционирующей ткани и совместно с интервенционным радиологом обрабатывает остаточные узлы электродом, при этом контролирует гемостаз, герметичность желчных путей и необходимость установки дренажей.
- Онколог формирует общую стратегию лечения, оценивает стадию рака печени, наличие внепечёночных метастазов, класс по Чайлд–Пью и сопутствующие заболевания, определяет, используется ли РЧА как самостоятельный локальный метод, как дополнение к трансартериальной химиоэмболизации, системной терапии, трансплантации или резекции, подбирает лекарственные режимы до и после локального вмешательства, организует наблюдение с контрольной визуализацией и при признаках прогрессирования пересматривает последовательность этапов.
- Гепатолог отвечает за оценку хронического поражения печени и подготовку к РЧА, по данным биохимических анализов, коагулограммы, ультразвука с оценкой портального кровотока и при необходимости эндоскопии верхних отделов желудочно-кишечного тракта определяет выраженность портальной гипертензии, асцита и риска кровотечений из варикозно-расширенных вен, корректирует диуретическую терапию, питание и лечение вирусного гепатита, после абляции следит за показателями цитолиза, холестаза и синтетической функции печени, решает вопрос о возможности повторных локальных вмешательств.
- Анестезиолог-реаниматолог оценивает анестезиологический риск, изучает кардиологический и дыхательный статус, анализирует данные ЭКГ, эхокардиографии, функции внешнего дыхания, решения консилиума по антикоагулянтной терапии, выбирает формат обезболивания от седации с контролем сознания при чрескожной РЧА до полноценного эндотрахеального наркоза при лапароскопическом доступе, во время процедуры обеспечивает стабильность гемодинамики, адекватную вентиляцию и контроль болевых импульсов, а в раннем послеоперационном периоде организует мониторинг и коррекцию жизненно важных параметров.
- Патоморфолог исследует биопсийный или операционный материал, подтверждает гепатоцеллюлярный рак, холангиокарциному или метастатическое поражение печени, определяет степень дифференцировки, наличие сосудистой и периневральной инвазии, при метастазах уточняет первичный источник по иммуногистохимическим маркёрам, даёт заключение о радикальности выполненного вмешательства при резекции, при сомнительных очагах после РЧА по данным последующих биопсий помогает отличить остаточный активный опухолевый компонент от фиброзного или некротического участка.
Какие обследования назначаются
- Общие обследования перед радиочастотной деструкции включают клинический анализ крови с оценкой уровня гемоглобина, лейкоцитов с формулой и тромбоцитов, развёрнутый биохимический профиль с обязательным определением билирубина, аспартат- и аланинаминотрансферазы, щелочной фосфатазы, гамма-глутамилтранспептидазы, альбумина, креатинина, мочевины, электролитов и глюкозы, коагулограмму с расчётом международного нормализованного отношения и оценки фибриногена, общий анализ мочи, стандартную электрокардиографию и при наличии сердечно-сосудистых заболеваний эхокардиографию, по совокупности этих данных определяется функциональный резерв печени, риск кровотечений, выраженность сопутствующей патологии и необходимость предварительной коррекции.
- Визуализирующие методики включают мультифазную КТ печени с контрастированием в артериальную, портальную и позднюю фазы, которая позволяет увидеть типичное артериальное накопление и портальное вымывание при гепатоцеллюлярном раке, оценить количество, размеры и сегментарное расположение очагов, отношение узлов к воротной вене, печёночным венам, жёлчным структурам и диафрагме, аналогичную задачу решает контрастная МРТ печени с динамическими сериями и гепатоспецифическими препаратами, по этим исследованиям формируется карта вмешательства и определяется, возможно ли достижение радикального локального контроля с помощью РЧА.
- Ультразвуковое исследование печени с допплерографией служит как для уточнения анатомии до вмешательства, так и для навигации во время чрескожной абляции, при сканировании оцениваются размеры печени, структура паренхимы, наличие регенераторных узлов и признаков цирроза, визуализируются опухолевые очаги и их эхогенность, диаметр и проходимость воротной и печёночных вен, направление кровотока, состояние жёлчного пузыря и внутрипечёночных протоков, при достаточном акустическом окне интервенционный радиолог ориентируется по ультразвуку при введении электрода, после РЧА по УЗИ выявляются крупные гематомы, свободная жидкость и грубые изменения кровоснабжения.
- Обследования для стадирования включают КТ органов грудной клетки для выявления метастазов в лёгких и медиастинальных лимфатических узлах, КТ брюшной полости и забрюшинного пространства или МРТ брюшной полости и забрюшинного пространства для оценки состояния лимфатических коллекторов, надпочечников и других органов, при подозрении на множественные внепечёночные очаги или неясную КТ-картину используют ПЭТ-КТ, данные стадирования позволяют отличить ограниченное поражение, при котором РЧА имеет смысл как часть радикальной программы, от распространённого процесса, где локальный метод рассматривается как паллиативный компонент на фоне системной терапии.
- Специальные обследования при подготовке к радиочастотной абляции включают определение сывороточного альфа-фетопротеина и, при метастатическом поражении, других опухолевых маркёров, серологические тесты на вирусные гепатиты с оценкой активности процесса, при выраженной портальной гипертензии выполняется эзофагогастродуоденоскопия для выявления и градации варикозного расширения вен пищевода и желудка, в отдельных случаях используется эластография для количественной оценки фиброза, полученные данные влияют на выбор объёма абляции, необходимость предварительного лечения варикозных вен, коррекции асцита и уточняют прогноз переносимости процедуры.
Что важно знать пациентам
Какие риски рецидива рака после РЧА?
Даже при тщательно спланированной РЧ-абляции сохраняется риск локального рецидива по периферии зоны некроза и появления новых очагов в других сегментах печени, особенно на фоне цирроза или активного вирусного гепатита, по контрольной КТ или МРТ врачи оценивают, полностью ли выключен прежний узел и не появились ли новые образования, при выявлении ранних изменений иногда удаётся выполнить повторную РЧА или резекцию и удерживать процесс под контролем, поэтому уверенность в хорошем самочувствии не заменяет регулярные обследования.
Какие ограничения после РЧА?
В раннем восстановительном периоде обычно рекомендуют избегать подъёма тяжестей, интенсивных физических нагрузок, резких наклонов, прыжков и занятий контактными видами спорта, чтобы не спровоцировать кровотечение или смещение гематомы, важно соблюдать умеренный щадящий режим, постепенно увеличивать объём ходьбы, не употреблять алкоголь, ограничить тяжёлую жирную пищу, по согласованию с врачом корректировать приём обезболивающих и других препаратов, при стойком повышении температуры, нарастающей боли в животе, выраженной слабости или желтушности кожи необходимо немедленно связаться с медицинской командой.
Что делать после радиочастотной деструкции?
У большинства онкопациентов рак печени развивается на фоне хронического заболевания печени, и даже после успешного уничтожения конкретного узла остаётся риск появления новых опухолевых очагов и декомпенсации цирроза, онколог контролирует динамику по снимкам и маркёрам, а гепатолог следит за функцией органа, подбирает терапию асцита, портальной гипертензии и вирусного или алкогольного поражения, вместе определяют оптимальные интервалы обследований и при необходимости вовремя предлагают повторную РЧА, резекцию, системное лечение или обсуждение трансплантации, именно такое совместное наблюдение позволяет максимально использовать эффект локального вмешательства и поддерживать качество жизни.





























