- ДИАГНОСТИКА
- МРТ
- КТ
- КТ ГОЛОВЫ
- КТ ШЕИ
- КТ ГРУДНОЙ КЛЕТКИ
- КТ БРЮШНОЙ ПОЛОСТИ
- КТ МАЛОГО ТАЗА
- КТ ПОЗВОНОЧНИКА
- КТ СУСТАВОВ
- КТ КОСТЕЙ
- КТ АНГИОГРАФИЯ
- КТ ЗУБОВ
- УЗИ
- УЗИ ОРГАНОВ МАЛОГО ТАЗА
- УЗИ БРЮШНОЙ ПОЛОСТИ
- УЗИ ЗАБРЮШИННОГО ПРОСТРАНСТВА
- УЗИ СЕРДЦА
- УЗИ СОСУДОВ
- УЗИ МЯГКИХ ТКАНЕЙ, НЕРВОВ И ЖЕЛЕЗ
- УЗИ СУСТАВОВ
- УЗИ ГОЛОВЫ
- УЗИ ЛИМФОУЗЛОВ
- УЗИ ПРИ БЕРЕМЕННОСТИ
- УЗИ ПЛОДА
- УЗИ НОВРОЖДЕННОМУ РЕБЕНКУ
- УЗИ ПОСЛЕ АБОРТА
- РЕНТГЕН
- ВРАЧИ
- КАКОЙ ВРАЧ ЛЕЧИТ
- АКУШЕР-ГИНЕКОЛОГ
- АЛЛЕРГОЛОГ
- ВЕРТЕБРОЛОГ
- ВЕСТИБУЛОЛОГ
- ГАСТРОЭНТЕРОЛОГ
- ГЕМАТОЛОГ
- ГИНЕКОЛОГ
- ДЕРМАТОЛОГ
- ДИЕТОЛОГ
- ИГЛОТЕРАПЕВТ
- ИММУНОЛОГ
- ИНФЕКЦИОНИСТ
- КАРДИОЛОГ
- ВРАЧ ЛЕЧЕБНОЙ ФИЗКУЛЬТУРЫ
- МАММОЛОГ
- НЕВРОЛОГ
- НЕЙРОХИРУРГ
- НЕОНАТОЛОГ
- НЕФРОЛОГ
- ОНКОЛОГ
- ОНКОЛОГ-МАММОЛОГ
- ОРТОПЕД
- ОРТОПЕД-ХИРУРГ
- ОТОЛАРИНГОЛОГ
- ОФТАЛЬМОЛОГ
- ОСТЕОПАТ
- ПЕДИАТР
- ПРОКТОЛОГ
- ПСИХИАТР
- ПСИХОТЕРАПЕВТ
- ПУЛЬМОНОЛОГ
- РЕВМАТОЛОГ
- РЕФЛЕКСОТЕРАПЕВТ
- СЕКСОЛОГ
- СОМНОЛОГ
- СОСУДИСТЫЙ ХИРУРГ
- СПОРТИВНЫЙ ВРАЧ
- ТЕРАПЕВТ
- ТРАВМАТОЛОГ
- ТРИХОЛОГ
- УРОЛОГ
- ФИЗИОТЕРАПЕВТ
- ФЛЕБОЛОГ
- ФТИЗИАТР
- ВРАЧ ФУНКЦИОНАЛЬНОЙ ДИАГНОСТИКИ
- ХИРУРГ
- ЭНДОКРИНОЛОГ
- ЭНДОСКОПИСТ
- ЭПИЛЕПТОЛОГ
- СПОРТИВНЫЙ МАССАЖИСТ
- ГЕПАТОЛОГ
- ПАРАЗИТОЛОГ
- МАНУАЛЬНЫЙ ТЕРАПЕВТ
- СЕМЕЙНЫЙ ПСИХОЛОГ
- ВРАЧ ОБЩЕЙ ПРАКТИКИ
- ПРОФПАТОЛОГ-ТЕРАПЕВТ
- АНДРОЛОГ
- АНГИОЛОГ
- АРИТМОЛОГ
- АРТРОЛОГ
- БРОНХОЛОГ
- ВЕНЕРОЛОГ
- ГЕМОСТАЗИОЛОГ
- ГИРУДОТЕРАПЕВТ
- ДИАБЕТОЛОГ
- КИНЕЗИОЛОГ
- РАДИОТЕРАПЕВТ
- РЕПРОДУКТОЛОГ
- СУРДОЛОГ
- ФОНИАТР
- ХИМИОТЕРАПЕВТ
- СКИДКИ
- НА КАРТЕ
- МРТ РЯДОМ (поиск по району)
- АДМИРАЛТЕЙСКИЙ РАЙОН
- ВАСИЛЕОСТРОВСКИЙ РАЙОН
- ВЫБОРГСКИЙ РАЙОН
- КАЛИНИНСКИЙ РАЙОН
- КИРОВСКИЙ РАЙОН
- КОЛПИНСКИЙ РАЙОН
- КРАСНОГВАРДЕЙСКИЙ РАЙОН
- КРАСНОСЕЛЬСКИЙ РАЙОН
- КРОНШТАДТСКИЙ РАЙОН
- КУРОРТНЫЙ РАЙОН
- МОСКОВСКИЙ РАЙОН
- НЕВСКИЙ РАЙОН
- ПЕТРОГРАДСКИЙ РАЙОН
- ПЕТРОДВОРЦОВЫЙ РАЙОН
- ПРИМОРСКИЙ РАЙОН
- ПУШКИНСКИЙ РАЙОН
- ФРУНЗЕНСКИЙ РАЙОН
- ЦЕНТРАЛЬНЫЙ РАЙОН
- ЛЕН. ОБЛАСТЬ
- КТ и МСКТ РЯДОМ (поиск по району)
- АДМИРАЛТЕЙСКИЙ РАЙОН
- ВАСИЛЕОСТРОВСКИЙ РАЙОН
- ВЫБОРГСКИЙ РАЙОН
- КАЛИНИНСКИЙ РАЙОН
- КИРОВСКИЙ РАЙОН
- КОЛПИНСКИЙ РАЙОН
- КРАСНОГВАРДЕЙСКИЙ РАЙОН
- КРАСНОСЕЛЬСКИЙ РАЙОН
- КРОНШТАДТСКИЙ РАЙОН
- КУРОРТНЫЙ РАЙОН
- МОСКОВСКИЙ РАЙОН
- НЕВСКИЙ РАЙОН
- ПЕТРОГРАДСКИЙ РАЙОН
- ПЕТРОДВОРЦОВЫЙ РАЙОН
- ПРИМОРСКИЙ РАЙОН
- ПУШКИНСКИЙ РАЙОН
- ФРУНЗЕНСКИЙ РАЙОН
- ЦЕНТРАЛЬНЫЙ РАЙОН
- ЛЕН. ОБЛАСТЬ
- МРТ АДРЕСА БОЛЬНИЦ В СПБ
- МРТ РЯДОМ (поиск по району)
Адреса и стоимость операции в СПБ
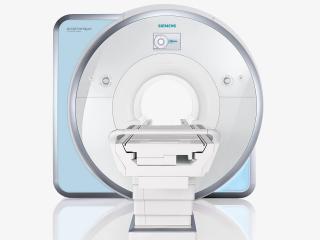
Цена указана с учетом льгот и акции
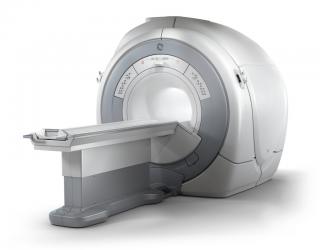
Цена указана с учетом льгот и акции
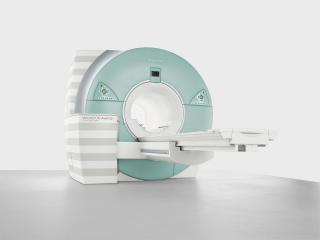
Цена указана с учетом льгот и акции
Услуга лечения онкологии
Услуга лечебного сопровождения для пациентов с онкологией — это индивидуальная комплексная помощь, которая может включать:
 Лучшиие онкологидоступ к ведущим специалистам Санкт-Петербурга, которые подберут современные схемы терапии и проконтролируют эффективность лечения на каждом этапе.
Лучшиие онкологидоступ к ведущим специалистам Санкт-Петербурга, которые подберут современные схемы терапии и проконтролируют эффективность лечения на каждом этапе. Госпитализация или дневной стационарвозможность пройти лечение в комфортных условиях ведущих онкологических центров Санкт-Петербурга.
Госпитализация или дневной стационарвозможность пройти лечение в комфортных условиях ведущих онкологических центров Санкт-Петербурга. Персональный протокол леченияразработка индивидуальной стратегии терапии с учётом типа опухоли, стадии заболевания, генетических особенностей, сопутствующих состояний и истории предыдущего лечения.
Персональный протокол леченияразработка индивидуальной стратегии терапии с учётом типа опухоли, стадии заболевания, генетических особенностей, сопутствующих состояний и истории предыдущего лечения. Второе независимое мнениеэкспертная оценка диагноза и лечебной тактики от ведущих онкологов, позволяющая подтвердить правильность выбранной стратегии, получить дополнительные варианты терапии, избежать ошибок и повысить шансы на успешный результат благодаря объективному профессиональному взгляду стороннего специалиста.
Второе независимое мнениеэкспертная оценка диагноза и лечебной тактики от ведущих онкологов, позволяющая подтвердить правильность выбранной стратегии, получить дополнительные варианты терапии, избежать ошибок и повысить шансы на успешный результат благодаря объективному профессиональному взгляду стороннего специалиста.
Лучшие специалисты в Санкт-Петербурге с рейтингом 4.5+
Последние отзывы
Что такое операция по удалению аденокарциномы легкого?
Операция по удалению аденокарциномы лёгкого представляет анатомическую резекцию части лёгкого с удалением опухоли и регионарных лимфатических узлов, объём может варьировать от сегментэктомии до лобэктомии или пневмонэктомии в зависимости от распространённости и функционального резерва.
Виды протоколов
Программа анатомической лобэктомии с систематической медиастинальной лимфодиссекцией используется, как базовый радикальный вариант при резектабельной аденокарциноме лёгкого, когда цель сводится к удалению опухоли в пределах доли с полноценной оценкой N-статуса. Доступ формируют торакотомически или эндоскопически по ситуации, затем пересекают и прошивают долевые ветви лёгочной артерии, вены и долевой бронх с поэтапной обработкой сосудисто-бронхиального пучка, удаляют долю единым препаратом и выполняют блоковое удаление лимфатической клетчатки ворот лёгкого и средостения с маркировкой станций. Практическая задача заключается в достижении R0-резекции и в уменьшении риска локорегионарного рецидива, поскольку неполная лимфодиссекция и оставленные микрометастазы в узлах ухудшают прогноз даже при небольшом первичном очаге.
Сегментэктомия с обязательной лимфодиссекцией, как органосохраняющий вариант рассматривается при периферических опухолях малого размера и при морфологической и визуализирующей уверенности в ограниченном распространении, когда требуется сохранить функциональный резерв лёгких без компромисса по онкологической радикальности. Этап строится на выделении сегментарной артерии, вены и бронха с последующим формированием межсегментарной плоскости по инфляционно-дефляционному признаку или по флуоресцентной навигации, затем выполняют анатомическое удаление сегмента и оценивают края резекции срочной морфологией по клинической ситуации. Практическая цель сводится к радикальному удалению очага при меньшей потере паренхимы, поскольку сохранение объёма дыхательной поверхности уменьшает одышку и повышает переносимость последующего лечения при необходимости.
Клиновидная резекция с интраоперационной верификацией краёв используется, как компромиссный вариант при крайне ограниченном кардиореспираторном резерве и при небольших периферических очагах, когда анатомическая резекция недоступна по функциональным причинам. Тактика строится на иссечении опухоли с адекватным клином здоровой ткани, герметизации паренхимы сшивающими аппаратами или ручным швом и обязательной оценке краёв, затем добавляют выборочную лимфатическую оценку ворот и средостения по ситуации. Практическая задача состоит в локальном контроле при минимальном объёме резекции, поскольку отсутствие радикальности по краю формирует высокий риск местного рецидива.
Пневмонэктомия при центральной аденокарциноме и при невозможности сформировать безопасный край бронха или сосудов в пределах доли рассматривается как радикальный вариант при условии достаточного функционального резерва и при отсутствии противопоказаний по правому желудочку и газообмену. Вмешательство включает поочерёдную обработку лёгочной артерии и вен с последующим пересечением главного бронха на уровне, обеспечивающем отрицательный край, затем выполняют ушивание культи бронха с укрытием тканевым лоскутом по возможности и удаляют лимфатические станции средостения. Практическая цель заключается в достижении R0 при центральном росте, поскольку попытка «сохранить долю» при сомнительных краях повышает риск бронхоплеврального свища и раннего местного рецидива.
Бронхопластическая резекция по типу «рукавной» лобэктомии при опухоли, вовлекающей устье долевого бронха, используется для сохранения лёгочной паренхимы при обеспечении радикального проксимального и дистального краёв. После удаления поражённой доли выполняют резекцию участка бронха с формированием бронхо-бронхиального анастомоза без натяжения и с контролем герметичности, по клинической ситуации выполняют укрытие анастомоза перикардиальным, плевральным или межрёберным лоскутом и дополняют операцию систематической лимфодиссекцией. Практическая задача связана с уменьшением объёма резекции при сохранении онкологической полноценности, поскольку сохранение дыхательной поверхности снижает риск хронической дыхательной недостаточности при сопоставимом радикальном результате.
Сосудистая реконструкция в рамках лобэктомии или билобэктомии при ограниченном вовлечении ветвей лёгочной артерии используется для избегания пневмонэктомии при сохранении возможности R0. Этап включает краевую резекцию артериальной стенки с пластикой или сегментарную резекцию с сосудистым анастомозом, затем выполняют стандартную обработку бронха и вен с последующей проверкой гемостаза и перфузии оставшейся паренхимы. Практическая цель заключается в сохранении объёма лёгкого без остаточной опухоли на сосудистой стенке, поскольку компромисс по сосудистому краю ведёт к раннему прогрессированию и осложнениям в зоне реконструкции.
Комбинированная резекция с удалением участка грудной стенки, перикарда или диафрагмы применяется при локально распространённой аденокарциноме с прямой инвазией соседних структур, когда R0 требует удаления единым блоком с поражённым компонентом. После мобилизации лёгкого выполняют резекцию вовлечённой структуры с реконструкцией сетчатым или тканевым материалом по ситуации, затем формируют анатомическую резекцию лёгкого и медиастинальную лимфодиссекцию с оценкой краёв. Практическая задача состоит в достижении отрицательных краёв и в устранении источника боли и компрессии, поскольку фрагментарное удаление без единого блока увеличивает риск опухолевой диссеминации и местного рецидива.
Минимально инвазивная программа резекции при аденокарциноме лёгкого с видеоторакоскопическим или робот-ассистированным доступом применяется при стадиях, допускающих выполнение анатомической резекции и полноценной лимфодиссекции без ухудшения онкологического объёма. Тактика включает эндоскопическую диссекцию сосудисто-бронхиальных структур под увеличением, удаление препарата в контейнере и систематическое удаление лимфатических станций средостения, затем выполняют аэростатическую пробу на утечку воздуха и устанавливают плевральный дренаж. Практическая цель заключается в снижении послеоперационной боли и ускорении восстановления дыхательной механики при сохранении радикальности, поскольку меньшая травматизация грудной стенки облегчает кашлевой толчок и снижает частоту ателектазов.
Программа хирургического этапа после индукционной химиолучевой или лекарственной терапии при исходно погранично резектабельном процессе используется, когда достигнута регрессия и сформированы условия для R0. Перед резекцией выполняют повторную оценку резектабельности по данным контрольных исследований и по интраоперационной ревизии, затем осуществляют анатомическую резекцию выбранного объёма с лимфодиссекцией, уделяя повышенное внимание тканевой хрупкости и гемостазу в зоне постлучевых изменений. Практическая задача состоит в закреплении достигнутого ответа и в удалении остаточной опухоли, поскольку фиброз и изменённая анатомия после индукции повышают риск сосудистых осложнений и требуют выверенной техники.
Помощь онкобольным
Профилактика дыхательных осложнений после резекции лёгкого строится на ранней активизации, восстановлении эффективного кашля и поддержании адекватной вентиляции нижних долей, поскольку боль и гиподинамия быстро приводят к ателектазам и пневмонии. В тактику включают дыхательные манёвры с контролем глубины вдоха, тренировку откашливания, ингаляционную поддержку по симптомам, раннюю вертикализацию и дозированную ходьбу, а при мокроте и бронхообструкции усиливают бронхолитическую и муколитическую часть. Нарастание одышки, лихорадка и снижение сатурации требуют немедленной оценки, поскольку аспирация, пневмония и тромбоэмболия нередко маскируются сходными симптомами.
Мультимодальная анальгезия после торакального вмешательства направлена на сохранение дыхательного объёма и возможности активного кашля без выраженной седации, поскольку поверхностное дыхание увеличивает риск осложнений. В раннем периоде используют регионарные методики по клинической ситуации в сочетании с ненаркотическими анальгетиками, при прорывной боли добавляют короткодействующие опиоиды под контролем дыхания и сознания. Усиление боли вместе с тахикардией и падением давления требует исключения внутриплеврального кровотечения, поскольку подобная динамика не укладывается в обычное послеоперационное течение.
Ведение плеврального дренажа и контроль утечки воздуха после резекции лёгкого опираются на оценку характера отделяемого, объёма воздуха по водяному затвору и динамику расправления лёгкого на контрольных снимках. При стойкой утечке воздуха корректируют режим дренирования, оценивают необходимость бронхоскопии для исключения проблем культи бронха и рассматривают эндоскопические методы герметизации по показаниям. Резкое нарастание подкожной эмфиземы, ухудшение дыхания и асимметрия грудной клетки требуют срочной оценки, поскольку напряжённый пневмоторакс и несостоятельность культи являются жизнеугрожающими ситуациями.
Профилактика тромбоэмболических осложнений после торакальной операции строится на сочетании ранней ходьбы, механической компрессии и антикоагулянтной поддержки по индивидуальному риску, поскольку онкологический процесс и вмешательство увеличивают склонность к тромбозам. Тактика кореллируется с кровоточивостью и дренажным отделяемым, при падении гемоглобина уточняют источник кровопотери и пересматривают баланс гемостаза. Внезапная одышка, боль в груди, кровохарканье и односторонний отёк конечности требуют срочной диагностики, поскольку тромбоэмболия лёгочной артерии развивается быстро.
Профилактика и раннее распознавание послеоперационной фибрилляции предсердий имеют значение после лобэктомии и пневмонэктомии, поскольку воспаление, болевой стресс и электролитные сдвиги повышают риск аритмий. Контроль строится на мониторинге ритма в ранние сутки, коррекции калия и магния, управлении болью и ранней мобилизации, при эпизодах тахиаритмии тактика включает частотный контроль и антикоагулянтные решения по индивидуальному риску. Учащённое сердцебиение с головокружением и падением давления требует немедленной оценки, поскольку гемодинамически значимая аритмия быстро ухудшает перфузию и дыхание.
Нутритивная поддержка после резекции лёгкого направлена на сохранение белково-энергетического баланса и профилактику саркопении, поскольку потеря мышечной массы снижает эффективность дыхательных упражнений и переносимость ходьбы. Питание выстраивают дробно с опорой на белок, контролируют достаточность жидкости, при снижении аппетита подключают специализированные смеси, а при выраженной тошноте корректируют противорвотную тактику по механизму действия. Прогрессирующая слабость, снижение массы тела и невозможность поддерживать активность требуют раннего усиления нутритивной поддержки, поскольку истощение увеличивает риск инфекций и замедляет восстановление.
Отказ от курения и контроль бронхиальной гиперреактивности до и после операции критичны для заживления и дыхательной функции, поскольку табачный дым ухудшает мукоцилиарный клиренс и усиливает бронхоспазм. План включает прекращение курения до операции с поддержкой никотинзаместительной терапии по ситуации, обучение ингаляционной технике при обструкции и контроль мокроты, что уменьшает риск пневмонии и длительной утечки воздуха. Упорный кашель с гнойной мокротой и лихорадкой требуют немедленной оценки, поскольку инфекция дыхательных путей быстро осложняет течение послеоперационного периода.
Какие врачи могут быть вовлечены
- Торакальный онкохирург определяет объём анатомической резекции от сегментэктомии до лобэктомии или пневмонэктомии, выбирает необходимость бронхопластики и сосудистой реконструкции, увязывает решение со стадией и с резервом дыхательной функции. Во время операции торакальный хирург контролирует радикальность по краям резекции, выполняет систематическое удаление лимфатических станций средостения и ворот лёгкого и задаёт тактику плеврального дренирования, поскольку качество лимфодиссекции и герметичность паренхимы определяют риск местного рецидива, утечки воздуха и инфекционных осложнений.
- Анестезиолог-реаниматолог формирует план однолёгочной вентиляции, управляет гемодинамикой и обезболиванием, оценивает риск аспирации и выбирает объём мониторинга с учётом длительности вмешательства и вероятной кровопотери. В раннем периоде анестезиолог-реаниматолог контролирует восстановление дыхания, тошноту, болевой синдром и кислотно-щелочной баланс, корректирует инфузионную нагрузку и потребность в вазопрессорах, поскольку перегрузка объёмом ухудшает газообмен и повышает риск отёка оставшейся паренхимы.
- Интенсивист отделения реанимации ведёт пациента в первые часы и сутки после обширных резекций, контролирует сатурацию, газообмен, диурез, электролиты и динамику дренажного отделяемого, быстро выявляет кровотечение, утечку воздуха и аритмии. Интенсивист координирует раннюю вертикализацию, дыхательные манёвры и профилактику тромбозов, поскольку задержка активизации резко увеличивает вероятность ателектазов и тромбоэмболических осложнений.
- Пульмонолог участвует до операции для оптимизации бронходилатационной схемы при обструкции, санации мокроты и оценки риска послеоперационного бронхоспазма, а также помогает интерпретировать одышку в раннем периоде. Пульмонолог отделяет ателектаз и пневмонию от тромбоэмболии и декомпенсации хронической обструктивной болезни лёгких, подбирает ингаляционную поддержку и режим физиотерапии дыхательных путей, поскольку ошибки в трактовке одышки приводят к поздней коррекции.
- Кардиолог оценивает ишемический и ритмологический риск, переносимость однолёгочной вентиляции при лёгочной гипертензии и состояние правых отделов сердца, задаёт безопасную тактику контроля давления и частоты пульса. Кардиолог корректирует ведение при послеоперационной фибрилляции предсердий и электролитных сдвигах, помогает выбрать антикоагулянтную тактику при наличии факторов риска, поскольку аритмии и правожелудочковая перегрузка способны резко ухудшать газообмен.
- Эндоскопист участвует в предоперационной бронхоскопии для уточнения эндобронхиального компонента, определения уровня резекции при бронхопластике и санации дыхательных путей при мокроте и кровохарканье. В послеоперационном периоде эндоскопист выполняет бронхоскопическую оценку культи бронха и проходимости анастомоза при подозрении на несостоятельность, а также помогает устранить слизистые пробки, поскольку обтурация бронха ускоряет формирование ателектаза.
- Патоморфолог подтверждает морфологический тип аденокарциномы, оценивает края резекции, степень дифференцировки, сосудистую и плевральную инвазию, а также статус лимфатических узлов по станциям. Заключение патоморфолога определяет послеоперационную стратегию консилиума, поскольку pT/pN, плевральная инвазия и микрососудистое распространение меняют показания к адъювантной терапии.
- Специалист лучевой диагностики интерпретирует предоперационные исследования грудной клетки и надключичных зон, оценивает динамику очага, признаки инвазии в сосуды и грудную стенку и состояние лимфатических коллекторов, что влияет на план резекции. В послеоперационном периоде специалист лучевой диагностики оценивает расправление лёгкого, плевральные проявления и признаки кровотечения, помогает быстро подтвердить причину ухудшения дыхания, поскольку клиническая картина осложнений нередко неспецифична.
- Онколог-химиотерапевт определяет последовательность лекарственного этапа при необходимости неоадъювантной или адъювантной терапии, согласует сроки операции с восстановлением гемограммы и формирует критерии безопасного возобновления системного лечения после резекции. Роль онколога-химиотерапевта важна для непрерывности лечения, поскольку затяжное восстановление после осложнений снижает шанс вовремя начать адъювантный этап.
- Реабилитолог формирует план дыхательной реабилитации и расширения физической активности, обучает технике дыхательных упражнений и контролирует переносимость ходьбы и лестничных нагрузок. Ранняя реабилитация уменьшает риск контрактур плечевого пояса и хронической одышки, поскольку ограничение движений и страх боли часто мешают полноценной вентиляции нижних долей лёгких.
Какие обследования назначаются
- Клиническая оценка перед вмешательством фиксирует функциональный статус, выраженность одышки, кашля и мокроты, переносимость ходьбы, наличие потери массы тела, а также признаки инфекции дыхательных путей. В раннем периоде клинический контроль ориентируют на сатурацию, частоту дыхания, температуру, характер мокроты, динамику боли и свойства дренажного отделяемого, поскольку первые признаки пневмонии, кровотечения и утечки воздуха часто проявляются системно.
- Компьютерная томография грудной клетки с контрастированием используется для планирования объёма резекции и оценки взаимоотношения опухоли с сосудами и бронхами, а также для уточнения медиастинальных узлов и плеврального компонента. При осложнённом течении после операции КТ помогает выявлять плевральные новообразования, активное кровотечение, инфаркт оставшейся паренхимы и тромбоэмболию при соответствующей клинической картине.
- ПЭТ-КТ применяют для уточнения распространённости процесса и оценки метаболической активности лимфатических узлов перед радикальным этапом, что снижает риск недооценки стадии и неоправданной операции. В послеоперационном наблюдении ПЭТ-КТ рассматривают при сомнительных находках на КТ и при необходимости отличить рубцовые изменения от рецидива.
- Магнитно-резонансная томография головного мозга используется при неврологической симптоматике и при клинической необходимости исключить метастатическое поражение до планирования радикальной резекции. МРТ обладает высокой чувствительностью к мелким очагам и помогает своевременно изменить лечебную последовательность, когда требуется локальный этап в отношении центральной нервной системы.
- Бронхоскопия помогает уточнить эндобронхиальное распространение, оценить источник кровохарканья и выполнить санацию трахеобронхиального дерева при выраженной мокроте. В послеоперационном периоде бронхоскопия используется при подозрении на обтурацию бронха слизистой пробкой и при необходимости оценить культю бронха, поскольку ранняя санация уменьшает риск ателектаза.
- Спирометрия с оценкой бронхиальной проходимости, диффузионной способности и, по клинической ситуации, нагрузочные тесты помогают рассчитать ожидаемую послеоперационную функцию лёгких и выбрать безопасный объём резекции. Данный блок критичен при планировании пневмонэктомии и при исходной обструкции, поскольку недостаточная предоперационная оценка повышает риск дыхательной недостаточности.
- Электрокардиография и эхокардиография уточняют кардиальный риск, оценивают состояние правых отделов сердца и лёгочное давление при подозрении на лёгочную гипертензию. В раннем периоде кардиологический мониторинг усиливают при тахиаритмиях и электролитных сдвигах, поскольку аритмии ухудшают перфузию и газообмен.
- Анализы крови контролируют до операции и в раннем периоде для оценки гемоглобина, лейкоцитарной реакции, электролитов, функции почек и печени и коагуляционного профиля, дополнительно отслеживают маркёры воспаления по клинической ситуации. Данный блок помогает корректировать анемию, контролировать инфекционные осложнения и безопасно вести антикоагулянтную профилактику.
Что важно знать пациентам
Почему вместе с опухолью удаляют лимфоузлы средостения?
Удаление лимфатических узлов средостения даёт точное стадирование и снижает риск локорегионарного рецидива, поскольку микрометастазы в узлах могут отсутствовать на КТ, но влиять на выбор адъювантной терапии и прогноз.
Какие осложнения?
Температура 38,0 °C и выше, нарастающая одышка, внезапная боль в груди, кровохарканье, выраженная слабость с тахикардией, резкое увеличение подкожной эмфиземы, усиление боли в зоне операции, обморок и односторонний отёк ноги требуют немедленной медицинской оценки, поскольку подобная динамика соответствует пневмонии, тромбоэмболии, кровотечению или проблеме с плевральной полостью.
восстановление дыхания
Ежедневная ходьба с постепенным увеличением дистанции, регулярные дыхательные упражнения, эффективное откашливание и адекватное обезболивание помогают поддерживать вентиляцию нижних долей лёгких и предотвращать ателектазы. Контроль мокроты и отказ от курения снижают риск воспаления, поскольку табачный дым ухудшает мукоцилиарный клиренс и повышает бронхиальную реактивность.
отказ от курения
Отказ от курения улучшает заживление бронхиальных структур, снижает риск длительной утечки воздуха и уменьшает частоту пневмонии, а контроль кашля позволяет отличить нормальный послеоперационный период от инфекции или аспирации. Упорный кашель с гнойной мокротой, лихорадка и снижение сатурации требуют ранней оценки, поскольку инфекционное осложнение быстро нарушает восстановление и откладывает последующие этапы лечения.
- Биопсия при раке легких
- Трансторакальная биопсия легкого
- Чрезбронхиальная биопсия легкого
- Паллиативное лечение рака легких
- Лечение метастазов легких
- Лечение немелкоклеточного рака легкого
- Лечение лимфомы легких
- Лечение центрального рака легкого
- Таргетная терапия рака легких
- Брахитерапия рака легкого
- Кибернож легких
- Цитогенетическая терапия легких
- Химиотерапия легких
- Операции метастазов легкого
- Скрининг рака легких
- Видеоторакоскопическая биопсия легких
- Аспирационная биопсия легких
- Паллиативная химиотерапия при раке легких
- Лечение рака легких
- Лечение периферического рака легкого
- Лечение меланомы легких
- Лечение аденокарциномы легкого
- Лучевая терапия рака легких
- Гормональная терапия легких
- Иммунотерапия легкого
- Химиотерапия аденокарциномы легкого
- Удаление лимфоузлов легких
- Стереотаксическая лучевая терапия легких











