- ДИАГНОСТИКА
- МРТ
- КТ
- КТ ГОЛОВЫ
- КТ ШЕИ
- КТ ГРУДНОЙ КЛЕТКИ
- КТ БРЮШНОЙ ПОЛОСТИ
- КТ МАЛОГО ТАЗА
- КТ ПОЗВОНОЧНИКА
- КТ СУСТАВОВ
- КТ КОСТЕЙ
- КТ АНГИОГРАФИЯ
- КТ ЗУБОВ
- УЗИ
- УЗИ ОРГАНОВ МАЛОГО ТАЗА
- УЗИ БРЮШНОЙ ПОЛОСТИ
- УЗИ ЗАБРЮШИННОГО ПРОСТРАНСТВА
- УЗИ СЕРДЦА
- УЗИ СОСУДОВ
- УЗИ МЯГКИХ ТКАНЕЙ, НЕРВОВ И ЖЕЛЕЗ
- УЗИ СУСТАВОВ
- УЗИ ГОЛОВЫ
- УЗИ ЛИМФОУЗЛОВ
- УЗИ ПРИ БЕРЕМЕННОСТИ
- УЗИ ПЛОДА
- УЗИ НОВРОЖДЕННОМУ РЕБЕНКУ
- УЗИ ПОСЛЕ АБОРТА
- РЕНТГЕН
- ВРАЧИ
- КАКОЙ ВРАЧ ЛЕЧИТ
- АКУШЕР-ГИНЕКОЛОГ
- АЛЛЕРГОЛОГ
- ВЕРТЕБРОЛОГ
- ВЕСТИБУЛОЛОГ
- ГАСТРОЭНТЕРОЛОГ
- ГЕМАТОЛОГ
- ГИНЕКОЛОГ
- ДЕРМАТОЛОГ
- ДИЕТОЛОГ
- ИГЛОТЕРАПЕВТ
- ИММУНОЛОГ
- ИНФЕКЦИОНИСТ
- КАРДИОЛОГ
- ВРАЧ ЛЕЧЕБНОЙ ФИЗКУЛЬТУРЫ
- МАММОЛОГ
- НЕВРОЛОГ
- НЕЙРОХИРУРГ
- НЕОНАТОЛОГ
- НЕФРОЛОГ
- ОНКОЛОГ
- ОНКОЛОГ-МАММОЛОГ
- ОРТОПЕД
- ОРТОПЕД-ХИРУРГ
- ОТОЛАРИНГОЛОГ
- ОФТАЛЬМОЛОГ
- ОСТЕОПАТ
- ПЕДИАТР
- ПРОКТОЛОГ
- ПСИХИАТР
- ПСИХОТЕРАПЕВТ
- ПУЛЬМОНОЛОГ
- РЕВМАТОЛОГ
- РЕФЛЕКСОТЕРАПЕВТ
- СЕКСОЛОГ
- СОМНОЛОГ
- СОСУДИСТЫЙ ХИРУРГ
- СПОРТИВНЫЙ ВРАЧ
- ТЕРАПЕВТ
- ТРАВМАТОЛОГ
- ТРИХОЛОГ
- УРОЛОГ
- ФИЗИОТЕРАПЕВТ
- ФЛЕБОЛОГ
- ФТИЗИАТР
- ВРАЧ ФУНКЦИОНАЛЬНОЙ ДИАГНОСТИКИ
- ХИРУРГ
- ЭНДОКРИНОЛОГ
- ЭНДОСКОПИСТ
- ЭПИЛЕПТОЛОГ
- СПОРТИВНЫЙ МАССАЖИСТ
- ГЕПАТОЛОГ
- ПАРАЗИТОЛОГ
- МАНУАЛЬНЫЙ ТЕРАПЕВТ
- СЕМЕЙНЫЙ ПСИХОЛОГ
- ВРАЧ ОБЩЕЙ ПРАКТИКИ
- ПРОФПАТОЛОГ-ТЕРАПЕВТ
- АНДРОЛОГ
- АНГИОЛОГ
- АРИТМОЛОГ
- АРТРОЛОГ
- БРОНХОЛОГ
- ВЕНЕРОЛОГ
- ГЕМОСТАЗИОЛОГ
- ГИРУДОТЕРАПЕВТ
- ДИАБЕТОЛОГ
- КИНЕЗИОЛОГ
- РАДИОТЕРАПЕВТ
- РЕПРОДУКТОЛОГ
- СУРДОЛОГ
- ФОНИАТР
- ХИМИОТЕРАПЕВТ
- СКИДКИ
- НА КАРТЕ
- МРТ РЯДОМ (поиск по району)
- АДМИРАЛТЕЙСКИЙ РАЙОН
- ВАСИЛЕОСТРОВСКИЙ РАЙОН
- ВЫБОРГСКИЙ РАЙОН
- КАЛИНИНСКИЙ РАЙОН
- КИРОВСКИЙ РАЙОН
- КОЛПИНСКИЙ РАЙОН
- КРАСНОГВАРДЕЙСКИЙ РАЙОН
- КРАСНОСЕЛЬСКИЙ РАЙОН
- КРОНШТАДТСКИЙ РАЙОН
- КУРОРТНЫЙ РАЙОН
- МОСКОВСКИЙ РАЙОН
- НЕВСКИЙ РАЙОН
- ПЕТРОГРАДСКИЙ РАЙОН
- ПЕТРОДВОРЦОВЫЙ РАЙОН
- ПРИМОРСКИЙ РАЙОН
- ПУШКИНСКИЙ РАЙОН
- ФРУНЗЕНСКИЙ РАЙОН
- ЦЕНТРАЛЬНЫЙ РАЙОН
- ЛЕН. ОБЛАСТЬ
- КТ и МСКТ РЯДОМ (поиск по району)
- АДМИРАЛТЕЙСКИЙ РАЙОН
- ВАСИЛЕОСТРОВСКИЙ РАЙОН
- ВЫБОРГСКИЙ РАЙОН
- КАЛИНИНСКИЙ РАЙОН
- КИРОВСКИЙ РАЙОН
- КОЛПИНСКИЙ РАЙОН
- КРАСНОГВАРДЕЙСКИЙ РАЙОН
- КРАСНОСЕЛЬСКИЙ РАЙОН
- КРОНШТАДТСКИЙ РАЙОН
- КУРОРТНЫЙ РАЙОН
- МОСКОВСКИЙ РАЙОН
- НЕВСКИЙ РАЙОН
- ПЕТРОГРАДСКИЙ РАЙОН
- ПЕТРОДВОРЦОВЫЙ РАЙОН
- ПРИМОРСКИЙ РАЙОН
- ПУШКИНСКИЙ РАЙОН
- ФРУНЗЕНСКИЙ РАЙОН
- ЦЕНТРАЛЬНЫЙ РАЙОН
- ЛЕН. ОБЛАСТЬ
- МРТ АДРЕСА БОЛЬНИЦ В СПБ
- МРТ РЯДОМ (поиск по району)
Показания для проведения операции
Основаниями для хирургического вмешательства могут служить следующие симптомы, которые могут указывать на наличие серьёзных нарушений и требовать хирургического вмешательства:
- рвота с кровью
- рвота
- нарушение функции глотания - дисфагия
- потеря веса
- боль при еде
- боль в эпигастрии
- боль в верхней части живота - эпигастральной области
Показания для проведения операции
Основаниями для хирургического вмешательства могут служить следующие симптомы, которые могут указывать на наличие серьёзных нарушений и требовать хирургического вмешательства:
- рвота
- рвота с кровью
- нарушение функции глотания - дисфагия
- потеря веса
- боль при еде
- боль в эпигастрии
- боль в верхней части живота - эпигастральной области
Кто выдает направление на пластику пищевода
- Гастроэнтеролог
Обязательные обследования перед операцией
Перед госпитализацией пациенту могут быть назначены ряд обследований и анализов:
- рентгенография органов грудной кетки
- электрокардиография
- коагулограмма
- анализ крови на скрытые инфекции
- биохимический анализ крови
- определение группы крови и резус-фактора
- общий анализ мочи
- общий анализ крови
- эзофагогастродуоденоскопия
- компьютерная виртуальная колоноскопия кишечника
- компьютерная томография пищевода
- рентгенография пищевода
- эзофагоскопия
- рентгенография желудка
Какой специалист выполняет хирургическое вмешательство
- Абдоминальный хирург
Адреса и стоимость операции пластики пищевода в СПБ
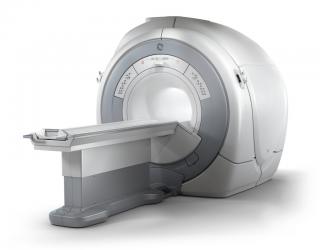
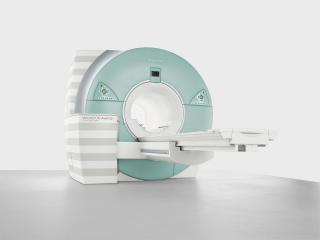
Лучшие специалисты в Санкт-Петербурге с рейтингом 4.5+
Что важно знать о записи на операцию
 Как пройти операцию по полису ОМС:если вам показана операция (включая высокотехнологичное вмешательство), лечащий врач направит вас на предоперационное обследование. Исходя из его результатов, он выпишет направление на операцию. Если необходима высокотехнологичная хирургия, финансируемая из бюджета, то решение о предоставлении такой помощи принимает специальная комиссия.
Как пройти операцию по полису ОМС:если вам показана операция (включая высокотехнологичное вмешательство), лечащий врач направит вас на предоперационное обследование. Исходя из его результатов, он выпишет направление на операцию. Если необходима высокотехнологичная хирургия, финансируемая из бюджета, то решение о предоставлении такой помощи принимает специальная комиссия. Сроки ожидания операции по ОМС:по законодательству, после того как лечащий врач выдаст направление, пациент должен быть госпитализирован в течение 14 дней. Для онкологических пациентов этот срок сокращается до 7 дней после получения результатов гистологии или предварительного диагноза. Для высокотехнологичных операций сроки ожидания не определены законом. Больницы, проводящие такие вмешательства, ведут свои списки ожидания.
Сроки ожидания операции по ОМС:по законодательству, после того как лечащий врач выдаст направление, пациент должен быть госпитализирован в течение 14 дней. Для онкологических пациентов этот срок сокращается до 7 дней после получения результатов гистологии или предварительного диагноза. Для высокотехнологичных операций сроки ожидания не определены законом. Больницы, проводящие такие вмешательства, ведут свои списки ожидания. Что взять с собой:для плановой госпитализации необходимо иметь с собой следующие документы: направление на госпитализацию от врача-хирурга из поликлиники, паспорт, полис обязательного медицинского страхования (ОМС), СНИЛС (страховой номер индивидуального лицевого счета), результаты амбулаторных обследований. Также рекомендуется взять с собой выписки из медицинских карт, заключения специалистов.
Что взять с собой:для плановой госпитализации необходимо иметь с собой следующие документы: направление на госпитализацию от врача-хирурга из поликлиники, паспорт, полис обязательного медицинского страхования (ОМС), СНИЛС (страховой номер индивидуального лицевого счета), результаты амбулаторных обследований. Также рекомендуется взять с собой выписки из медицинских карт, заключения специалистов. Врач не дает направление на операцию:если вам отказывают в выдаче направления формы 057/у-04 в нужную медицинскую организацию по ОМС, сначала обратитесь к администрации медучреждения с просьбой предоставить письменный отказ. Если проблему не решат, направьте жалобу в территориальный фонд ОМС или в Росздравнадзор.
Врач не дает направление на операцию:если вам отказывают в выдаче направления формы 057/у-04 в нужную медицинскую организацию по ОМС, сначала обратитесь к администрации медучреждения с просьбой предоставить письменный отказ. Если проблему не решат, направьте жалобу в территориальный фонд ОМС или в Росздравнадзор. Подготовка:перед операцией необходимо пройти ряд обязательных предоперационных обследований, включая клинический анализ крови, коагулограмма, общий анализ мочи, биохимический анализ крови, анализ крови на гепатит В и С (HBsAg и HCV), анализ крови на RW, группа крови и резус фактор, электрокардиограмма (ЭКГ), рентген грудной клетки. В зависимости от вида операции могут быть назначены различные виды диагностических исследований для оценки состояния органов. Операция может быть отложена, если результаты анализов покажут наличие противопоказаний.
Подготовка:перед операцией необходимо пройти ряд обязательных предоперационных обследований, включая клинический анализ крови, коагулограмма, общий анализ мочи, биохимический анализ крови, анализ крови на гепатит В и С (HBsAg и HCV), анализ крови на RW, группа крови и резус фактор, электрокардиограмма (ЭКГ), рентген грудной клетки. В зависимости от вида операции могут быть назначены различные виды диагностических исследований для оценки состояния органов. Операция может быть отложена, если результаты анализов покажут наличие противопоказаний. Анестезия:перед операцией уточните, какой тип анестезии будет применяться: местная, региональная или общая. Важно быть информированным о возможных рисках, связанных с выбранным методом. В отдельных случаях может потребоваться консультация с анестезиологом для оценки вашего состояния. Необходимо строго следовать рекомендациям анестезиолога, включая соблюдение режима отказа от пищи и воды перед операцией. Это поможет предотвратить такие осложнения, как рвота или аспирация во время хирургического вмешательства.
Анестезия:перед операцией уточните, какой тип анестезии будет применяться: местная, региональная или общая. Важно быть информированным о возможных рисках, связанных с выбранным методом. В отдельных случаях может потребоваться консультация с анестезиологом для оценки вашего состояния. Необходимо строго следовать рекомендациям анестезиолога, включая соблюдение режима отказа от пищи и воды перед операцией. Это поможет предотвратить такие осложнения, как рвота или аспирация во время хирургического вмешательства. Риски и осложнения:врач обязан ознакомить вас с возможными рисками и осложнениями, которые могут возникнуть во время и после операции, а также объяснить, какие меры будут предприняты для их устранения. К таким рискам могут относиться кровотечения, инфекции, аллергические реакции и другие возможные осложнения. Перед проведением операции вам предложат подписать информированное согласие, подтверждающее, что вы осведомлены обо всех рисках и даёте согласие на проведение хирургического вмешательства.
Риски и осложнения:врач обязан ознакомить вас с возможными рисками и осложнениями, которые могут возникнуть во время и после операции, а также объяснить, какие меры будут предприняты для их устранения. К таким рискам могут относиться кровотечения, инфекции, аллергические реакции и другие возможные осложнения. Перед проведением операции вам предложат подписать информированное согласие, подтверждающее, что вы осведомлены обо всех рисках и даёте согласие на проведение хирургического вмешательства. Послеоперационный период:в зависимости от типа операции, может потребоваться пребывание в стационаре для наблюдения за вашим состоянием и оказания необходимой медицинской помощи. Важно следовать всем рекомендациям врача, включая приём назначенных лекарств, соблюдение режима покоя и уход за операционной раной. Также может быть ограничена физическая активность. Врач предоставит вам подробный план реабилитации, который может включать восстановительные процедуры и контрольные осмотры.
Послеоперационный период:в зависимости от типа операции, может потребоваться пребывание в стационаре для наблюдения за вашим состоянием и оказания необходимой медицинской помощи. Важно следовать всем рекомендациям врача, включая приём назначенных лекарств, соблюдение режима покоя и уход за операционной раной. Также может быть ограничена физическая активность. Врач предоставит вам подробный план реабилитации, который может включать восстановительные процедуры и контрольные осмотры.
Как проходит пластика пищевода
Пластика пищевода проводится под общей анестезией с оротрахеальной интубацией и управляемой вентиляцией, катетеризируются центральная вена и артерия для мониторинга и инфузионной терапии, обеспечивается профилактика тромбозов и инфекций, доступ формируется в зависимости от уровня вмешательства — лапаротомия, торакоабдоминальный или комбинированный доступ, в ряде случаев используется лапароскопическая или торакоскопическая ассистенция. В реконструктивной фазе мобилизуется трансплантант с сохранением питающей сосудистой ножки, формируется необходимая длина и диаметр, сегмент проводится через заднее средостение, ретростернально или антеторакально, после чего накладывается пищеводно-кишечный или пищеводно-желудочный анастомоз.
Пластика пищевода желудком является наиболее распространённой методикой и заключается в формировании узкой желудочной трубки на основе правой желудочно-сальниковой артерии, после чего трансплантант проводится в грудную или шейную полость и анастомозируется с проксимальным отделом пищевода. Достоинствами метода являются хорошее кровоснабжение, простота формирования и низкий риск некроза, однако существует вероятность рефлюкса и нарушения моторики.
Пластика пищевода кишкой применяется при невозможности использования желудка, чаще используется сегмент тонкой кишки с сохранением сосудистой ножки, который мобилизуется на длину, достаточную для замещения дефекта, проводится в ретростернальном или антеторакальном положении и соединяется с пищеводом и желудком, обеспечивая непрерывность, при этом важно исключить перегибы и натяжение.
Пластика пищевода толстой кишкой показана при обширных дефектах или при невозможности использования других сегментов, трансплантант формируется из левого или правого отдела ободочной кишки с сохранением питающих сосудов, преимуществом является достаточная длина и устойчивость к кислотному воздействию, недостатком — техническая сложность и риск ишемии, поэтому контроль кровотока обязателен. Антеторакальная пластика пищевода участком тонкой кишки используется у пациентов с высоким риском при внутригрудных вмешательствах, при этом сегмент тонкой кишки проводится подкожно перед грудиной, что облегчает доступ для контроля и ревизии, однако повышает риск механической травмы и формирования стриктур.
Пластика пищевода желудочным стеблем заключается в формировании длинного узкого стебля из желудка с сохранением сосудистой ножки, который проводится в грудную или шейную полость. Метод обеспечивает надёжное кровоснабжение и высокую выживаемость трансплантанта, но требует тщательной мобилизации желудка и контроля перфузии.
Резекция пищевода с пластикой представляет собой комбинированное вмешательство, при котором удаляется поражённый сегмент органа и сразу восстанавливается непрерывность с помощью желудочного или кишечного фрагмента, выбор зависит от объёма резекции и состояния соседних органов, при онкологическом процессе операция дополняется лимфодиссекцией.
Одномоментная пластика пищевода выполняется в рамках одной операции и предусматривает одновременное удаление поражённого сегмента и реконструкцию, что позволяет быстрее восстановить питание и уменьшить риск осложнений, однако требует высокой технической точности и тщательного интраоперационного контроля герметичности анастомоза.
Пластика пищевода по Льюису выполняется в два этапа: сначала мобилизуется желудок через лапаротомию и формируется трансплантант, затем проводится торакотомия с резекцией пищевода и наложением внутригрудного пищеводно-желудочного анастомоза, методика применяется при опухолях средней и нижней трети и отличается радикальностью, однако сопровождается риском дыхательных осложнений.
Пластика пищевода ребёнку проводится с учётом меньшего объёма полостей и особенностей сосудистой анатомии, чаще используется желудок или сегмент толстой кишки, операция требует максимальной осторожности, исключения натяжения и перегибов пересаживаемого лоскута, у детей выше риск несостоятельности анастомоза и формирования стриктур, поэтому послеоперационный период требует строгого наблюдения, щадящей диеты и эндоскопического контроля на протяжении нескольких лет.
Осложнения и риски
Наиболее опасным ранним осложнением является несостоятельность анастомоза, которая приводит к медиастиниту, плевральному эмпиеме и септическим состояниям, требующим немедленной хирургической коррекции. Существенным риском является ишемия или некроз тканей, возникающие при нарушении кровотока по питающей ножке, что делает трансплантант нежизнеспособным и требует его замены. Ранние послеоперационные осложнения включают пневмонию, плеврит, ателектазы, сепсис, кровотечения и повреждение возвратного гортанного нерва, что сопровождается охриплостью, дисфонией и аспирацией. В поздние сроки высок риск формирования рубцовых стриктур в зоне анастомоза, требующих эндоскопического бужирования или стентирования, а также развития хронической дисфагии и гастроэзофагеального рефлюкса. У части пациентов отмечаются нутритивные нарушения в виде гипопротеинемии, анемии, гиповитаминозов и мальабсорбции, что требует длительной диетической коррекции и медикаментозной поддержки. Редкими, но тяжёлыми осложнениями являются формирование трахеопищеводных свищей, хроническая боль в грудной клетке, демпинг-синдром и функциональная несостоятельность восстановленного пищевода.
Как проходит восстановление
Восстановительный период проходит поэтапно и требует строгого контроля за состоянием анастомоза, кровоснабжением пересаженных тканей и функциональной адаптацией пищеварительной системы. В первые сутки пациент находится в отделении реанимации под инвазивным мониторингом гемодинамики, газообмена и диуреза, проводится эпидуральная или мультимодальная аналгезия, осуществляется профилактика тромбозов и дыхательных осложнений. Питание обеспечивается через еюностому или назоинтестинальный зонд, калорийность постепенно увеличивается в течение 3–5 суток, а на 5–7 сутки выполняется рентгенологическое исследование с водорастворимым контрастом для исключения несостоятельности анастомоза. При благоприятных результатах начинается переход к пероральному питанию: сначала прозрачные жидкости, затем пюреобразные блюда и мягкая диета. В течение последующих недель пациенту рекомендуется придерживаться дробного питания малыми порциями, избегать твёрдой и грубой пищи, соблюдать вертикальное положение после еды и сон с приподнятым изголовьем. На амбулаторном этапе, который может длиться до года, проводится наблюдение у хирурга и гастроэнтеролога, регулярная эндоскопическая оценка состояния слизистой и анастомоза, контроль лабораторных показателей с целью своевременной коррекции витаминно-минеральных нарушений. Ключевым признаком успешного восстановления является стабильное глотание, отсутствие выраженной дисфагии, поддержание массы тела и адаптация пищевода к новым условиям функционирования.