- ДИАГНОСТИКА
- МРТ
- КТ
- КТ ГОЛОВЫ
- КТ ШЕИ
- КТ ГРУДНОЙ КЛЕТКИ
- КТ БРЮШНОЙ ПОЛОСТИ
- КТ МАЛОГО ТАЗА
- КТ ПОЗВОНОЧНИКА
- КТ СУСТАВОВ
- КТ КОСТЕЙ
- КТ АНГИОГРАФИЯ
- КТ ЗУБОВ
- УЗИ
- УЗИ ОРГАНОВ МАЛОГО ТАЗА
- УЗИ БРЮШНОЙ ПОЛОСТИ
- УЗИ ЗАБРЮШИННОГО ПРОСТРАНСТВА
- УЗИ СЕРДЦА
- УЗИ СОСУДОВ
- УЗИ МЯГКИХ ТКАНЕЙ, НЕРВОВ И ЖЕЛЕЗ
- УЗИ СУСТАВОВ
- УЗИ ГОЛОВЫ
- УЗИ ЛИМФОУЗЛОВ
- УЗИ ПРИ БЕРЕМЕННОСТИ
- УЗИ ПЛОДА
- УЗИ НОВРОЖДЕННОМУ РЕБЕНКУ
- УЗИ ПОСЛЕ АБОРТА
- РЕНТГЕН
- ВРАЧИ
- КАКОЙ ВРАЧ ЛЕЧИТ
- АКУШЕР-ГИНЕКОЛОГ
- АЛЛЕРГОЛОГ
- ВЕРТЕБРОЛОГ
- ВЕСТИБУЛОЛОГ
- ГАСТРОЭНТЕРОЛОГ
- ГЕМАТОЛОГ
- ГИНЕКОЛОГ
- ДЕРМАТОЛОГ
- ДИЕТОЛОГ
- ИГЛОТЕРАПЕВТ
- ИММУНОЛОГ
- ИНФЕКЦИОНИСТ
- КАРДИОЛОГ
- ВРАЧ ЛЕЧЕБНОЙ ФИЗКУЛЬТУРЫ
- МАММОЛОГ
- НЕВРОЛОГ
- НЕЙРОХИРУРГ
- НЕОНАТОЛОГ
- НЕФРОЛОГ
- ОНКОЛОГ
- ОНКОЛОГ-МАММОЛОГ
- ОРТОПЕД
- ОРТОПЕД-ХИРУРГ
- ОТОЛАРИНГОЛОГ
- ОФТАЛЬМОЛОГ
- ОСТЕОПАТ
- ПЕДИАТР
- ПРОКТОЛОГ
- ПСИХИАТР
- ПСИХОТЕРАПЕВТ
- ПУЛЬМОНОЛОГ
- РЕВМАТОЛОГ
- РЕФЛЕКСОТЕРАПЕВТ
- СЕКСОЛОГ
- СОМНОЛОГ
- СОСУДИСТЫЙ ХИРУРГ
- СПОРТИВНЫЙ ВРАЧ
- ТЕРАПЕВТ
- ТРАВМАТОЛОГ
- ТРИХОЛОГ
- УРОЛОГ
- ФИЗИОТЕРАПЕВТ
- ФЛЕБОЛОГ
- ФТИЗИАТР
- ВРАЧ ФУНКЦИОНАЛЬНОЙ ДИАГНОСТИКИ
- ХИРУРГ
- ЭНДОКРИНОЛОГ
- ЭНДОСКОПИСТ
- ЭПИЛЕПТОЛОГ
- СПОРТИВНЫЙ МАССАЖИСТ
- ГЕПАТОЛОГ
- ПАРАЗИТОЛОГ
- МАНУАЛЬНЫЙ ТЕРАПЕВТ
- СЕМЕЙНЫЙ ПСИХОЛОГ
- ВРАЧ ОБЩЕЙ ПРАКТИКИ
- ПРОФПАТОЛОГ-ТЕРАПЕВТ
- АНДРОЛОГ
- АНГИОЛОГ
- АРИТМОЛОГ
- АРТРОЛОГ
- БРОНХОЛОГ
- ВЕНЕРОЛОГ
- ГЕМОСТАЗИОЛОГ
- ГИРУДОТЕРАПЕВТ
- ДИАБЕТОЛОГ
- КИНЕЗИОЛОГ
- РАДИОТЕРАПЕВТ
- РЕПРОДУКТОЛОГ
- СУРДОЛОГ
- ФОНИАТР
- ХИМИОТЕРАПЕВТ
- СКИДКИ
- НА КАРТЕ
- МРТ РЯДОМ (поиск по району)
- АДМИРАЛТЕЙСКИЙ РАЙОН
- ВАСИЛЕОСТРОВСКИЙ РАЙОН
- ВЫБОРГСКИЙ РАЙОН
- КАЛИНИНСКИЙ РАЙОН
- КИРОВСКИЙ РАЙОН
- КОЛПИНСКИЙ РАЙОН
- КРАСНОГВАРДЕЙСКИЙ РАЙОН
- КРАСНОСЕЛЬСКИЙ РАЙОН
- КРОНШТАДТСКИЙ РАЙОН
- КУРОРТНЫЙ РАЙОН
- МОСКОВСКИЙ РАЙОН
- НЕВСКИЙ РАЙОН
- ПЕТРОГРАДСКИЙ РАЙОН
- ПЕТРОДВОРЦОВЫЙ РАЙОН
- ПРИМОРСКИЙ РАЙОН
- ПУШКИНСКИЙ РАЙОН
- ФРУНЗЕНСКИЙ РАЙОН
- ЦЕНТРАЛЬНЫЙ РАЙОН
- ЛЕН. ОБЛАСТЬ
- КТ и МСКТ РЯДОМ (поиск по району)
- АДМИРАЛТЕЙСКИЙ РАЙОН
- ВАСИЛЕОСТРОВСКИЙ РАЙОН
- ВЫБОРГСКИЙ РАЙОН
- КАЛИНИНСКИЙ РАЙОН
- КИРОВСКИЙ РАЙОН
- КОЛПИНСКИЙ РАЙОН
- КРАСНОГВАРДЕЙСКИЙ РАЙОН
- КРАСНОСЕЛЬСКИЙ РАЙОН
- КРОНШТАДТСКИЙ РАЙОН
- КУРОРТНЫЙ РАЙОН
- МОСКОВСКИЙ РАЙОН
- НЕВСКИЙ РАЙОН
- ПЕТРОГРАДСКИЙ РАЙОН
- ПЕТРОДВОРЦОВЫЙ РАЙОН
- ПРИМОРСКИЙ РАЙОН
- ПУШКИНСКИЙ РАЙОН
- ФРУНЗЕНСКИЙ РАЙОН
- ЦЕНТРАЛЬНЫЙ РАЙОН
- ЛЕН. ОБЛАСТЬ
- МРТ АДРЕСА БОЛЬНИЦ В СПБ
- МРТ РЯДОМ (поиск по району)
Адреса и стоимость таргетной терапии в СПБ
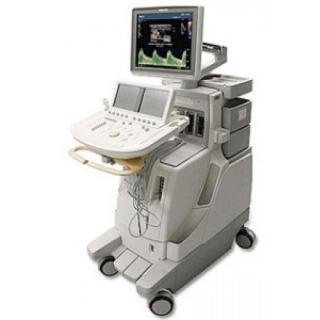
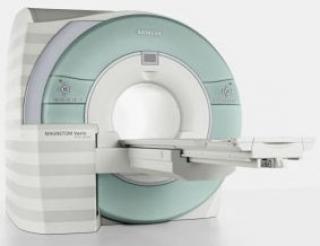
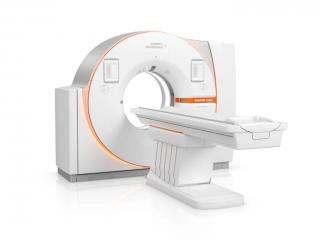
Услуга лечения онкологии
Услуга лечебного сопровождения для пациентов с онкологией — это индивидуальная комплексная помощь, которая может включать:
 Лучшиие онкологидоступ к ведущим специалистам Санкт-Петербурга, которые подберут современные схемы терапии и проконтролируют эффективность лечения на каждом этапе.
Лучшиие онкологидоступ к ведущим специалистам Санкт-Петербурга, которые подберут современные схемы терапии и проконтролируют эффективность лечения на каждом этапе. Госпитализация или дневной стационарвозможность пройти лечение в комфортных условиях ведущих онкологических центров Санкт-Петербурга.
Госпитализация или дневной стационарвозможность пройти лечение в комфортных условиях ведущих онкологических центров Санкт-Петербурга. Персональный протокол леченияразработка индивидуальной стратегии терапии с учётом типа опухоли, стадии заболевания, генетических особенностей, сопутствующих состояний и истории предыдущего лечения.
Персональный протокол леченияразработка индивидуальной стратегии терапии с учётом типа опухоли, стадии заболевания, генетических особенностей, сопутствующих состояний и истории предыдущего лечения. Второе независимое мнениеэкспертная оценка диагноза и лечебной тактики от ведущих онкологов, позволяющая подтвердить правильность выбранной стратегии, получить дополнительные варианты терапии, избежать ошибок и повысить шансы на успешный результат благодаря объективному профессиональному взгляду стороннего специалиста.
Второе независимое мнениеэкспертная оценка диагноза и лечебной тактики от ведущих онкологов, позволяющая подтвердить правильность выбранной стратегии, получить дополнительные варианты терапии, избежать ошибок и повысить шансы на успешный результат благодаря объективному профессиональному взгляду стороннего специалиста.
Лучшие специалисты в Санкт-Петербурге с рейтингом 4.5+
Последние отзывы
Что такое таргетная терапия при карциноме пищевода?
Таргетная терапия при раке пищевода основана на препаратах, которые действуют на конкретные молекулярные мишени в опухолевых клетках, например HER2 или факторы ангиогенеза. Для её назначения требуются иммуногистохимия и молекулярные тесты, подтверждающие нужные изменения, поэтому такой подход подходит не всем. Чаще эти препараты применяют при распространённом процессе или в линиях системного лечения аденокарцином дистального отдела и области гастроэзофагеального перехода с целью замедлить рост опухоли, уменьшить симптомы и продлить жизнь.
Варианты протоколов таргетной терапии рака пищевода
HER2-таргетная терапия с трастузумабом назначается при HER2-положительной аденокарциноме дистального отдела пищевода и зоны гастроэзофагеального перехода, когда по иммуногистохимии и дополнительным тестам подтверждена гиперэкспрессия или амплификация HER2. Препарат добавляют к платиново-фторпиримидиновой схеме в первой линии системного лечения, при этом регулярно контролируют функцию сердца по ЭхоКГ и оценивают динамику болезни по данным визуализации и уровню опухолевых маркеров. При хорошем ответе лечение продолжают до утраты эффективности или неприемлемой токсичности, что позволяет продлить контроль над заболеванием.
Анти-HER2-терапия антитело-конъюгатом фам-трастузумаб дерукстекан рассматривается при прогрессировании HER2-положительной аденокарциномы пищевода после режима с трастузумабом. Молекула сочетает в себе таргетное связывание с HER2 и доставку цитотоксического агента внутрь опухолевой клетки, поэтому способна работать в ситуации, когда классическая комбинация уже перестала давать эффект. На протяжении лечения внимательно отслеживают гематологические показатели, функцию лёгких и сердца, так как возможны интерстициальные поражения лёгочной ткани и кардиотоксичность, а при первых признаках осложнений дозу корректируют или временно прерывают терапию.
Антиангиогенная таргетная терапия рамуцирумабом используется при прогрессирующей аденокарциноме пищевода и гастроэзофагеального перехода, обычно во второй линии, в комбинации с паклитакселом или как монотерапия при ограниченном ресурсе организма. Препарат блокирует рецептор к сосудистому эндотелиальному фактору роста, снижая стимуляцию неоангиогенеза в опухоли и усиливая действие цитостатиков. Перед началом и в динамике контролируют артериальное давление, уровень белка в моче, показатели свёртываемости крови, а также оценивают риск тромботических и геморрагических осложнений, что особенно важно у пациентов с сердечно-сосудистыми заболеваниями.
EGFR-таргетная терапия моноклональными антителами или ингибиторами тирозинкиназ рассматривается при плоскоклеточном варианте рака пищевода преимущественно в рамках клинических исследований. Для отбора пациентов анализируют экспрессию EGFR и другие молекулярные характеристики опухоли, сопоставляя ожидаемую пользу со стандартными режимами, где основой остаются химиолучевые комбинации и иммунотерапия. На фоне лечения необходим тщательный мониторинг кожной сыпи, диареи, электролитных нарушений и функции печени, так как эти осложнения часто ограничивают дозу и длительность терапии.
Таргетная терапия при редких молекулярных нарушениях, таких как слияния генов NTRK или экспрессия CLDN18.2 в зоне гастроэзофагеального перехода, обсуждается у небольшой группы пациентов после расширенного молекулярного профилирования опухоли. В подобных ситуациях используют высокоспецифичные ингибиторы NTRK или таргетные антитела к CLDN18.2, чаще в рамках клинических исследований или программ раннего доступа, когда стандартные линии лечения уже исчерпаны. Решение принимается на мультидисциплинарном консилиуме с учётом общего состояния, целей терапии и ожидаемого профиля токсичности, а динамика контролируется по данным визуализации и самочувствию пациента.
Помощь онкобольным
Поддержка желудочно-кишечного тракта при таргетной терапии рака пищевода направлена на контроль диареи, тошноты, рвоты и воспаления слизистой. Рекомендуется щадящий режим питания с дробными приёмами пищи, мягкой или пюреобразной консистенцией, отказом от грубой клетчатки, очень горячих, острых и кислых блюд, усиливающих боль при глотании. При первых эпизодах диареи сразу подключают регидратацию, пероральные растворы, противодиарейные средства, периодически оценивают электролиты и функцию почек. При выраженной тошноте усиливают противорвотную терапию, при признаках обезвоживания переходят на внутривенное введение жидкости.
Кардиологическая и сосудистая поддержка особенно важна при схемах с HER2-направленными и антиангиогенными препаратами, которые воздействуют на миокард и сосуды. Перед началом курса фиксируют исходное артериальное давление, выполняют ЭКГ и эхокардиографию, уточняют перенесённые инфаркты, инсульты, тромбозы. В процессе лечения регулярно контролируют давление, одышку, отёки, появление перебоев в работе сердца, по показаниям корректируют антигипертензивную и антитромботическую терапию. При появлении признаков сердечной недостаточности или тяжёлой гипертензии временно приостанавливают таргетный препарат и усиливают кардиологическую защиту.
Контроль кожной и слизистой токсичности особенно актуален при схемах с воздействием на EGFR, где часто появляется акнеподобная сыпь, сухость кожи, трещины, поражения ногтевых валиков. Заблаговременно дают рекомендации по мягкому уходу за кожей, использованию увлажняющих средств без спирта и отдушек, защите от солнца и холода. При лёгких проявлениях достаточно местных противовоспалительных и антисептических средств, при более тяжёлых изменениях рассматривают системные препараты и временное снижение дозы таргетного лекарства. Важна профилактика вторичной инфекции: объясняют, почему нельзя выдавливать элементы сыпи и травмировать поражённые участки.
Нутритивная поддержка и коррекция нарушения глотания занимают центральное место, так как опухоль пищевода и лечение часто приводят к выраженной потере массы тела. Оценивают динамику веса, степень дисфагии, совместно с диетологом подбирают высококалорийные и высокобелковые продукты в мягкой или жидкой форме, а также специализированные смеси, которые легче проходят через суженный просвет. При невозможности обеспечить адекватное питание через рот обсуждают эндоскопическую установку стента, гастростомы или еюностомы, чтобы сохранить энтеральный путь и поддержать силы организма. Регулярно пересматривают нутритивный план по мере изменения симптомов и переносимости лечения.
Обезболивание и общий симптоматический контроль ориентированы на снижение боли за грудиной, дискомфорта при глотании и проявлений метастатического процесса. Начинают с нестероидных противовоспалительных препаратов с обязательной защитой слизистой желудка, при усилении болевого синдрома переходят на ступенчатые опиоидные схемы с подбором формы, удобной при дисфагии. Параллельно усиливают антисекреторную терапию, добавляют средства для защиты слизистой пищевода, при костных метастазах рассматривают локальное облучение или системные препараты для защиты костной ткани. Такая комбинация позволяет уменьшить страдания и сохранить повседневную активность.
Психологическая и паллиативная поддержка помогает справляться со страхом удушья, изменением внешнего вида, зависимостью от щадящей диеты или зондового питания. Психоонколог объясняет пациенту цели таргетной терапии, возможные сценарии течения болезни, обучает техникам снижения тревоги перед приёмом пищи и обострениями симптомов. При выраженной депрессии или стойкой бессоннице подключают медикаментозную помощь, обсуждают варианты посильной социальной активности и участие родственников в уходе. Команда паллиативной помощи помогает организовать наблюдение дома, контролировать боль и другие тяжёлые симптомы, чтобы максимально сохранить качество жизни на всех этапах лечения.
Какие врачи могут быть вовлечены
- Онколог координирует таргетную терапию рака пищевода, выбирает препарат с учётом стадии, молекулярных маркеров, общего состояния и переносимости предыдущих линий лечения. Онколог формирует последовательность линий, решает, когда комбинировать таргетный препарат с химиотерапией или иммунотерапией, и определяет необходимость перерыва или смены режима при токсичности. На консультациях онколог оценивает жалобы, массу тела, результаты анализов и визуализации, по совокупности данных корректирует дозу, интервал введения и длительность терапии, при сложных ситуациях выносит случай на консилиум.
- Торакальный хирург или абдоминальный хирург участвует в планировании лечения при резектабельном или погранично-резектабельном процессе, когда таргетная терапия сочетается с операцией. Хирург оценивает, удаётся ли за счёт лекарственного лечения уменьшить объём опухоли и улучшить условия для вмешательства, формулирует показания к стентированию пищевода или наложению гастростомы при выраженной дисфагии. После операции хирург контролирует заживление анастомоза, следит за риском кровотечения и перфорации на фоне продолжающегося системного лечения и участвует в выборе объёма паллиативных вмешательств при далеко зашедшем процессе.
- Гастроэнтеролог отвечает за ведение поражённого пищевода, желудка и кишечника в ходе таргетной терапии. Такой врач подбирает антисекреторные препараты, средства для защиты слизистой, схемы лечения рефлюкса, диареи или запоров, ориентируясь на профиль токсичности конкретного препарата. При выраженном эзофагите гастроэнтеролог корректирует питание, рекомендует лечебные смеси, изменяет текстуру пищи, при необходимости направляет на дополнительные обследования для исключения осложнений, которые требуют изменения системной терапии.
- Эндоскопист обеспечивает оценку просвета пищевода и выполнение вмешательств до начала и на этапах таргетной терапии. Эндоскопист определяет протяжённость стриктуры, состояние слизистой, проходимость стента, при необходимости выполняет дилатацию или замену конструкции. При кровотечении эндоскопист проводит гемостаз и по результату исследования помогает онкологу и хирургу решить, допустимо ли продолжать таргетное лечение в прежнем объёме или требуется коррекция.
- Кардиолог нужен при схемах с HER2-направленными и антиангиогенными препаратами, которые воздействуют на миокард и сосудистую систему. Кардиолог интерпретирует ЭКГ и эхокардиографию, оценивает фракцию выброса, контролирует артериальное давление, подбирает антигипертензивную и антиаритмическую терапию с учётом всей онкологической схемы. При появлении одышки, отёков, болей в грудной клетке кардиолог определяет, связано ли состояние с поражением сердца, и даёт рекомендации по временной отмене таргетного препарата, снижению дозы или усилению кардиологической защиты.
- Дерматолог подключается при лечении препаратами с выраженной кожной токсичностью, прежде всего при воздействии на EGFR. Врач оценивает степень сыпи, сухости, трещин, поражения ногтевых валиков, подбирает наружную терапию, антисептики, по показаниям назначает системные средства. Врач даёт подробные рекомендации по уходу за кожей, выбору моющих средств, защите от солнечного излучения и холода, а при тяжёлых проявлениях участвует в решении о временном снижении дозы или перерыве в таргетной терапии.
- Диетолог или врач по клиническому питанию ведёт нутритивную поддержку на фоне дисфагии и побочных эффектов лечения. Специалист оценивает исходный и текущий вес, рассчитывает потребность в калориях и белке, подбирает высококалорийные и белковые смеси, варианты мягкой, пюреобразной и жидкой пищи с учётом степени сужения просвета пищевода. При заметной потере массы тела и невозможности обеспечить достаточное питание через рот диетолог совместно с онкологом и хирургом обосновывает необходимость стента, гастростомы или еюностомы, а затем регулярно пересматривает нутритивный план.
- Психоонколог помогает справляться с тревогой, связанной с нарушением глотания, потерей веса, длительностью таргетной терапии и неопределённостью прогноза. Врач объясняет цели лечения, обсуждает возможные сценарии, обучает техникам релаксации и самопомощи при приступах страха перед приёмом пищи или обострением симптомов. При выраженной депрессии, стойкой бессоннице, панических реакциях психоонколог взаимодействует с психиатром, чтобы подобрать медикаментозную поддержку, что повышает приверженность лечению и снижает риск отказа от эффективной терапии.
- Врач по паллиативной помощи вовлекается при распространённом процессе, выраженной боли, тяжёлых симптомах, когда основная задача — облегчить состояние и сохранить качество жизни. Паллиативная служба подбирает опиоидную и сопутствующую терапию, схемы контроля тошноты, запоров, слабости, помогает организовать уход на дому и обучает родственников. Совместно с онкологом врач по паллиативной помощи решает, насколько целесообразно продолжать агрессивное лечение, какой объём обследований действительно нужен, и какие меры дадут наибольший прирост комфорта для пациента.
Какие обследования назначаются
- Лабораторные анализы крови при таргетной терапии рака пищевода охватывают общий анализ, базовую биохимию, печёночные ферменты, креатинин, электролиты, маркёры воспаления. До начала лечения фиксируют исходные значения, чтобы понимать запас по функции печени и почек, а также риск цитопений. В процессе курсов периодически пересматривают показатели, оценивают гепато- и нефротоксичность, склонность к тромбозам и кровотечениям, после завершения терапии продолжают редкий мониторинг с учётом полученной нагрузки.
- Общий анализ мочи и оценка протеинурии важны при использовании антиангиогенных препаратов, которые могут повреждать клубочковый аппарат и сосуды. Перед стартом лечения уточняют наличие белка, эритроцитов, цилиндров, чтобы не пропустить исходное поражение почек. В дальнейшем анализ мочи выполняют регулярно, обращают внимание на нарастающую протеинурию или гематурию, при существенных изменениях обсуждают коррекцию дозы или временную остановку таргетного препарата.
- ЭКГ относится к базовым обследованиям перед назначением HER2-направленных и антиангиогенных схем. На плёнке оценивают ритм, проводимость, признаки ишемии, гипертрофии, что помогает кардиологу судить о переносимости будущего лечения. В ходе терапии ЭКГ повторяют при появлении одышки, болей в груди, перебоев, а также перед сменой линий, особенно у пациентов с исходной кардиальной патологией.
- Эхокардиография используется для контроля сократительной функции миокарда при схемах с HER2-таргетными и некоторыми антиангиогенными препаратами. До начала лечения фиксируют фракцию выброса, состояние клапанов, признаки лёгочной гипертензии. В дальнейшем ЭхоКГ выполняют с заданной периодичностью, а при снижении сократимости или появлении клиники сердечной недостаточности решают вопрос о перерыве, смене схемы или усилении кардиологической терапии.
- КТ брюшной полости с контрастированием служит основным методом визуализации для оценки эффективности таргетной терапии и контроля осложнений. До старта лечения получают исходную картину распространённости опухоли, метастазов в лимфоузлах и органах. В процессе и после завершения курсов повторные исследования помогают судить о регрессе, стабилизации или прогрессировании заболевания, а также выявлять нежелательные явления, например тромбозы или перфорацию полых органов.
- ПЭТ-КТ с ФДГ проводится у части пациентов для более точной оценки метаболической активности очагов и раннего ответа на таргетную терапию. Исследование позволяет отличить живую опухолевую ткань от фиброза и посттерапевтических изменений, что особенно важно при сложной анатомии зоны гастроэзофагеального перехода. При подозрении на рецидив или олигометастатическое поражение ПЭТ-КТ помогает определить объём дальнейшего лечения и целесообразность локальных вмешательств.
- УЗИ органов брюшной полости и УЗИ лимфоузлов используется для динамического контроля печени, селезёнки, желчных путей и доступных зон лимфогенного распространения. До начала терапии метод помогает зафиксировать исходное состояние паренхимы и выявить мелкие очаги, которые не всегда заметны на КТ без контраста. В дальнейшем УЗИ удобно применять как промежуточный контроль между большими циклами томографии, особенно у пациентов с высоким риском лекарственного повреждения печени.
- КТ лёгких с контрастом используется при подозрении на интерстициальное поражение на фоне HER2-направленных антитело-конъюгатов или других таргетных схем с риском лекарственного пневмонита. Поводом для такого исследования служат сухой кашель, нарастающая одышка, субфебрилитет без явных признаков инфекции. Сравнение текущих снимков с исходными позволяет своевременно выявить интерстициальные изменения, принять решение о прекращении терапии и начать кортикостероидное лечение.
- Эзофагогастродуоденоскопия до, во время и после таргетной терапии даёт представление о состоянии слизистой пищевода, степени стеноза и риске кровотечения. Перед началом лечения эндоскопия помогает оценить протяжённость опухолевого поражения и сопутствующий эзофагит, а также установить или проконтролировать стент, если он уже стоит. В динамике метод используют при усилении дисфагии, болей, появлении крови, чтобы вовремя выявить язвы, некроз, кровоточащие сосуды и выполнить локальное лечение.
- Исследование акта глотания с контрастом или видеофлюороскопия применяется для оценки функциональных нарушений, которые сохраняются или усиливаются на фоне таргетной терапии. Тест показывает, как продвигается пищевой комок, где именно возникает задержка, есть ли риск аспирации, что важно для выбора консистенции пищи и необходимости зондового или гастростомического питания. На поздних этапах по результатам исследования решают, можно ли расширить рацион или требуется дальнейшая реабилитация с участием логопеда и команды по нутритивной поддержке.
Что важно знать пациентам
Как долго длится таргетное лечение?
Продолжительность терапии зависит от ответа опухоли и переносимости: терапию обычно продолжают месяцами до прогрессирования или выраженной токсичности. Введение может быть внутривенным раз в две–три недели или пероральным ежедневно по схеме, согласованной с онкологом. На всём протяжении курса проводятся регулярные осмотры, сдача анализов и контроль по визуализирующим методам, чтобы своевременно оценивать пользу и риски.
Какие побочные эффекты?
На фоне схем онколечения у пациента возможны утомляемость, снижение аппетита, тошнота, послабление стула или запоры, усиление боли при глотании. Отдельные препараты вызывают кожную сыпь, трещины кожи, изменения ногтей, другие влияют на артериальное давление, работу сердца и риск тромбозов. Антитело-конъюгаты могут приводить к кашлю и одышке за счёт лекарственного поражения лёгких. Любые новые или усиливающиеся симптомы нужно обсуждать с лечащей командой, чтобы вовремя изменить схему и подобрать поддерживающее лечение.
Комплексное исследования во время таргетной терапии
Лабораторные тесты позволяют отслеживать функцию печени и почек, электролитный баланс, свёртывание, признаки воспаления, что критично при длительном приёме таргетных препаратов. ЭКГ и ЭхоКГ используются для контроля сердца, если схема связана с риском кардиотоксичности или тяжёлой гипертензии. КТ, ПЭТ-КТ и эндоскопия показывают, уменьшается ли опухоль, остаётся стабильной или растёт, а также помогают вовремя заметить осложнения в зоне пищевода и других органах. Решения о продолжении, смене или остановке лечения принимаются на основании этих данных вместе с оценкой самочувствия.
Как легче перенести молекулярно-таргетную терапию?
Важно следить за питанием и весом, выбирать мягкую или пюреобразную пищу, использовать рекомендованные высококалорийные смеси и не допускать выраженного похудения. Нельзя самостоятельно менять дозу или полностью отменять назначенные препараты, в том числе сопутствующие средства от давления, боли или изжоги, любые коррекции согласуются с онкологом. Полезно вести краткий дневник симптомов с отметкой боли при глотании, эпизодов рвоты, диареи, температуры, одышки. При появлении крови в рвотных массах или стуле, внезапной сильной слабости, резкой одышки следует обращаться за неотложной помощью, не ожидая планового визита.