- ДИАГНОСТИКА
- МРТ
- КТ
- КТ ГОЛОВЫ
- КТ ШЕИ
- КТ ГРУДНОЙ КЛЕТКИ
- КТ БРЮШНОЙ ПОЛОСТИ
- КТ МАЛОГО ТАЗА
- КТ ПОЗВОНОЧНИКА
- КТ СУСТАВОВ
- КТ КОСТЕЙ
- КТ АНГИОГРАФИЯ
- КТ ЗУБОВ
- УЗИ
- УЗИ ОРГАНОВ МАЛОГО ТАЗА
- УЗИ БРЮШНОЙ ПОЛОСТИ
- УЗИ ЗАБРЮШИННОГО ПРОСТРАНСТВА
- УЗИ СЕРДЦА
- УЗИ СОСУДОВ
- УЗИ МЯГКИХ ТКАНЕЙ, НЕРВОВ И ЖЕЛЕЗ
- УЗИ СУСТАВОВ
- УЗИ ГОЛОВЫ
- УЗИ ЛИМФОУЗЛОВ
- УЗИ ПРИ БЕРЕМЕННОСТИ
- УЗИ ПЛОДА
- УЗИ НОВРОЖДЕННОМУ РЕБЕНКУ
- УЗИ ПОСЛЕ АБОРТА
- РЕНТГЕН
- ВРАЧИ
- КАКОЙ ВРАЧ ЛЕЧИТ
- АКУШЕР-ГИНЕКОЛОГ
- АЛЛЕРГОЛОГ
- ВЕРТЕБРОЛОГ
- ВЕСТИБУЛОЛОГ
- ГАСТРОЭНТЕРОЛОГ
- ГЕМАТОЛОГ
- ГИНЕКОЛОГ
- ДЕРМАТОЛОГ
- ДИЕТОЛОГ
- ИГЛОТЕРАПЕВТ
- ИММУНОЛОГ
- ИНФЕКЦИОНИСТ
- КАРДИОЛОГ
- ВРАЧ ЛЕЧЕБНОЙ ФИЗКУЛЬТУРЫ
- МАММОЛОГ
- НЕВРОЛОГ
- НЕЙРОХИРУРГ
- НЕОНАТОЛОГ
- НЕФРОЛОГ
- ОНКОЛОГ
- ОНКОЛОГ-МАММОЛОГ
- ОРТОПЕД
- ОРТОПЕД-ХИРУРГ
- ОТОЛАРИНГОЛОГ
- ОФТАЛЬМОЛОГ
- ОСТЕОПАТ
- ПЕДИАТР
- ПРОКТОЛОГ
- ПСИХИАТР
- ПСИХОТЕРАПЕВТ
- ПУЛЬМОНОЛОГ
- РЕВМАТОЛОГ
- РЕФЛЕКСОТЕРАПЕВТ
- СЕКСОЛОГ
- СОМНОЛОГ
- СОСУДИСТЫЙ ХИРУРГ
- СПОРТИВНЫЙ ВРАЧ
- ТЕРАПЕВТ
- ТРАВМАТОЛОГ
- ТРИХОЛОГ
- УРОЛОГ
- ФИЗИОТЕРАПЕВТ
- ФЛЕБОЛОГ
- ФТИЗИАТР
- ВРАЧ ФУНКЦИОНАЛЬНОЙ ДИАГНОСТИКИ
- ХИРУРГ
- ЭНДОКРИНОЛОГ
- ЭНДОСКОПИСТ
- ЭПИЛЕПТОЛОГ
- СПОРТИВНЫЙ МАССАЖИСТ
- ГЕПАТОЛОГ
- ПАРАЗИТОЛОГ
- МАНУАЛЬНЫЙ ТЕРАПЕВТ
- СЕМЕЙНЫЙ ПСИХОЛОГ
- ВРАЧ ОБЩЕЙ ПРАКТИКИ
- ПРОФПАТОЛОГ-ТЕРАПЕВТ
- АНДРОЛОГ
- АНГИОЛОГ
- АРИТМОЛОГ
- АРТРОЛОГ
- БРОНХОЛОГ
- ВЕНЕРОЛОГ
- ГЕМОСТАЗИОЛОГ
- ГИРУДОТЕРАПЕВТ
- ДИАБЕТОЛОГ
- КИНЕЗИОЛОГ
- РАДИОТЕРАПЕВТ
- РЕПРОДУКТОЛОГ
- СУРДОЛОГ
- ФОНИАТР
- ХИМИОТЕРАПЕВТ
- СКИДКИ
- НА КАРТЕ
- МРТ РЯДОМ (поиск по району)
- АДМИРАЛТЕЙСКИЙ РАЙОН
- ВАСИЛЕОСТРОВСКИЙ РАЙОН
- ВЫБОРГСКИЙ РАЙОН
- КАЛИНИНСКИЙ РАЙОН
- КИРОВСКИЙ РАЙОН
- КОЛПИНСКИЙ РАЙОН
- КРАСНОГВАРДЕЙСКИЙ РАЙОН
- КРАСНОСЕЛЬСКИЙ РАЙОН
- КРОНШТАДТСКИЙ РАЙОН
- КУРОРТНЫЙ РАЙОН
- МОСКОВСКИЙ РАЙОН
- НЕВСКИЙ РАЙОН
- ПЕТРОГРАДСКИЙ РАЙОН
- ПЕТРОДВОРЦОВЫЙ РАЙОН
- ПРИМОРСКИЙ РАЙОН
- ПУШКИНСКИЙ РАЙОН
- ФРУНЗЕНСКИЙ РАЙОН
- ЦЕНТРАЛЬНЫЙ РАЙОН
- ЛЕН. ОБЛАСТЬ
- КТ и МСКТ РЯДОМ (поиск по району)
- АДМИРАЛТЕЙСКИЙ РАЙОН
- ВАСИЛЕОСТРОВСКИЙ РАЙОН
- ВЫБОРГСКИЙ РАЙОН
- КАЛИНИНСКИЙ РАЙОН
- КИРОВСКИЙ РАЙОН
- КОЛПИНСКИЙ РАЙОН
- КРАСНОГВАРДЕЙСКИЙ РАЙОН
- КРАСНОСЕЛЬСКИЙ РАЙОН
- КРОНШТАДТСКИЙ РАЙОН
- КУРОРТНЫЙ РАЙОН
- МОСКОВСКИЙ РАЙОН
- НЕВСКИЙ РАЙОН
- ПЕТРОГРАДСКИЙ РАЙОН
- ПЕТРОДВОРЦОВЫЙ РАЙОН
- ПРИМОРСКИЙ РАЙОН
- ПУШКИНСКИЙ РАЙОН
- ФРУНЗЕНСКИЙ РАЙОН
- ЦЕНТРАЛЬНЫЙ РАЙОН
- ЛЕН. ОБЛАСТЬ
- МРТ АДРЕСА БОЛЬНИЦ В СПБ
- МРТ РЯДОМ (поиск по району)
Адреса онкоцентров для лечения рака пищевода в СПБ


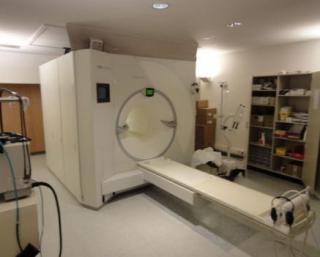
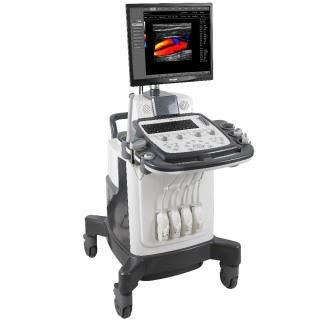
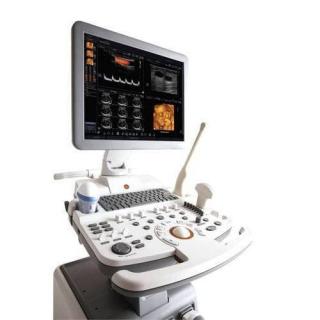
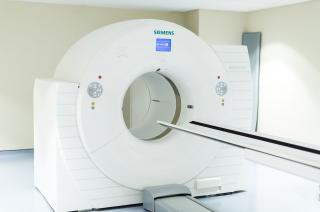
Услуга лечения онкологии
Услуга лечебного сопровождения для пациентов с онкологией — это индивидуальная комплексная помощь, которая может включать:
 Лучшиие онкологидоступ к ведущим специалистам Санкт-Петербурга, которые подберут современные схемы терапии и проконтролируют эффективность лечения на каждом этапе.
Лучшиие онкологидоступ к ведущим специалистам Санкт-Петербурга, которые подберут современные схемы терапии и проконтролируют эффективность лечения на каждом этапе. Госпитализация или дневной стационарвозможность пройти лечение в комфортных условиях ведущих онкологических центров Санкт-Петербурга.
Госпитализация или дневной стационарвозможность пройти лечение в комфортных условиях ведущих онкологических центров Санкт-Петербурга. Персональный протокол леченияразработка индивидуальной стратегии терапии с учётом типа опухоли, стадии заболевания, генетических особенностей, сопутствующих состояний и истории предыдущего лечения.
Персональный протокол леченияразработка индивидуальной стратегии терапии с учётом типа опухоли, стадии заболевания, генетических особенностей, сопутствующих состояний и истории предыдущего лечения. Второе независимое мнениеэкспертная оценка диагноза и лечебной тактики от ведущих онкологов, позволяющая подтвердить правильность выбранной стратегии, получить дополнительные варианты терапии, избежать ошибок и повысить шансы на успешный результат благодаря объективному профессиональному взгляду стороннего специалиста.
Второе независимое мнениеэкспертная оценка диагноза и лечебной тактики от ведущих онкологов, позволяющая подтвердить правильность выбранной стратегии, получить дополнительные варианты терапии, избежать ошибок и повысить шансы на успешный результат благодаря объективному профессиональному взгляду стороннего специалиста.
Лучшие специалисты в Санкт-Петербурге с рейтингом 4.5+
Последние отзывы
Что такое рак пищевода?
Под этим диагнозом понимается злокачественная опухоль, исходящая из клеток слизистой или подслизистых структур стенки пищевода, которая нарушает прохождение пищи, может распространяться на прилежащие органы и давать метастазы в лимфатические узлы и отдалённые органы, при этом от локализации, глубины прорастания, наличия поражённых узлов и общего состояния организма зависят возможные варианты лечения, его объём и прогноз.
Варианты протоколов лечения рака пищевода
Хирургическое лечение включает различные виды эзофагэктомии с формированием пищеводного заместителя из желудка, тонкой или толстой кишки, при этом по данным эндоскопии, компьютерной и эндоскопической ультрасонографии оценивается глубина инвазии и поражение лимфатических узлов, выбирается трансторакальный или трансхиатальный доступ, определяется объём лимфодиссекции, детально планируется линия пересечения пищевода и желудка, метод формирования анастомоза и его уровень, заранее рассчитывается необходимость наложения питающей еюностомы, а в послеоперационном периоде проводится строгий контроль за состоятельностью анастомоза, дыхательной функцией и нутритивным статусом.
Эндоскопическое лечение применяется на ранних стадиях при ограниченном поражении слизистой и подслизистого слоя, включает эндоскопическую резекцию слизистой и диссекцию в подслизистом слое, при которых под визуальным контролем выполняется разметка границ, послойное поднятие поражённого участка раствором, циркулярный или сегментарный разрез слизистой, выделение блока ткани единым фрагментом и тщательный гемостаз, а в дальнейшем обеспечивается эндоскопическое наблюдение за зоной вмешательства, контроль за рубцеванием и раннее выявление рецидива или метахронных очагов.
Комбинированное химиолучевое лечение используется как самостоятельный радикальный метод или в неоадъювантном режиме перед операцией, предполагает последовательное или одновременное проведение лучевой терапии с системным введением цитостатиков или препаратов таргетного действия, при планировании по данным компьютерной томографии формируется объём облучения с включением первичного очага и регионарных лимфатических узлов, рассчитываются суммарная доза и режим фракционирования, подбираются схемы лекарственной терапии с учётом функции органов и сопутствующей патологии, а в процессе лечения проводится регулярный контроль за выраженностью эзофагита, миелосупрессии и других осложнений с возможной коррекцией доз и режимов.
Лучевая терапия как самостоятельный метод применяется при невозможности хирургического вмешательства или отказе от операции, а также в паллиативных целях для уменьшения дисфагии и болевого синдрома, включает использование трёхмерно-конформных и интенсивно-модулированных методик, при которых по данным томографии задаются объёмы мишени и критических органов, рассчитываются поля, углы и режим фракционирования, проводится ежедневный контроль позиционирования, оценивается динамика симптомов и ответ опухоли, а при необходимости корректируются параметры плана для сохранения эффективности при допустимой токсичности.
Системная лекарственная терапия применяется при местно-распространённых и метастатических формах, включает схемы на основе производных платины, фторпиримидинов и других цитостатиков, а также при наличии показаний добавление таргетных и иммуноонкологических препаратов, при выборе режима учитываются морфологический вариант опухоли, общее состояние и сопутствующие заболевания, проводится расчёт доз по площади поверхности тела, определяются интервалы между циклами, организуется регулярный лабораторный и инструментальный контроль за токсичностью и эффектом, а при непереносимости или прогрессировании пересматриваются комбинации и последовательность линий терапии.
Паллиативные вмешательства при дисфагии включают эндоскопическое стентирование пищевода, дилатацию стриктур, лазерную или аргоноплазменную коагуляцию опухолевой ткани, наложение гастростомы или еюностомы для обеспечения адекватного питания, при этом по данным эндоскопии и рентгенологического исследования определяется уровень и протяжённость сужения, подбирается диаметр и длина стента, контролируется его раскрытие и положение, оценивается риск аспирации и боли, а при использовании питательных стом формируется индивидуальный план нутритивной поддержки в сочетании с продолжающимся противоопухолевым лечением.
Помощь онкобольным при лечении рака пищевода
Обезболивающая терапия направлена на купирование болевого синдрома, связанного с инвазией опухоли, воспалением слизистой, осложнениями со стороны плевры и позвоночника, а также последствиями хирургических и лучевых вмешательств, включает ступенчатое применение ненаркотических анальгетиков, слабых и сильных опиоидов, использование адъювантных средств при нейропатической боли, подбор формы введения от пероральной до парентеральной и трансдермальной, регулярную оценку интенсивности боли и побочных эффектов, коррекцию схем при прорывной боли, а при необходимости применение интервенционных методик, таких как нейролиз или эпидуральные инфузии.
Противорвотная терапия и коррекция диспепсических нарушений проводятся на фоне системной химиотерапии, лучевого лечения и выраженной дисфагии, включают профилактическое назначение антагонистов серотониновых и нейрокининовых рецепторов, глюкокортикоидов и других препаратов перед введением цитостатиков, сочетание нескольких классов средств при высокоэметогенных схемах, коррекцию терапии при прорывной тошноте и рвоте, дополнительно использование прокинетиков и препаратов для снижения кислотности при изжоге и рефлюксе, а также обязательный контроль водно-электролитного баланса и массы тела с прицельной инфузионной поддержкой при риске дегидратации.
Нутритивная поддержка имеет ключевое значение из-за выраженной дисфагии и потери массы тела, включает оценку нутритивного статуса и энергетических потребностей, подбор текстуры пищи и специальных высокобелковых и высококалорийных смесей для перорального приёма, при невозможности достаточного питания — организацию зондового питания через назогастральный зонд или через гастростому, а при тяжёлых нарушениях глотания и высоком риске аспирации — переход на парентеральное питание с поэтапным наращиванием объёма, регулярный контроль белковых фракций, микроэлементов и гликемии, а также тесное взаимодействие с диетологом для корректировки схем по мере изменения состояния.
Поддержка при нарушении глотания и профилактика аспирации проводится совместно с логопедом и специалистом по реабилитации, включает обучение безопасным позам и техникам глотания, подбор консистенции пищи с загустителями, использование специальных столовых приборов и режимов питания малыми порциями, оценку степени нарушения по шкалам и при необходимости принятие решения о временном или постоянном переходе на зондовое или стомическое питание, а также своевременное выявление признаков аспирации, таких как приступы кашля, хрипы, частые пневмонии, с последующей коррекцией тактики для снижения риска серьёзных респираторных осложнений.
Коррекция гематологических нарушений и тромбопрофилактика необходимы в связи с частой анемией, лейкопенией и тромбоцитопенией на фоне системной терапии, а также повышенным риском венозных тромбозов из-за малоподвижности и опухолевого процесса, включает использование препаратов железа, витамина B12 и фолиевой кислоты, при показаниях — трансфузии эритроцитарной массы и тромбоцитарных концентратов, динамический контроль коагулограммы, назначение антикоагулянтов для профилактики тромбозов с учётом риска кровотечения из опухоли и язвенных дефектов, а также коррекцию доз химиопрепаратов при выраженной миелосупрессии для сохранения баланса между эффективностью лечения и безопасностью.
Психологическая и паллиативная поддержка направлены на снижение выраженной тревоги, депрессивных реакций и страха удушья, которые характерны для пациентов с поражением пищевода, включают работу психоонколога с обсуждением целей и этапов лечения, обучение методам самопомощи и управления дыханием, участие семьи в планировании ухода, раннее подключение паллиативной службы для организации контроля боли, одышки, слабости и других симптомов на дому или в стационаре, а также регулярный пересмотр тактики лечения с учётом качества жизни, предпочтений пациента и реальной эффективности проводимых активных вмешательств.
Какие врачи могут быть вовлечены
- Хирург-онколог (торакальный или абдоминальный) оценивает резектабельность опухоли по данным эндоскопии, компьютерной и эндоскопической ультрасонографии, определяет показания к эзофагэктомии и объём вмешательства, выбирает доступ и вид реконструкции пищевода с формированием заместителя из желудка или кишечника, рассчитывает объём лимфодиссекции, планирует необходимость наложения питающей еюностомы, выполняет операцию с контролем кровопотери и состоятельности анастомозов, ведёт послеоперационный период и взаимодействует с онкологом по вопросам дальнейшей химиолучевой терапии.
- Эндоскопист выполняет диагностическую эзофагогастродуоденоскопию с прицельной биопсией, определяет протяжённость и характер поражения, участвует в стадировании вместе с онкологом и хирургом, проводит лечебные манипуляции при стриктурах и дисфагии, такие как стентирование, баллонная дилатация, лазерная или аргоноплазменная коагуляция опухолевой ткани, контролирует состояние просвета пищевода в динамике, оценивает эффективность проведённых вмешательств и при необходимости планирует повторные процедуры.
- Лучевой терапевт по данным компьютерной томографии, эндоскопии и, при необходимости, позитронно-эмиссионной томографии формирует объём мишени и критических органов, совместно с медицинским физиком рассчитывает суммарную дозу и режим фракционирования, подбирает трёхмерно-конформные или интенсивно-модулированные методики, контролирует точность позиционирования и переносимость облучения, оценивает выраженность лучевого эзофагита и других осложнений, а также анализирует ответ опухоли по результатам контрольных обследований, участвуя в решении о продолжении или изменении плана лечения.
- Гастроэнтеролог и диетолог оценивают выраженность дисфагии, нутритивный статус и сопутствующие заболевания желудочно-кишечного тракта, подбирают диету с учётом степени нарушения глотания, рекомендуют консистенцию пищи и объём приёма, участвуют в принятии решения о зондовом или стомическом питании, контролируют динамику массы тела, белково-энергетический баланс и переносимость нутритивной поддержки на фоне химиолучевого или хирургического лечения, своевременно корректируя схемы.
- Анестезиолог-реаниматолог проводит предоперационную оценку риска с учётом функции дыхательной и сердечно-сосудистой систем, состояния лёгких, уровня гемоглобина и других показателей, выбирает оптимальную схему анестезии и обезболивания для длительных торакальных и абдоминальных вмешательств, контролирует дыхание и гемодинамику во время операции, обеспечивает послеоперационное наблюдение в отделении реанимации, занимается профилактикой дыхательной недостаточности, тромбоэмболических и инфекционных осложнений, а также участвует в интенсивной терапии при тяжёлом течении заболевания.
- Врач паллиативной помощи и психоонколог помогают справляться с болью, выраженной дисфагией, страхом удушья и тревогой, подбирают комплекс обезболивающих, противорвотных и успокаивающих средств, организуют паллиативное наблюдение на дому или в стационаре, обучают пациента и семью принципам контроля симптомов и безопасного питания, обсуждают цели лечения и возможные изменения тактики на разных этапах, чтобы максимально сохранить качество жизни и сделать прогнозируемыми дальнейшие шаги.
Какие обследования назначаются
- Компьютерная томография пищевода с контрастированием используется для оценки протяжённости опухоли за пределами стенки пищевода, выявления увеличенных лимфатических узлов средостения и брюшной полости, поиска отдалённых метастазов в лёгких, печени, надпочечниках и костях, уточнения отношения опухоли к трахее, аорте и другим крупным сосудам, а также для планирования объёма хирургического вмешательства или химиолучевого лечения и последующего контроля его результатов.
- Позитронно-эмиссионная томография, совмещённая с компьютерной томографией, применяется для оценки метаболической активности опухоли и лимфатических узлов, поиска скрытых отдалённых метастазов, уточнения стадии при спорных данных других исследований, помогает отличить рубцовые изменения после лечения от жизнеспособной опухолевой ткани, используется для оценки ответа на химиолучевую терапию и принятия решения о целесообразности радикальной операции или изменении системной терапии.
- Эзофагогастродуоденоскопия с биопсией является ключевым методом диагностики, позволяет визуально оценить локализацию, протяжённость и характер роста опухоли, выявить сопутствующие поражения слизистой желудка и двенадцатиперстной кишки, выполнить прицельный забор нескольких фрагментов ткани для гистологического и иммуногистохимического исследования, что необходимо для точного подтверждения диагноза, уточнения типа опухоли и подбора лекарственного лечения, а также служит основой для планирования эндоскопических и паллиативных вмешательств.
- Эндоскопическое ультразвуковое исследование пищевода используется для оценки глубины инвазии опухоли в стенку, состояния регионарных лимфатических узлов и соседних структур, выполняется с введением специального ультразвукового зонда через эндоскоп, позволяет отличить поверхностные поражения от более глубоко проникающих, что критически важно при выборе между эндоскопическим лечением и радикальной хирургией, а также служит ориентиром при формировании объёма облучения.
- Магнитно-резонансная томография пищевода с контрастом проводится при необходимости более детальной оценки мягкотканых структур, вовлечения трахеи, крупных сосудов, позвоночника и нервных элементов, помогает уточнить распространённость процесса при опухолях верхнегрудного и шейного отделов пищевода, дополняет данные компьютерной томографии и влияет на решение о технической возможности и объёме хирургического вмешательства, а также на выбор режима лучевой терапии.
- Лабораторные и функциональные исследования включают общий и биохимический анализ крови с оценкой функции печени и почек, уровня белка и электролитов, коагулограмму, определение маркёров воспаления, а также спирометрию, электрокардиографию и при необходимости эхокардиографию, что позволяет оценить готовность дыхательной и сердечно-сосудистой систем к операции или химиолучевой терапии, подобрать безопасные схемы лечения и вовремя скорректировать сопутствующую терапию при выявлении отклонений.
Что важно знать пациентам
Почему схемы лечения различаются у разных пациентов?
На выбор между операцией, химиолучевым лечением, комбинированным или паллиативным подходом влияет не только стадия и локализация опухоли, но и возраст, функция сердца и лёгких, выраженность потери массы тела, наличие других серьёзных заболеваний, степень дисфагии и переносимость лекарственных препаратов, поэтому одному пациенту может быть предложена радикальная операция после курса химиолучевой терапии, другому — только химиолучевое лечение, а третьему — преимущественно паллиативные вмешательства для облегчения глотания и контроля симптомов.
Что сделать, чтобы повысить эффективность онколечения?
Важно полностью отказаться от курения и алкоголя, строго соблюдать рекомендации по питанию с учётом степени дисфагии, подбирать консистенцию пищи по совету врача и диетолога, не пропускать приём назначенных лекарств, приходить на все запланированные процедуры и обследования, сообщать врачу о любых новых симптомах, поддерживать посильную физическую активность и режим отдыха, так как сохранение нутритивного статуса, функции дыхания и общего тонуса организма помогает легче переносить химиолучевую терапию и операции и снижает риск осложнений.
Какие осложнения возможны?
Особую настороженность должны вызывать резкое ухудшение глотания, невозможность проглотить даже жидкость, появление или усиление болей за грудиной, кашель с кровью или рвота с примесью крови, чёрный стул, выраженная одышка, высокая температура с ознобом, резкая слабость, головокружение и обмороки, а также появление сильных болей в ногах или отёка конечности, при таких проявлениях нужно сразу связаться с лечащим врачом или службой неотложной помощи.
Что делать после онкотерапии?
Такая тактика позволяет на каждом этапе уточнять распространённость процесса, оценивать ответ на химиолучевую или хирургическую терапию, вовремя выявлять осложнения и корректировать лечение, при этом онколог, хирург, лучевой терапевт, анестезиолог, диетолог и врач паллиативной помощи дополняют друг друга, отвечая каждый за свой участок, а регулярные осмотры, анализы и инструментальные исследования дают возможность заранее увидеть неблагоприятные изменения, изменить схему лечения и тем самым повысить шансы на длительный контроль заболевания и сохранение максимально возможного качества жизни.