- ДИАГНОСТИКА
- МРТ
- КТ
- КТ ГОЛОВЫ
- КТ ШЕИ
- КТ ГРУДНОЙ КЛЕТКИ
- КТ БРЮШНОЙ ПОЛОСТИ
- КТ МАЛОГО ТАЗА
- КТ ПОЗВОНОЧНИКА
- КТ СУСТАВОВ
- КТ КОСТЕЙ
- КТ АНГИОГРАФИЯ
- КТ ЗУБОВ
- УЗИ
- УЗИ ОРГАНОВ МАЛОГО ТАЗА
- УЗИ БРЮШНОЙ ПОЛОСТИ
- УЗИ ЗАБРЮШИННОГО ПРОСТРАНСТВА
- УЗИ СЕРДЦА
- УЗИ СОСУДОВ
- УЗИ МЯГКИХ ТКАНЕЙ, НЕРВОВ И ЖЕЛЕЗ
- УЗИ СУСТАВОВ
- УЗИ ГОЛОВЫ
- УЗИ ЛИМФОУЗЛОВ
- УЗИ ПРИ БЕРЕМЕННОСТИ
- УЗИ ПЛОДА
- УЗИ НОВРОЖДЕННОМУ РЕБЕНКУ
- УЗИ ПОСЛЕ АБОРТА
- РЕНТГЕН
- ВРАЧИ
- КАКОЙ ВРАЧ ЛЕЧИТ
- АКУШЕР-ГИНЕКОЛОГ
- АЛЛЕРГОЛОГ
- ВЕРТЕБРОЛОГ
- ВЕСТИБУЛОЛОГ
- ГАСТРОЭНТЕРОЛОГ
- ГЕМАТОЛОГ
- ГИНЕКОЛОГ
- ДЕРМАТОЛОГ
- ДИЕТОЛОГ
- ИГЛОТЕРАПЕВТ
- ИММУНОЛОГ
- ИНФЕКЦИОНИСТ
- КАРДИОЛОГ
- ВРАЧ ЛЕЧЕБНОЙ ФИЗКУЛЬТУРЫ
- МАММОЛОГ
- НЕВРОЛОГ
- НЕЙРОХИРУРГ
- НЕОНАТОЛОГ
- НЕФРОЛОГ
- ОНКОЛОГ
- ОНКОЛОГ-МАММОЛОГ
- ОРТОПЕД
- ОРТОПЕД-ХИРУРГ
- ОТОЛАРИНГОЛОГ
- ОФТАЛЬМОЛОГ
- ОСТЕОПАТ
- ПЕДИАТР
- ПРОКТОЛОГ
- ПСИХИАТР
- ПСИХОТЕРАПЕВТ
- ПУЛЬМОНОЛОГ
- РЕВМАТОЛОГ
- РЕФЛЕКСОТЕРАПЕВТ
- СЕКСОЛОГ
- СОМНОЛОГ
- СОСУДИСТЫЙ ХИРУРГ
- СПОРТИВНЫЙ ВРАЧ
- ТЕРАПЕВТ
- ТРАВМАТОЛОГ
- ТРИХОЛОГ
- УРОЛОГ
- ФИЗИОТЕРАПЕВТ
- ФЛЕБОЛОГ
- ФТИЗИАТР
- ВРАЧ ФУНКЦИОНАЛЬНОЙ ДИАГНОСТИКИ
- ХИРУРГ
- ЭНДОКРИНОЛОГ
- ЭНДОСКОПИСТ
- ЭПИЛЕПТОЛОГ
- СПОРТИВНЫЙ МАССАЖИСТ
- ГЕПАТОЛОГ
- ПАРАЗИТОЛОГ
- МАНУАЛЬНЫЙ ТЕРАПЕВТ
- СЕМЕЙНЫЙ ПСИХОЛОГ
- ВРАЧ ОБЩЕЙ ПРАКТИКИ
- ПРОФПАТОЛОГ-ТЕРАПЕВТ
- АНДРОЛОГ
- АНГИОЛОГ
- АРИТМОЛОГ
- АРТРОЛОГ
- БРОНХОЛОГ
- ВЕНЕРОЛОГ
- ГЕМОСТАЗИОЛОГ
- ГИРУДОТЕРАПЕВТ
- ДИАБЕТОЛОГ
- КИНЕЗИОЛОГ
- РАДИОТЕРАПЕВТ
- РЕПРОДУКТОЛОГ
- СУРДОЛОГ
- ФОНИАТР
- ХИМИОТЕРАПЕВТ
- СКИДКИ
- НА КАРТЕ
- МРТ РЯДОМ (поиск по району)
- АДМИРАЛТЕЙСКИЙ РАЙОН
- ВАСИЛЕОСТРОВСКИЙ РАЙОН
- ВЫБОРГСКИЙ РАЙОН
- КАЛИНИНСКИЙ РАЙОН
- КИРОВСКИЙ РАЙОН
- КОЛПИНСКИЙ РАЙОН
- КРАСНОГВАРДЕЙСКИЙ РАЙОН
- КРАСНОСЕЛЬСКИЙ РАЙОН
- КРОНШТАДТСКИЙ РАЙОН
- КУРОРТНЫЙ РАЙОН
- МОСКОВСКИЙ РАЙОН
- НЕВСКИЙ РАЙОН
- ПЕТРОГРАДСКИЙ РАЙОН
- ПЕТРОДВОРЦОВЫЙ РАЙОН
- ПРИМОРСКИЙ РАЙОН
- ПУШКИНСКИЙ РАЙОН
- ФРУНЗЕНСКИЙ РАЙОН
- ЦЕНТРАЛЬНЫЙ РАЙОН
- ЛЕН. ОБЛАСТЬ
- КТ и МСКТ РЯДОМ (поиск по району)
- АДМИРАЛТЕЙСКИЙ РАЙОН
- ВАСИЛЕОСТРОВСКИЙ РАЙОН
- ВЫБОРГСКИЙ РАЙОН
- КАЛИНИНСКИЙ РАЙОН
- КИРОВСКИЙ РАЙОН
- КОЛПИНСКИЙ РАЙОН
- КРАСНОГВАРДЕЙСКИЙ РАЙОН
- КРАСНОСЕЛЬСКИЙ РАЙОН
- КРОНШТАДТСКИЙ РАЙОН
- КУРОРТНЫЙ РАЙОН
- МОСКОВСКИЙ РАЙОН
- НЕВСКИЙ РАЙОН
- ПЕТРОГРАДСКИЙ РАЙОН
- ПЕТРОДВОРЦОВЫЙ РАЙОН
- ПРИМОРСКИЙ РАЙОН
- ПУШКИНСКИЙ РАЙОН
- ФРУНЗЕНСКИЙ РАЙОН
- ЦЕНТРАЛЬНЫЙ РАЙОН
- ЛЕН. ОБЛАСТЬ
- МРТ АДРЕСА БОЛЬНИЦ В СПБ
- МРТ РЯДОМ (поиск по району)
Адреса онкоцентров для терапии аденокарциномы пищевода в СПБ
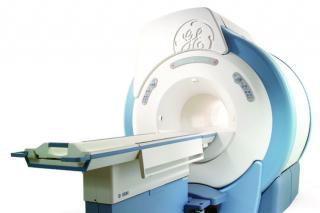
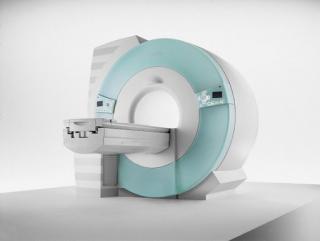
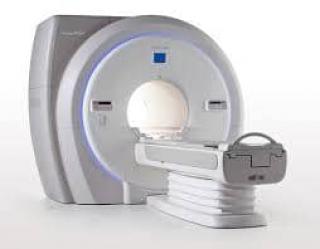
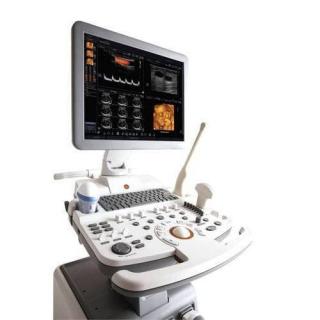
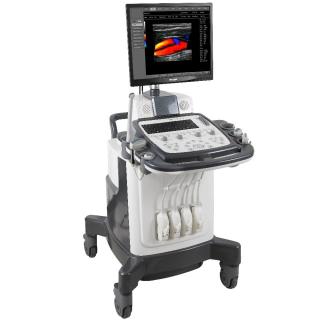
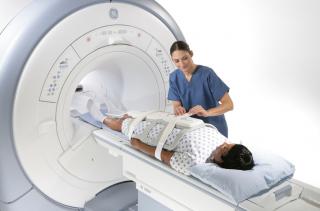
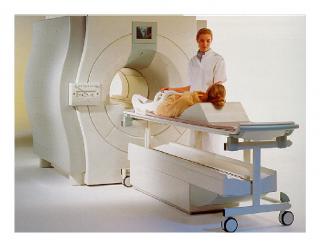
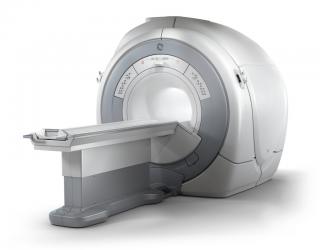
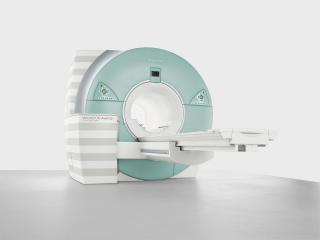
Услуга лечения онкологии
Услуга лечебного сопровождения для пациентов с онкологией — это индивидуальная комплексная помощь, которая может включать:
 Лучшиие онкологидоступ к ведущим специалистам Санкт-Петербурга, которые подберут современные схемы терапии и проконтролируют эффективность лечения на каждом этапе.
Лучшиие онкологидоступ к ведущим специалистам Санкт-Петербурга, которые подберут современные схемы терапии и проконтролируют эффективность лечения на каждом этапе. Госпитализация или дневной стационарвозможность пройти лечение в комфортных условиях ведущих онкологических центров Санкт-Петербурга.
Госпитализация или дневной стационарвозможность пройти лечение в комфортных условиях ведущих онкологических центров Санкт-Петербурга. Персональный протокол леченияразработка индивидуальной стратегии терапии с учётом типа опухоли, стадии заболевания, генетических особенностей, сопутствующих состояний и истории предыдущего лечения.
Персональный протокол леченияразработка индивидуальной стратегии терапии с учётом типа опухоли, стадии заболевания, генетических особенностей, сопутствующих состояний и истории предыдущего лечения. Второе независимое мнениеэкспертная оценка диагноза и лечебной тактики от ведущих онкологов, позволяющая подтвердить правильность выбранной стратегии, получить дополнительные варианты терапии, избежать ошибок и повысить шансы на успешный результат благодаря объективному профессиональному взгляду стороннего специалиста.
Второе независимое мнениеэкспертная оценка диагноза и лечебной тактики от ведущих онкологов, позволяющая подтвердить правильность выбранной стратегии, получить дополнительные варианты терапии, избежать ошибок и повысить шансы на успешный результат благодаря объективному профессиональному взгляду стороннего специалиста.
Лучшие специалисты в Санкт-Петербурге с рейтингом 4.5+
Последние отзывы
Что такое аденокарцинома пищевода?
Аденокарцинома пищевода представляет собой злокачественную опухоль железистого происхождения, чаще возникающую в нижней трети пищевода и зоне перехода в желудок на фоне длительного рефлюкса и хронического воспаления, по мере роста образование сужает просвет, затрудняет прохождение пищи, может разрушать стенку, вызывать кровотечения и распространяться на лимфоузлы, лёгкие, печень и другие органы, поэтому появление стойкой дисфагии, боли или жжения за грудиной, непреднамеренного похудания и эпизодов рвоты с примесью крови требует не только приёма антацидов, а полноценного обследования с эндоскопией и биопсией.
Протоколы лечения аденокарциномы пищевода
Трансторакальная эзофагэктомия по типу Ивора Льюиса применяется при опухолях средней и нижней трети грудного отдела пищевода, по данным эндоскопии, КТ, МРТ и ПЭТ-КТ уточняется длина поражения, глубина инвазии и статус средостенных лимфоузлов, в ходе вмешательства выполняется лапаротомный или лапароскопический этап с мобилизацией желудка и формированием желудочной трубки, затем через торакотомию удаляется грудной отдел пищевода с регионарной клетчаткой и лимфоузлами, формируется внутригрудной эзофагогастроанастомоз, тщательно дренируется плевральная полость, после чего в реанимации проводится строгий контроль дыхания, гемодинамики и раннего выявления несостоятельности швов.
Трёхпольная эзофагэктомия по типу МакКьюна применяется при более протяжённых аденокарциномах и при высоком расположении верхнего края опухоли, выполняются абдоминальный, торакальный и шейный доступы, последовательно мобилизуются желудок и пищевод до шейного отдела, удаляется единый блок тканей с медиастинальными и верхними брюшными лимфоузлами, формируется шейный эзофагогастроанастомоз, подобный протокол обеспечивает расширенную лимфодиссекцию и возможность отступить на большее расстояние от опухоли проксимально, однако требует особо внимательного послеоперационного наблюдения за дыхательной функцией и состоянием шейного анастомоза.
Трансхиатальная эзофагэктомия используется при дистальных аденокарциномах без выраженного вовлечения средостенных структур, хирург через лапаротомию и разрез на шее мобилизует пищевод тупо через диафрагмальное отверстие, удаляет поражённый сегмент с абдоминальными лимфоузлами и формирует шейный эзофагогастроанастомоз, методика позволяет избежать торакотомии, уменьшить травму грудной клетки и снизить риск тяжёлых лёгочных осложнений, при этом радикальность вмешательства оценивается по результатам морфологии и количеству удалённых лимфоузлов.
Резекция дистального пищевода и проксимальной части желудка с реконструкцией по типу эзофагогастроанастомоза или эзофагоеюнального анастомоза применяется при аденокарциномах зоны пищеводно-желудочного перехода, по данным эндоскопии и визуализирующих методов оценивается степень вовлечения кардиального отдела желудка и поддиафрагмальных лимфоузлов, во время операции удаляется дистальный пищевод, кардиальная зона и часть желудка с регионарной клетчаткой, затем создаётся анастомоз с оставшимся желудком или петлёй тонкой кишки, выбирается такой вариант реконструкции, который обеспечивает адекватный просвет и минимизирует риск выраженного рефлюкса.
Эндоскопическая резекция слизистой или подслизистая диссекция включается в протокол при ранней аденокарциноме пищевода, ограниченной слизистым или поверхностными подслизистыми слоями без признаков поражения лимфоузлов, во время вмешательства под эндоскопическим контролем выполняется приподнятие очага инъекциями, затем послойное иссечение образования с захватом подлежащих структур, препарат извлекается целиком для детального морфологического анализа, при подтверждении полного удаления в пределах здоровых тканей и благоприятных факторов риска удаётся избежать большой резекции, при неблагоприятных признаках пациент переводится на стандартный хирургический или комбинированный протокол.
Неоадъювантная химиолучевая терапия с последующей эзофагэктомией применяется при местнораспространённых аденокарциномах без отдалённых метастазов, по КТ и ПЭТ-КТ оценивается глубина инвазии и статус лимфоузлов, выполняется курс сочетанного облучения области пищевода и средостения с одновременным введением цитостатиков, после завершения выдерживается интервал для регресса опухоли, затем выполняется резекция по одному из радикальных вариантов, степень патологического ответа по операционному материалу используется как важный прогностический признак и фактор при выборе последующей системной терапии.
Периперационная химиотерапия при аденокарциномах пищеводно-желудочного перехода включается в протокол при опухолях с вовлечением кардиальной зоны и поддиафрагмальных лимфоузлов, до операции проводится несколько циклов системного лечения, направленного на уменьшение объёма опухолевой массы и микрометастатического процесса, после резекции и реконструкции курс продолжается до полной запланированной длительности, режимы подбираются с учётом функции печени и почек, переносимости и морфологических факторов риска.
Дефинитивная химиолучевая терапия применяется при нерезектабельных аденокарциномах пищевода, тяжёлой сопутствующей патологии или отказе от операции, планируется облучение первичного очага и регионарных лимфоузлов с подведением дозы, способной обеспечить локальный контроль, параллельно назначаются цитостатики в сенсибилизирующих дозах или в полноценных схемах, динамика оценивается по клинической картине, эндоскопии и КТ, при хорошей переносимости и ограниченном объёме остаточной опухоли иногда обсуждается спасительная резекция.
Паллиативные эндоскопические вмешательства при неоперабельной аденокарциноме пищевода включают стентирование опухолевого стеноза, лазерную или термическую реканализацию просвета и внутриполостную брахитерапию, при выраженной дисфагии под эндоскопическим и рентгенологическим контролем устанавливается саморасправляющийся стент, который расширяет сужение и позволяет принимать пищу через рот, локальное лучевое воздействие уменьшает объём опухолевой массы и кровоточивость, такие меры не устраняют заболевание, но значительно улучшают качество жизни и облегчают нутритивную поддержку.
Системная терапия метастатической аденокарциномы пищевода включает линии химиотерапии, таргетной терапии и иммунотерапии в зависимости от морфологического и молекулярного профиля, по результатам иммуногистохимии и дополнительных тестов оценивается экспрессия ключевых мишеней и уровень иммунной активности, подбираются комбинации цитостатиков и таргетных либо иммунных препаратов, лечение выполняется циклами с регулярной оценкой по КТ и клиническим симптомам, при ограниченном числе метастатических очагов обсуждаются дополнительные локальные вмешательства в сочетании с продолжающейся системной программой.
Помощь онкобольным
Нутритивная поддержка и коррекция дисфагии занимают центральное место в сопроводительной терапии, так как нарушение прохождения пищи по пищеводу приводит к быстрому истощению, сначала оценивается степень дисфагии, возможность приёма мягкой или жидкой пищи, при сохранённом просвете подбирается дробное питание с высокой энергетической плотностью и изменённой консистенцией, при критическом сужении или длительном курсе химиолучевой терапии рассматривается установка назоинтестинального зонда или наложение гастростомы либо еюностомы, через которые вводятся специальные смеси, параллельно обучается техника безопасного глотания, подбирается положение тела во время приёма пищи и после него, что снижает риск аспирации и позволяет поддерживать массу тела на допустимом уровне.
Лечение болевого синдрома учитывает ретростернальную, межлопаточную и надчревную локализацию боли, возникающей как из-за опухолевого процесса, так и после крупных резекций и химиолучевого воздействия, на ранних этапах используются противовоспалительные и комбинированные анальгетики с оценкой влияния на слизистую желудка и свёртывание, при усилении боли строится ступенчатая схема с постепенным добавлением средств центрального действия в удобных формах, для жгучих и стреляющих ощущений назначаются препараты, влияющие на нейропатический компонент, при выраженном локальном болевом очаге в зоне метастаза или остаточной опухоли рассматривается прицельное облучение или малоинвазивная блокада нервных структур, что уменьшает потребность в высоких дозах системных анальгетиков.
Коррекция воспалительных поражений слизистой пищевода и ротовой полости проводится при лучевом эзофагите и мукозите, которые развиваются на фоне химиолучевой терапии, назначаются местные анестезирующие растворы и гели для полоскания и обработки, препараты, образующие защитную плёнку на слизистой, мягкие противовоспалительные средства, даются рекомендации по отказу от горячей, грубой и кислой пищи, ограничивается приём раздражающих напитков, при выраженных эрозивных изменениях и болевом синдроме схема дополняется системными анальгетиками и препаратами, снижающими кислотность желудочного сока, что уменьшает заброс агрессивного содержимого на воспалённую слизистую.
Поддержка при тошноте, рвоте и нарушениях моторики верхних отделов пищеварительного тракта выстраивается с учётом причин, связанных с химиотерапией, облучением или механическим препятствием, до каждого цикла лекарственного лечения назначается противорвотное средство с центральным механизмом действия в конкретной дозировке и режиме приёма, при чувстве переполнения и застое пищи подключаются препараты, улучшающие эвакуацию из желудка и двенадцатиперстной кишки, рацион дробится на небольшие порции, усиливается контроль запахов и продуктов, провоцирующих приступы, в межкурсовой период при необходимости используются дополнительные мягкие средства, подобранные по индивидуальной реакции, что позволяет снизить частоту эпизодов рвоты и сохранить возможность питания.
Коррекция водно-электролитных нарушений и обезвоживания проводится при сочетании дисфагии, рвоты и поноса, часто возникающего на фоне системной терапии, регулярно контролируются уровни натрия, калия, хлоридов, креатинина и показатели кислотно-щелочного состояния, при умеренных отклонениях даются растворы для питья с заданным содержанием солей и рекомендации по распределению объёма жидкости в течение дня, при выраженном дефиците и невозможности приёма достаточного количества через рот назначается внутривенная инфузионная терапия с расчётом суточной потребности и корректировкой по динамике, такая поддержка предотвращает ухудшение функции почек и сердечно-сосудистой системы и улучшает переносимость химиолучевого лечения.
Терапия анемии и дефицита железа необходима при хронических микро- и макрокровопотерях из опухоли и после крупных операций, по анализам оценивается уровень гемоглобина, ферритина и других показателей, при подтверждённом дефиците железа выбирается форма препарата для приёма внутрь или внутривенного введения, при выраженной анемии и симптомах кислородной недостаточности выполняются переливания эритроцитарной массы, одновременно проводится эндоскопический и хирургический контроль источника кровотечения, коррекция анемии повышает толерантность к физической нагрузке, уменьшает одышку и позволяет проводить системную терапию без лишних отсрочек.
Профилактика и лечение инфекционных осложнений направлены на предупреждение и своевременное выявление аспирационной пневмонии, медиастинита, инфекций в зоне стентов и анастомозов, пациенты обучаются признакам дыхательной недостаточности, усиления кашля и повышения температуры, при появлении таких симптомов выполняется рентгенография или КТ органов грудной клетки и лабораторная диагностика, стартует эмпирическая антибактериальная терапия с последующей корректировкой по результатам посевов, при подозрении на несостоятельность анастомоза или осложнение стентирования выполняется экстренное эндоскопическое или хирургическое обследование, своевременное вмешательство снижает риск генерализации инфекции и тяжёлых гнойно-септических последствий.
Профилактика тромбоэмболических осложнений включается в план лечения с учётом высокой тромбогенности опухолевого процесса, длительных операций на грудной и брюшной полости и периодов вынужденной гиподинамии, оцениваются индивидуальные факторы риска, назначаются профилактические дозы антикоагулянтов в периоперационном периоде и во время системной терапии, рекомендуются ранняя активизация, дыхательная гимнастика и упражнения для нижних конечностей, используются компрессионные чулки, при выявлении тромбоза схема переводится в лечебный режим с длительным наблюдением и коррекцией доз в зависимости от функции печени и почек.
Реабилитационная, логопедическая и психоонкологическая терапия дополняют медикаментозные мероприятия на всех этапах, реабилитолог и логопед обучают безопасным техникам глотания, подбору консистенции пищи и положения тела, помогают уменьшить страх удушья и аспирации, постепенно увеличивается двигательная активность с учётом перенесённой операции и химиолучевого лечения, психоонколог работает с тревогой, изменением образа тела, нарушением привычного процесса питания и общения за столом, при необходимости подключаются групповая поддержка и медикаментозная коррекция тревожно-депрессивных расстройств, благодаря такому подходу удаётся сохранить не только физическую, но и социальную и эмоциональную составляющие качества жизни даже при тяжёлом диагнозе.
Какие врачи могут быть вовлечены
- Онколог координирует весь маршрут терапии, сопоставляет данные эндоскопии, КТ, ПЭТ-КТ, морфологии и иммуногистохимии, формирует стадию, оценивает резектабельность, подбирает последовательность неоадъювантной терапии, хирургической, адъювантной терапии и паллиативной терапии, назначает и корректирует системное лечение при местнораспространённом и метастатическом процессе, организует консилиум с участием всех профильных специалистов и ведёт наблюдение после завершения активной терапии.
- Торакальный хирург или торакоабдоминальный хирург отвечает за выбор вида операции, оценивает по снимкам отношение опухоли к трахее, бронхам, аорте, перикарду и диафрагме, планирует трансторакальную или трансхиатальную эзофагэктомию, резекцию зоны пищеводно-желудочного перехода, объём лимфодиссекции и тип реконструкции пищеварительного тракта, выполняет вмешательство с контролем анастомозов и профилактикой дыхательных и гнойно-септических осложнений.
- Эндоскопист проводит первичную эзофагогастродуоденоскопию с биопсией, при ранних стадиях может выполнять эндоскопическую резекцию слизистой или подслизистую диссекцию, при стенозе устанавливает саморасправляющийся стент для восстановления проходимости, участвует в контроле состояния анастомозов и стентов в послеоперационном и паллиативном периодах.
- Радиотерапевт оценивает показания к неоадъювантной, дефинитивной или паллиативной химиолучевой терапии, по данным КТ и ПЭТ-КТ планирует поля облучения на область первичного очага и регионарных лимфоузлов, подбирает суммарную дозу и режим фракционирования, следит за выраженностью лучевого эзофагита и реакций со стороны лёгких и сердца, при необходимости меняет конфигурацию полей и график.
- Химиотерапевт формирует схемы системного лечения в периперационном и метастатическом форматах, выбирает комбинации цитостатиков и таргетных или иммунных препаратов с учётом молекулярного профиля, функции печени и почек, переносимости и сопутствующей патологии, контролирует токсичность, вовремя меняет линию терапии и решает вопрос о переходе к симптомоориентированному подходу.
- Анестезиолог-реаниматолог готовит к объёмным операциям на грудной и брюшной полости, оценивает дыхательный и сердечно-сосудистый резерв, подбирает анестезиологическую тактику, ведёт пациентa в раннем послеоперационном периоде с контролем гемодинамики, вентиляции и дренажей, участвует в лечении дыхательной недостаточности и септических осложнений.
- Диетолог и специалист по нутритивной поддержке оценивают степень истощения, индекс массы тела и лабораторные признаки белково-энергетической недостаточности, подбирают варианты питания через рот, зонд, гастростому или еюностому, рассчитывают калорийность и состав смесей, контролируют динамику массы тела и адаптацию к новым условиям прохождения пищи.
- Логопед и реабилитолог обучают безопасным техникам глотания, подбору консистенции блюд, положению тела во время приёма пищи, формируют программу дыхательной гимнастики и ранней активизации, помогают уменьшить риск аспирации и восстановить выносливость после химиолучевого лечения и хирургических вмешательств.
- Психоонколог и специалист по паллиативной помощи сопровождают на всех этапах, помогают справляться с тревогой, изменением образа тела и привычек питания, выстраивают ступенчатую анальгетическую терапию, организуют контроль симптомов дома, поддерживают семью и участвуют в обсуждении целей лечения при поздних стадиях заболевания.
Какие обследования назначаются
- Общие обследования включают клинический анализ крови с оценкой уровня гемоглобина, лейкоцитарной формулы и тромбоцитов, биохимический анализ с показателями функции печени и почек, электролитами, белком, альбумином, глюкозой и маркёрами воспаления, коагулограмму, общий анализ мочи, ЭКГ, при необходимости эхокардиографию и исследование функции внешнего дыхания, совокупность этих данных позволяет оценить соматический статус, анестезиологический риск и переносимость химиолучевой терапии.
- Эзофагогастродуоденоскопия с множественной биопсией является ключевым методом, позволяет визуально увидеть протяжённость аденокарциномы, степень сужения просвета, наличие изъязвления и кровоточивости, взять материал из разных участков для морфологического и иммуногистохимического исследования, при ранних поражениях оценить пригодность для эндоскопической резекции.
- Эндоскопическое ультразвуковое исследование пищевода даёт послойную картину стенки пищевода, определяет глубину инвазии, вовлечение околопищеводной клетчатки и ближайших лимфоузлов, помогает отличить поверхностную форму от поражения мышечного слоя, что критично для выбора между эндоскопическим и радикальным хирургическим подходом.
- Контрастная КТ органов грудной клетки и брюшной полости используется для стадирования, показывает толщину стенки в зоне опухоли, отношение к трахее, бронхам, аорте, перикарду, выявляет увеличенные средостенные, надключичные и абдоминальные лимфоузлы, метастазы в лёгких, печени и надпочечниках, позволяет оценить резектабельность и спланировать доступ.
- ПЭТ-КТ или КТ всего тела с внутривенным контрастом и расширенным протоколом могут применяться при подозрении на отдалённые метастазы или рецидив, визуализируют метаболически активные очаги в лимфоузлах и органах, помогают отличить рубцовые изменения после лучевой терапии от жизнеспособной опухоли и выбрать оптимальное место для повторной биопсии.
- Рентгеноскопия пищевода с барием используется для оценки конфигурации просвета, длины и характера стриктуры, наличия свищей и нарушений эвакуации, помогает спланировать эндоскопическое стентирование и оценить риск аспирации.
- Бронхоскопия показана при высоком расположении опухоли или по данным КТ о тесном контакте с дыхательными путями, даёт возможность исключить прорастание в трахею и бронхи, выявить свищи и взять материал для исследования при подозрении на синхронный процесс.
- Морфологическое исследование биопсий и операционного материала подтверждает аденокарциному, определяет степень дифференцировки, архитектуру, наличие сосудистой и периневральной инвазии, состояние краёв резекции и количество поражённых лимфоузлов, формирует окончательную стадию и влияет на показания к нео- и адъювантной терапии.
- Иммуногистохимическое и молекулярно-генетическое исследование дополняют стандартную морфологию, оценивают экспрессию потенциальных мишеней для таргетной и иммунотерапии, показатели пролиферации и иммунного ответа, результаты используются при выборе схем системного лечения и прогнозировании чувствительности к отдельным препаратам.
Что важно знать пациентам
Можно ли вылечить аденокарциному пищевода?
Полное излечение возможно при выявлении процесса на стадиях, когда поражение ограничивается стенкой пищевода и регионарными лимфоузлами без отдалённых метастазов, в этой ситуации радикальная операция в сочетании с нео- и адъювантной терапией способна обеспечить длительную ремиссию и фактическое излечение, при более поздних стадиях лечение направлено на максимальное уменьшение опухолевой массы, контроль симптомов, восстановление возможности питания и продление жизни, степень успеха зависит от исходного распространения, общего состояния, полноты проведённых этапов и приверженности назначенной программе.
Дисфагия при аденокарциноме пищевода
Дисфагия при аденокарциноме пищевода формируется постепенно, часто маскируется под обострение гастроэзофагеальной рефлюксной болезни, спазмы или функциональные нарушения, самостоятельное ограничение рациона и длительный приём симптоматических средств приводит к тому, что момент обследования смещается на более поздний срок, когда просвет уже значительно сужен и опухоль вышла за пределы стенки, ранняя эндоскопия при стойком ощущении застревания пищи, болях при глотании или сочетании этих симптомов с похуданием даёт шанс обнаружить заболевание на стадии, когда доступны органосохраняющие эндоскопические вмешательства или радикальная операция с меньшим объёмом.
Питание при аденокарциноме пищевода
Нарушение прохождения пищи по пищеводу быстро приводит к потере массы тела, дефициту белка, витаминов и микроэлементов, в таком состоянии организм хуже переносит химиолучевую терапию и объёмные операции, риск осложнений и несостоятельности швов возрастает, установка эндоскопического стента, наложение гастростомы или еюностомы, подбор высокоэнергетических смесей и обучение безопасному глотанию позволяют стабилизировать массу тела, поддерживать иммунитет и сократить число отмен и отсрочек лечения, поэтому нутритивная поддержка считается таким же важным элементом протокола, как и собственно противоопухолевые вмешательства.
Что делать после онколечения?
После операции и химиолучевой терапии сохраняется риск местного рецидива в области анастомоза, появления новых очагов в лимфоузлах, лёгких, печени и других органах, особенно в первые годы, плановые визиты с осмотром, обсуждением жалоб, контролем массы тела, эндоскопическими и визуализирующими обследованиями позволяют обнаружить рецидив или метастатическое поражение на стадии, когда возможны дополнительные локальные или системные вмешательства, кроме того, во время наблюдения оцениваются отдалённые последствия лечения, состояние сердца и лёгких, выраженность нарушений глотания и питания, при необходимости подключаются диетолог, реабилитолог и психоонколог, что помогает не только контролировать онкологический процесс, но и поддерживать качество жизни.